肥満症の治療標的として期待される「褐色脂肪組織」の新規制御因子を同定
プレスリリース
国立研究開発法人日本医療研究開発機構
発表者
山内 敏正(東京大学医学部附属病院 糖尿病・代謝内科 准教授)
脇 裕典(東京大学医学部附属病院 糖尿病・代謝内科 /東京大学大学院医学系研究科 分子糖尿病科学講座 特任准教授)
油谷 浩幸(東京大学先端科学技術研究センター ゲノムサイエンス分野 教授)
堤 修一(東京大学先端科学技術研究センター ゲノムサイエンス分野 特任准教授)
平池 勇雄(東京大学医学部附属病院 糖尿病・代謝内科 特任研究員)
発表のポイント
- 熱産生によりエネルギーを消費し、またBMIや年齢とその活性が負に相関することから肥満症の治療標的として期待される「褐色脂肪組織」の新規主要制御因子 NFIA(Nuclear factor I-A)を、DNA上のオープンクロマチン領域の解析から同定しました。
- NFIAを欠損させると褐色脂肪の遺伝子プログラムが著しく障害される一方、NFIAを導入すると筋芽細胞やエネルギーの貯蔵を担う白色脂肪細胞においても褐色脂肪の遺伝子プログラムが活性化されました。
- 「エネルギー摂取の抑制」ではなく「エネルギー消費の促進」に基づく肥満症、メタボリックシンドローム、肥満2型糖尿病の新しい治療につながる可能性があります。
発表概要
肥満症とそれに起因するメタボリックシンドロームや肥満2型糖尿病は、心血管疾患、腎疾患や悪性腫瘍のリスクを高めることから、健康寿命の延伸を目指す上で大きな障害です。近年、エネルギーの貯蔵を担う「白色脂肪組織」以外に、熱産生を介してエネルギーを消費する「褐色脂肪組織」がヒト成人にも存在することが分かり、褐色脂肪組織の数や働きを高めることが肥満症の新しい治療法につながり得るとして期待されています。
このたび東京大学医学部附属病院 糖尿病・代謝内科 門脇孝教授、山内敏正准教授、脇裕典特任准教授、平池勇雄特任研究員及び東京大学先端科学技術研究センター ゲノムサイエンス分野 油谷浩幸教授、堤修一特任准教授らの研究グループは、褐色脂肪組織に特異的なDNA上のオープンクロマチン領域の解析から、褐色脂肪組織の新規の主要制御因子としてNFIAを同定しました。NFIAを欠損させたマウスでは褐色脂肪の遺伝子プログラムが著しく障害されていた一方、NFIAを導入した場合には、筋芽細胞や白色脂肪細胞においても褐色脂肪の遺伝子プログラムが活性化されました。更に、ヒト成人の褐色脂肪組織でも白色脂肪組織と比較してNFIA遺伝子が高発現していました。この結果は、NFIAの働きを高めることで「エネルギー摂取の抑制」ではなく「エネルギー消費の促進」に基づく肥満症、メタボリックシンドローム、肥満2型糖尿病の新しい治療につながる可能性があると期待されます。
本研究は国立研究開発法人日本医療研究開発機構の革新的先端研究開発支援事業(AMED‐CREST)「エピゲノム研究に基づく診断・治療へ向けた新技術の創出」研究開発領域における研究開発課題「2型糖尿病・肥満における代謝制御機構とその破綻のエピゲノム解析」(研究開発代表者:山内敏正)の一環で行われました。なお、本研究開発領域は、2015年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。その成果は日本時間2017年8月15日午前0時(英国時間 2017年8月14日16時)に英国科学雑誌 Nature Cell Biology オンライン版に掲載されます。
発表内容
研究の背景
近年、エネルギーの貯蔵を担う「白色脂肪組織」以外に、ミトコンドリアにおけるUCP1(Uncoupling protein-1)タンパク質による熱産生を介してエネルギーを消費する「褐色脂肪組織」がヒト成人にも存在することが分かってきました。既に、BMI(Body mass index、肥満度の指標)と褐色脂肪組織の活性が負に相関すること、また加齢に伴い褐色脂肪組織の活性が低下することが報告されています。褐色脂肪組織の数や働きを高めることが肥満症の新しい治療法につながり得るとして期待されています。
また発生学的な観点において、褐色脂肪組織は白色脂肪組織よりもむしろ骨格筋組織に近い可能性が報告されている一方で、白色脂肪組織も寒冷刺激や交感刺激に応じて褐色脂肪組織に近い機能を持ち得ることが示されており、褐色脂肪組織の分化の全体像には未解決の部分が多く残されています。
ヒトを含む多細胞生物は、同一のDNAを有するにも関わらず形態や機能が異なる様々な細胞の集団として成り立っています。DNAは通常「ヒストン」と呼ばれるタンパク質に巻き付いた状態で存在しており、ヒストンとDNAの複合体は「クロマチン」と呼ばれます。同一のDNAを有するにも関わらず全身の様々な細胞がそれぞれ異なる機能を発揮できるのは、DNAの異なる部分から情報を読み出しているためです。DNAのうち、情報として読み出される部分が「遺伝子」であり、読み出す現象は「転写」と呼ばれます。DNAから情報を読み出す際、DNAはヒストンからほどけて、遺伝子の転写に必要な因子の結合を許すような「オープンクロマチン」構造を取ることが知られています。
研究内容
NFIAを欠損させたマウスでは、熱産生を担うUCP1のみならず褐色脂肪の遺伝子プログラム全体が著しく障害されており、反対に骨格筋の遺伝子プログラムは活性化されていました。一方で、NFIAを導入すると筋芽細胞や白色脂肪細胞においても褐色脂肪の遺伝子プログラムが活性化されました。更に、ヒト成人の褐色脂肪組織でも白色脂肪組織と比較してNFIA遺伝子が高発現しており、その発現は褐色脂肪に特異的な遺伝子の発現と正に相関していることがわかりました。以上から、NFIAはクロマチンの制御を介してPPARγと協調的に褐色脂肪の遺伝子プログラムを活性化する転写因子と考えられました。
社会的意義
発表雑誌
- 雑誌名:
- Nature Cell Biology(オンライン版に日本時間8月15日に掲載)
- 論文タイトル:
- NFIA co-localizes with PPARγ and transcriptionally controls the brown fat gene program
- 著者:
- Yuta Hiraike, Hironori Waki*, Jing Yu, Masahiro Nakamura, Kana Miyake, GakuNagano, Ryo Nakaki, Ken Suzuki, Hirofumi Kobayashi, Shogo Yamamoto, Wei Sun,Tomohisa Aoyama, Yusuke Hirota, Haruya Ohno, Kenji Oki, Masayasu Yoneda,Andrew P. White, Yu-Hua Tseng, Aaron M. Cypess, Therese J. Larsen, Naja Z.Jespersen, Camilla Scheele, Shuichi Tsutsumi, Hiroyuki Aburatani*, ToshimasaYamauchi* and Takashi Kadowaki*(*責任著者)
- DOI番号:
- 10.1038/ncb3590
添付資料
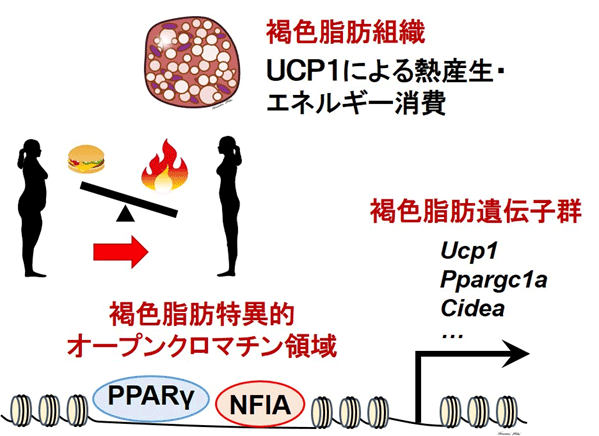
本研究の概念図
NFIAは褐色脂肪特異的なオープンクロマチン領域においてPPARγと協調して働く、褐色脂肪組織の新規かつ主要な制御因子であり、NFIAの働きを高めることで「エネルギー摂取の抑制」ではなく「エネルギー消費の促進」に基づく肥満症の新しい治療につながる可能性がある (Nature Cell Biology本論文より引用・改変)
お問い合わせ先
研究内容に関するお問い合せ先
東京大学医学部附属病院 糖尿病・代謝内科
教授 門脇 孝(かどわき たかし)
TEL:03-5800-8815(直通)FAX:03-5800-9797
E-mail:kadowaki-3im“AT”h.u-tokyo.ac.jp
東京大学医学部附属病院 糖尿病・代謝内科
准教授 山内 敏正(やまうち としまさ)
TEL:03-3815-5411(代表)内線:36638
E-mail:tyamau-tky“AT”umin.net
東京大学先端科学技術研究センター ゲノムサイエンス分野
教授 油谷 浩幸(あぶらたに ひろゆき)
TEL:03- 5452-5352(直通)FAX:03- 5452-5259
E-mail:haburata-tky“AT”umin.ac.jp
広報担当者連絡先
東京大学医学部附属病院
パブリック・リレーションセンター(担当:渡部、小岩井)
TEL:03-5800-9188(直通)
E-mail:pr“AT”adm.h.u-tokyo.ac.jp
東京大学先端科学技術研究センター
広報・情報室(担当:村山)
TEL:03-5452-5424(直通)
E-mail:press“AT”rcast.u-tokyo.ac.jp
事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
TEL:03-6870-2224 FAX:03-6870-2243
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成29年8月15日
最終更新日 平成29年8月15日


