矯正歯科治療において歯の移動の新たな鍵となる細胞を同定―矯正歯科治療の標的細胞が明らかに―
プレスリリース
国立研究開発法人日本医療研究開発機構
ポイント
- 矯正歯科治療における歯の移動では、今まで破骨細胞による歯槽骨(注1)の吸収が重要な役割を果たすことが知られていました。
- 破骨細胞の分化に不可欠なRANKL(注2)産生を、歯槽骨においては骨細胞が担うことを今回新たに発見しました。
- 骨細胞特異的にRANKLを欠損させたマウスでは、歯に矯正力を加えても破骨細胞の出現が抑制され、歯の移動量も減少しました。
- この発見は、骨細胞を標的とした新たな治療法の開発につながることが期待されます。
東京医科歯科大学大学院医歯学総合研究科 分子情報伝達学分野の中島 友紀教授と同大学院 顎顔面矯正学分野の森山 啓司教授、庄司 あゆみ大学院生らの研究グループは、東京大学の研究グループと共同研究で、歯科矯正学的な歯の移動に骨細胞が産生するRANKLが重要な役割を担うことを明らかにしました。
この研究は国立研究開発法人日本医療研究開発機構 (AMED) 革新的先端研究開発支援事業(AMED-CREST) 「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「骨恒常性を司る骨細胞のメカノ・カスケードの解明」(研究開発代表者:中島友紀)、科学技術振興機構(JST) 戦略的創造研究推進事業(さきがけ)、文部科学省・科学研究費補助金などの支援のもとで行われたもので、その研究成果は、国際科学誌Scientific Reportsに、2017年8月18日午前10時(米国東部時間)にオンライン版で発表されました。
研究の背景
研究成果の概要
そこで、骨細胞特異的なRANKL欠損マウスを作出し、歯科矯正学的な歯の移動モデルを用いて実験を行ったところ、圧迫側における破骨細胞数が減少し、歯の移動量が有意に低下することが明らかになりました(図1)。加えて、RANKLを標的とした中和抗体OYC1を歯根周囲の歯槽骨に投与すると、歯の移動が有意に減少することも見出されました。以上より、骨細胞の発現するRANKLが歯の移動に重要な役割を担っていることを世界に先駆け明らかにしました(図2)。
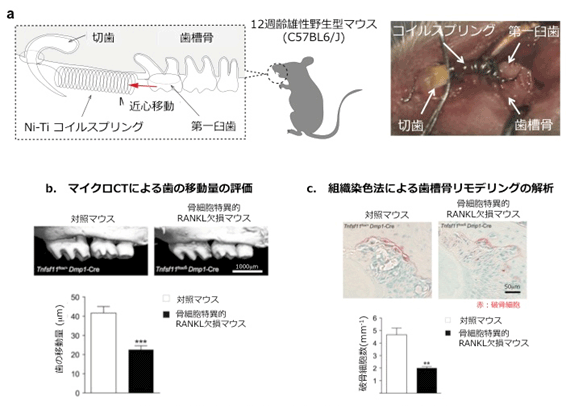 図1 骨細胞特異的RANKL欠損マウスにおける歯の移動量および破骨細胞数の比較
図1 骨細胞特異的RANKL欠損マウスにおける歯の移動量および破骨細胞数の比較
b.マイクロCTによる歯の移動量の評価。骨細胞特異的RANKL欠損マウスでは、歯の移動量が有意に減少した。
c.組織染色法による歯槽骨リモデリングの解析。骨細胞特異的RANKL欠損マウスでは、破骨細胞(図中の赤の細胞)が有意に減少した。
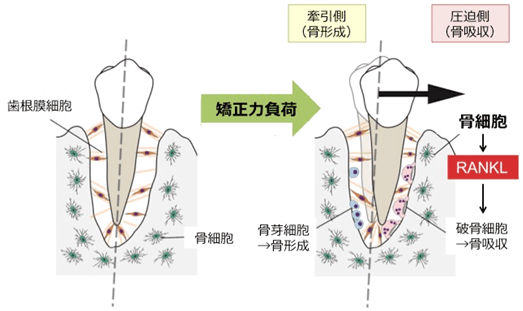 図2 矯正力負荷時の歯の移動のメカニズム
図2 矯正力負荷時の歯の移動のメカニズム
研究成果の意義
本研究の成果が、より精密な歯の移動の制御を可能にし、今後の矯正歯科治療における骨細胞を標的とした新規治療法開発の分子基盤の確立につながることが期待されます。
用語の説明
- (注1)歯槽骨:
- 歯を取り囲み支持している骨。歯周組織の一部。
- (注2)RANKL:
- 破骨細胞分化促進因子。破骨細胞の分化に必須であり、生体内では骨細胞、骨芽細胞をはじめ様々な細胞が発現する。
論文情報
- 掲載誌:
- 国際科学誌 Scientific Reports
- 論文タイトル:
- Osteocyte regulation of orthodontic force-mediated tooth movement via RANKL expression
問い合わせ先
研究に関すること
国立大学法人東京医科歯科大学大学院医歯学総合研究科
顎顔面矯正学分野 森山 啓司(モリヤマ ケイジ)
TEL:03-5803-5534 FAX:03-5803-5534
E-mail:k-moriyama.mort“AT”tmd.ac.jp
分子情報伝達学分野 中島 友紀(ナカシマ トモキ)
TEL:03-5803-5474 FAX:03-5803-0193
E-mail:naka.csi“AT”tmd.ac.jp
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm“AT”tmd.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2224
E-mail:kenkyuk-ask“AT”amed.go.jp
※Emailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成29年8月28日
最終更新日 平成29年8月28日


