中国の患者から分離された高病原性H7N9鳥インフルエンザウイルスの特性を解明
プレスリリース
東京大学 医科学研究所
国立研究開発法人日本医療研究開発機構
発表者
発表のポイント
- 2013年に出現したH7N9鳥インフルエンザウイルスが2016年後半に高病原性に変異し、さらに人に感染し死に至らしめた。この高病原性H7N9鳥インフルエンザウイルスの性状を解明するため、哺乳類を用いて感染伝播実験を行った。
- 高病原性H7N9鳥インフルエンザウイルスは、哺乳類間で飛沫感染すること、哺乳類に対して致死的な感染を引き起こすことが分かった。
- 高病原性H7N9鳥インフルエンザウイルスの性状が解明されたことで、本ウイルスに由来するインフルエンザ・パンデミックへの対策が大きく進展する。
発表概要
東京大学医科学研究所感染・免疫部門ウイルス感染分野の河岡義裕教授らの研究グループは、中国で発生した高病原性H7N9鳥インフルエンザウイルス(注1、2)の性状を明らかにしました。
2013年に中国で低病原性H7N9鳥インフルエンザウイルスのヒト感染例が確認されて以来、現在までに1,500名を超える感染者が報告されています。2017年2月、世界保健機関(WHO)は中国において、高病原性H7N9鳥インフルエンザウイルスの感染者が2名発生したと発表しました。家禽に対して致死的な全身感染を引き起こす高病原性鳥ウイルスは、低病原性鳥ウイルスと比べて哺乳類に対する病原性も高いことが知られています。しかし、今回の高病原性H7N9鳥ウイルスが哺乳類に対してどのような病原性を持っているのか、また哺乳類から哺乳類に伝播する能力を持っているのかは明らかにされていませんでした。高病原性H7N9鳥ウイルスの性状解明は、今後のインフルエンザ対策を遂行する上で、緊急に取り組まなければならない課題となっています。
本研究グループは今回、中国の患者から分離された高病原性H7N9鳥ウイルスに関する性状解析を行いました。その結果、高病原性H7N9鳥ウイルスは、哺乳類で効率よく増殖できること、フェレットの間で飛沫感染する能力を持つこと、フェレットに対して致死的な感染を引き起こすことが分かりました。さらに、このウイルスは伝播によって感染したフェレットを死に至らしめることも分かりました。すなわち、この結果は体内に入ったウイルスが少量であってもフェレットは重症化して死に至ることを示しています。また、高病原性H7N9鳥ウイルスは臨床現場で用いられている抗インフルエンザ薬(注3)に対する感受性が低いことも動物実験で明らかとなりました。従って、高病原性H7N9鳥ウイルスによる世界的大流行(パンデミック)が起これば、甚大な健康被害をもたらす可能性が高いと予想されます。
本研究成果は、今後のインフルエンザ・パンデミック対策計画を策定、実施する上で、重要な情報となります。
本研究成果は、2017年10月19日(米国東部時間 午後12時)、米国科学雑誌「CellHost&Microbe」のオンライン速報版で公開されます。
なお本研究は、東京大学、国立感染症研究所、米国ウィスコンシン大学、米国スクリプス研究所が共同で行ったものです。本研究成果は、日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業、文部科学省新学術領域研究などの一環として得られました。
発表内容
➀研究の背景・先行研究における問題点
2013年に低病原性H7N9鳥インフルエンザウイルスのヒト感染例が中国で確認されて以来、高い死亡率を伴うヒト感染例が同国を中心に毎年報告されています。国連食糧農業機関(FAO)の報告によると、2017年9月20日時点で1,589例の感染者が確認され、そのうちの616名が死亡しています。一方、低病原性H7N9鳥ウイルスの変異によって生まれた高病原性H7N9鳥ウイルスが2016年末に中国において家禽から検出されました。さらに2017年2月、同国で初めて、高病原性H7N9鳥ウイルスのヒトへの感染事例が2件報告され、その後も30名近い感染者が確認されています。現時点では感染経路は不明ですが、高病原性H7N9鳥ウイルスは低病原性H7N9鳥ウイルスと同様に鳥からヒトに直接感染したと考えられています。一般的に、鳥インフルエンザウイルスはヒトに感染しにくく、感染したとしてもヒトからヒトへの伝播が起こりにくいため、これまでのところパンデミックの発生には至っていません。しかし、今後もH7N9鳥インフルエンザウイルスのヒトへの感染が繰り返されることで、同ウイルスがよりヒトへの適応性を高め、その結果ヒトの間で容易に伝播するパンデミックウイルスへと変わる恐れがあります。
インフルエンザウイルスの感染や伝播には、ウイルスが宿主細胞に結合し侵入する時の効率が大きく関わっています。そのような性質を決めるのが、ウイルス粒子表面にあるHAたんぱく質(注4、以下、HA)です(図1)。すなわち、ヒト型レセプター(受容体、注5)を認識するHAを持つウイルスは、ヒトで効率よく感染し、伝播する可能性が高くなります。実際、これまでに世界的に大流行した1918年から1919年のスペイン風邪(H1N1)ウイルス、1957年のアジア風邪(H2N2)ウイルスおよび1968年の香港風邪(H3N2)ウイルスにおいて、もとは鳥型レセプターを認識していたHAが、ヒト型レセプターを認識するようになったため、ヒトでパンデミックを起こしたことが知られています。患者から分離された高病原性H7N9鳥ウイルスの遺伝子解析の結果から、HAには鳥ウイルスのヒト型レセプターへの認識を高めるアミノ酸変異があること、さらにウイルスの増殖に大きな役割を担っているウイルスポリメラーゼたんぱく質には、鳥ウイルスの哺乳類細胞での増殖効率を高めるアミノ酸変異があることが分かりました。
このように、ヒトから分離された高病原性H7N9鳥ウイルスが、ヒトへの適応に関わる変異を既に持っていることを考えると、このウイルスがヒトでパンデミックを起こす恐れがあることを示しています。従って、今回中国で出現した高病原性H7N9鳥ウイルスの哺乳類に対する病原性や哺乳類間での伝播力を調べることは急務です。
➁研究内容
本研究グループは、中国の患者から分離された高病原性H7N9鳥ウイルスのin vitro(試験管内の細胞)とin vivo(生体内)における性状解析を行い、2013年に中国の患者から分離された低病原性H7N9鳥ウイルスの性状と比較しました。ウイルスのレセプター結合特異性を調べたところ、高病原性H7N9鳥ウイルスは鳥型レセプターとヒト型レセプターの両方を認識することが分かりました。
マウスを用いた実験では、高病原性H7N9鳥ウイルスは呼吸器や脳など多種類の臓器で増殖したのに対し、低病原性H7N9鳥ウイルスは呼吸器のみで増殖しました。このように高病原性H7N9鳥ウイルスは低病原性H7N9鳥ウイルスよりもマウスに対して強い病原性を示すことが分かりました。
次に、インフルエンザ感染のモデル動物であるフェレットを用いて、高病原性H7N9鳥ウイルスの病原性および伝播力を調べる実験を行いました。その結果、高病原性H7N9鳥ウイルスは肺や脳で良く増殖し、フェレットを殺すことが分かりました(図2)。それに対して、低病原性H7N9鳥ウイルスを感染させたフェレットは一匹も死にませんでした。また、高病原性H7N9鳥ウイルスはフェレット間で飛沫感染すること、その伝播によって感染したフェレットも殺すことが明らかになりました(図2)。このことは、体内に入ったウイルスが少量であってもフェレットは感染し重症化して死に至ることを示しています。
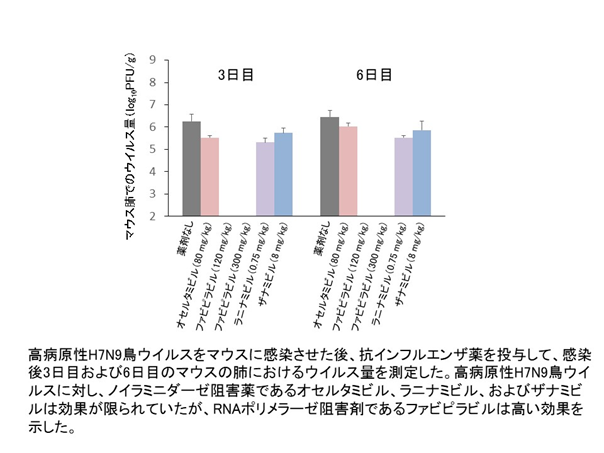
最後に既存の抗インフルエンザ薬に対する感受性を調べたところ、高病原性H7N9鳥ウイルスは、ノイラミニダーゼ阻害剤に対する感受性がマウスを用いた実験では比較的低いことが明らかとなりました(図3)。それに対して、インフルエンザウイルスのRNAポリメラーゼ活性を阻害する薬剤はウイルスの増殖を抑制しました。
➂社会的意義
今回の研究から、中国でヒトから分離された高病原性H7N9鳥ウイルスは、1)哺乳類で良く増殖できる能力を持つこと、2)感染したフェレットが死亡するなど哺乳類に対して高い病原性を示すこと、3)フェレット間で飛沫感染すること、4)動物実験では既存のノイラミニダーゼ阻害剤に対する感受性が低いことが明らかとなりました。そのため、ひとたびパンデミックが起これば、甚大な健康被害とそれに伴う大きな社会・経済活動の混乱が生じる可能性があると予想されます。本研究を通して得られた成果は、将来のパンデミック出現予測や感染拡大阻止に役立つだけでなく、高病原性H7N9鳥ウイルスに対するワクチンの備蓄・製造方針の決定など今後のインフルエンザ・パンデミック対策計画を策定、実施する上で、重要な情報となります。
発表雑誌
- 雑誌名:
- Cell Host & Microbe(10月19日オンライン版)
- 論文タイトル:
- A highly pathogenic avian H7N9 influenza virus isolated from a human is lethal in some ferrets infected via respiratory droplets
- 著者:
- 河岡 義裕
問い合わせ先
研究に関するお問い合わせ
東京大学医科学研究所 感染・免疫部門ウイルス感染分野
教授 河岡 義裕(カワオカ ヨシヒロ)
Tel:03-5449-5310
E-mail:kawaoka“AT”ims.u-tokyo.ac.jp
報道に関するお問い合わせ
東京大学医科学研究所 国際学術連携室URA
Tel:03-6409-2027
国立研究開発法人日本医療研究開発機構(AMED)
経営企画部 企画・広報グループ
Tel:03-6870-2245
AMEDの事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 感染症研究課
〒100-0004 東京都千代田区大手町1-7-1
Tel:03-6870-2225
E-mail:kansen“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
用語解説
- (注1)インフルエンザウイルス
- A型、B型、C型、D型と4種類に分かれるインフルエンザウイルスの中で、ウイルスが変化しやすく過去に何度か世界的大流行(パンデミック)を起こしてきたA型インフルエンザウイルスは、ウイルス表面にある2つの糖たんぱく質、ヘマグルチニン(HA)とノイラミニダーゼ(NA)の抗原性(抗体物質と結合することができる性質)の違いにより、さらに細かく亜型が分類されている。現在までに、HAでは18種類(H1からH18)、NAでは11種類(N1からN11)の亜型が報告されている。H7N9というのは、H7亜型、N9亜型に分類されるA型インフルエンザウイルスのこと。
- (注2)鳥インフルエンザウイルス
- 鳥インフルエンザはA型インフルエンザウイルスを原因として起こる鳥の病気である。鳥インフルエンザウイルスは家禽に対する病原性を指標に、低病原性と高病原性の2つのカテゴリーに分類される。低病原性鳥ウイルスに感染した家禽は無症状か軽い呼吸器症状、下痢、産卵率の低下を示す程度であるが、高病原性鳥ウイルスでは重篤な急性の全身症状を呈して、ほぼ100%の家禽が死亡する。
- (注3)抗インフルエンザ薬
- インフルエンザウイルス粒子表面にある糖たんぱく質ノイラミニダーゼ(NA)の機能を阻害する薬剤のことで、インフルエンザウイルスの増殖を抑制する。ノイラミニダーゼ阻害剤には、オセルタミビル、ザナミビル、ラニナミビル、ペラミビルがある。インフルエンザウイルスのRNAポリメラーゼ活性を阻害する薬剤(ファビピラビル)が2014年に認可されたが、副作用の問題から、その使用はパンデミック発生時のみに限られている。
- (注4)HAたんぱく質
- ウイルス膜表面たんぱく質の1つで、HA(ヘマグルチニン)が動物細胞の表面にあるレセプター(受容体)と結合することで、ウイルス粒子が細胞に取り込まれ、感染が開始される。
- (注5)レセプター(受容体)
- 一般に、外界からの刺激や情報を受け取るための細胞表面にある分子、またはその複合体のことをいう。インフルエンザウイルスは、レセプターとして細胞表面にあるシアル酸と結合する。
添付資料
図1 A型インフルエンザウイルスの模式図
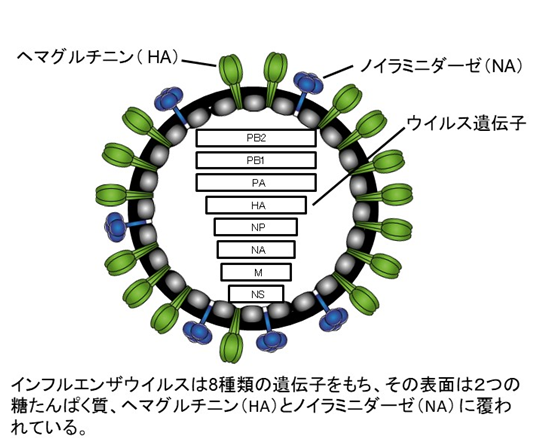
図2 フェレットを用いたウイルス感染伝播実験
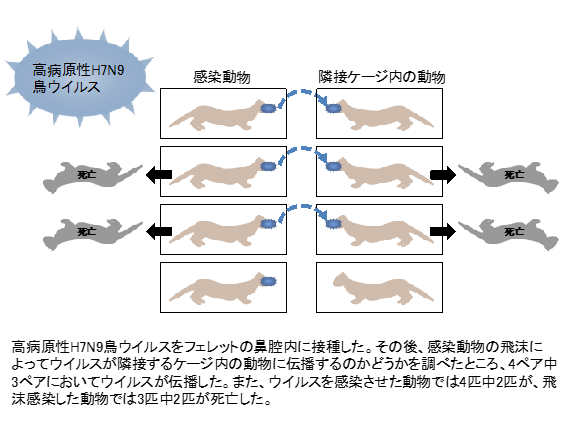
図3 高病原性H7N9島インフルエンザウイルスに対する抗インフルエンザ薬の効果
掲載日 平成29年10月20日
最終更新日 平成29年10月20日


