アレルギー性気管支肺アスペルギルス症の悪化機構を解明
プレスリリース
秋田大学
国立研究開発法人日本医療研究開発機構
秋田大学大学院医学系研究科 総合診療・検査診断学講座の植木 重治 准教授らの研究グループは、ブラジルなどの研究チームと共同で、アレルギー性気管支肺アスペルギルス症と呼ばれる難治性疾患が悪化する仕組みを明らかにしました。
研究分野の背景とこれまでの研究の問題点
自然界に広く存在するカビ(真菌)の一種であるアスペルギルスは、通常人に対して病原体とはなりにくい菌です。しかし、一部の喘息患者さんの中に、アスペルギルスが気管支に定着し、過敏反応が強く出ることで重症化する方がいらっしゃいます。この「アレルギー性気管支肺アスペルギルス症」では、喘息の特徴である咳や喘鳴(ゼイゼイ,ヒューヒューする呼吸)に加え、血痰や食欲不振が出現したり、気管支や肺が破壊され元に戻らなくなったりすることがあります。
通常の喘息とは異なり、アレルギー性気管支肺アスペルギルス症では、非常に粘性の高い痰である「粘液栓」によって気管支が詰まって病気の悪化につながっていることが知られていましたが、その詳しいメカニズムはこれまでわかっていませんでした。
成果の要点
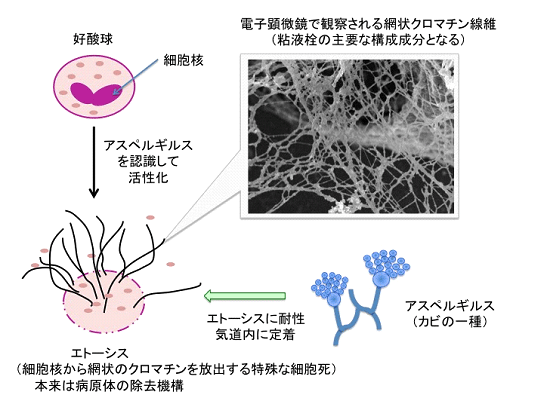
はじめに研究チームは、粘液栓に多く見られる白血球の一種である「好酸球」に注目し、病気の患者さんたちから採取した粘液栓を詳しく観察しました。この結果、全ての患者さんの粘液栓において、好酸球はエトーシス(ETosis)と呼ばれる特殊な細胞死を起こしていることが明らかになりました。エトーシスをおこした好酸球からは、粘性の高い線維状のクロマチン(細胞核に存在するDNAと蛋白の複合体)が大量に放出され、粘液栓が形成されていました。
そこでブラジルの研究チームと協力し、気管支においてどのようにエトーシスが起きるのかを、血液から分離採取した好酸球を用いて詳細に検討しました。この結果、好酸球はアスペルギルスに対して直接反応し、細胞表面のCD11bや細胞内のSykと呼ばれる蛋白を介して活性化することで、エトーシスに至ることがわかりました。また、エトーシスを起こした好酸球は種々の殺菌作用を有する蛋白を放出するものの、アスペルギルスはこれらに耐性を有していることも明らかになりました。
今後の展開と社会へのインパクトやアピールポイント
近年になって喘息治療は進歩していますが、アレルギー性気管支肺アスペルギルス症のように重症化する患者さんの治療方法が十分でないことが大きな課題になっています。今回の研究は、重症化の原因となる粘液栓の形成機構を、気管に定着した真菌に対する過剰な生体反応と、真菌の耐性という面から科学的に明らかにしたものです。
この研究結果から、詰まりやすい粘液栓の原因になっているクロマチン繊維の除去、好酸球の活性化とエトーシスの制御といった、これまでにない新しい治療方法が開発されることが期待されます。
本研究は国立研究開発法人日本医療研究開発機構の免疫アレルギー疾患等実用化研究事業(免疫アレルギー疾患実用化研究分野)「アレルギー性気管支肺真菌症の新・診断基準の検証と新規治療開発(研究代表者:浅野浩一郎)」の一環として行われました。東海大学、国立病院機構東京病院、リオデジャネイロ連邦大学などとの共同研究であり、2017年9月21日に米国アレルギー・喘息・免疫学会誌「Journal of Allergy and Clinical Immunology」のオンライン速報版で公開されました。
お問い合わせ先
本研究に関するお問い合わせ
秋田大学大学院医学系研究科 総合診療・検査診断学講座
TEL:018-884-6209
AMED事業に関するお問い合わせ先
日本医療研究開発機構 戦略推進部難病研究課
〒100-0004 東京都千代田区大手町1-7-1
Tel:03-6870-2223 Fax:03-6870-2243
E-mail:nambyo-i“AT”amed.go.jp
※E-mailは上記アドレス"AT"の部分を@に変えてください。
掲載日 平成29年11月16日
最終更新日 平成29年11月16日


