カフェインとその代謝産物がパーキンソン病診断のバイオマーカーになる―血液による診断とカフェイン補充治療への期待―
プレスリリース
順天堂大学
国立研究開発法人日本医療研究開発機構
概要
順天堂大学大学院医学研究科・神経学講座(脳神経内科)の藤巻基紀大学院生、斉木臣二准教授、服部信孝教授らの研究グループは、パーキンソン病*1患者血清中のカフェイン*2及びカフェイン代謝産物*39種がパーキンソン病診断のバイオマーカーになりうることを明らかにしました。本成果はパーキンソン病の簡便・低侵襲な診断精度向上に寄与するとともに、体内への吸収方法を改善・工夫したカフェイン投与による予防や治療の可能性に繋がるものと期待されます。本研究は、米国科学雑誌「Neurology」のオンライン版(日本時間2018年1月4日)で公開されました。
本研究成果のポイント
- パーキンソン病患者(軽症~重症)の血中のカフェイン及びカフェイン代謝産物9種の低下を発見
- カフェイン及びカフェイン代謝産物はパーキンソン病診断の新規バイオマーカーになりうる
- カフェイン投与によるパーキンソン病の新規予防・治療法の開発へ
背景
パーキンソン病は有病率が10万人あたり140人に上るわが国で2番目に多い神経変性疾患で、運動に関する症状(手足・首が震える、手足がこわばる、転びやすくなる)が徐々に進行することが特徴的とされています。最近の研究より、パーキンソン病患者の中脳黒質神経細胞数の減少が、上記症状発現の少なくとも10年以上前から進行していることが明らかになっており、できるだけ早期にその予兆を見つけ、治療介入する「先制医療」の重要性が示唆されています。
一方、2002年頃からカフェインの適切量(コーヒー1日1-2杯程度)の摂取がパーキンソン病発症予防効果を示すことが複数の疫学的研究からわかってきましたが、そのメカニズムは不明でした。
そこで、私たち研究グループは、実際に疾病を発症したパーキンソン病患者で、カフェインがどのように吸収され、どのように代謝されているかを明らかにすることがパーキンソン病に対するカフェイン作用を解明する手がかりになると考えました。まず、実際のパーキンソン病患者血清を調べた結果、血中のカフェイン濃度が低下していることを突き止めました。また、今回の研究では、パーキンソン病患者のカフェイン代謝変化の全体像に迫るため、さらに病期・重症度との関連をカフェインとその代謝産物全てに拡張して評価し、併せて代謝酵素遺伝子の関与を調べることにより、それらのパーキンソン病診断バイオマーカーとしての有用性を検討しました。
内容
今回の研究では、まず軽症から重症までのそれぞれのパーキンソン病患者の血清カフェイン及びカフェイン代謝産物濃度とカフェイン代謝関連酵素(シトクロムP450)*3遺伝子一塩基多型(SNP*4)との関連を検討しました。なお、血液中代謝産物は採血前の運動・食事、基礎疾患(膠原病、腫瘍、肺炎など)に大きく影響されるため、採血条件を統一し、厳密な条件のもと、パーキンソン病患者108名、健常者31名から採取した血清(0.5ミリリットル)を用いて、液体クロマトグラフィー装置と質量分析計によるカフェインおよびその下流代謝産物10種の濃度を測定しました。
代謝産物測定の結果、パーキンソン病群ではカフェインおよびその直下代謝産物3種(テオフィリン・テオブロミン・パラキサンチン)、更にその下流代謝産物6種が有意に低下していました(図表1)。次に、カフェイン摂取量とカフェイン濃度の関係を調べたところ、健常者ではカフェイン摂取量に比例してカフェイン血中濃度が高いのに比し、パーキンソン病患者ではその相関が弱くなっていました。さらに、カフェインの分解に関わる遺伝子であるCYP1A2、CYP2E1 *3について既報告のSNPをゲノムDNAを用いて調べたところ、パーキンソン病患者群と健常者群に有意な変化を認めませんでした。以上から、パーキンソン病患者ではカフェインの分解促進ではなく、吸収低下により血中濃度が低下し、その保護的な効果が得られにくい状況が生じていると推察されました。
パーキンソン病群において重症度を問わずカフェインとその下流代謝産物が低下していたという結果から、カフェイン、カフェインと直下代謝産物3種、カフェインと下流代謝産物9種の各濃度の組み合わせによりパーキンソン病を極めて高確率で診断できる(図表2)ことがわかり、バイオマーカーとしての有用性を実証することができました。
今後の展開
侵襲の低い採血から得られるごく微量の血液成分がパーキンソン病の診断マーカーとして利用できれば、現在の診断を正確で簡便かつスピーディにすることができます。さらに運動障害などからみる従来の診断法で判定のつきにくい早期のパーキンソン病を精度高く診断できれば、超早期の前臨床期・前駆症状期における発症前診断に繋がり、早い段階から進行を食い止めたり、予防としての先制医療の一助となるものと期待されます。
加えて、パーキンソン病患者では腸管からのカフェイン吸収障害が想定されるため、他の経路からの適切量のカフェイン投与がパーキンソン病進行抑制、発症予防に繋がる可能性があります。これは、患者では吸収しにくいカフェインをカフェイン構造の改変または経皮的投与などの工夫によって治療効果を得ることを目的とし、研究グループでは、その有効性の検討を進め、パーキンソン病の新たな治療法の開発も目指しています。
| 代謝産物名 | 健常者平均 ± 標準偏差 (LLD) | パーキンソン病患者 平均 ± 標準偏差 (LLD) | p値 |
|---|---|---|---|
| Caffeine | 79.10 ± 91.5 (2) | 23.53 ± 22.4 (4) | <0.0001 |
| Theophylline | 14.40 ± 12.1 (2) | 6.01 ± 4.7 (6) | <0.0001 |
| Theobromine | 48.65 ± 46.9 (2) | 24.50 ± 32.1 (5) | 0.0004 |
| Paraxanthine | 73.71 ± 59.5 (2) | 30.70 ± 23.9 (3) | <0.0001 |
| 1,7-dimethyluric acid | 1.59 ± 1.0 (2) | 0.47 ± 0.6 (53) | <0.0001 |
| 1-methylxanthine | 1.47 ± 0.9 (2) | 0.70 ± 0.7 (23) | <0.0001 |
| 3-methylxanthine | 2.94 ± 3.3 (2) | 1.44 ± 1.8 (30) | 0.0005 |
| 1-methyluric acid | 2.44 ± 2.0 (4) | 1.97 ± 2.1 (41) | 0.1351 |
| 7-methylxanthine | 3.11 ± 2.9 (2) | 1.63 ± 1.5 (15) | 0.0004 |
| AFMU | 2.17 ± 1.5 (2) | 0.61 ± 0.5 (27) | <0.0001 |
| AAMU | 1.00 ± 0.8 (2) | 0.548 ± 0.5 (21) | 0.0005 |
各代謝産物の中でパーキンソン病群で有意に上昇した10化合物と軽度上昇した1-methyluric acidの平均値±標準偏差を示します。なおパーキンソン病で低下傾向を示すものの有意差を認めなかった1-methyluric acidについては測定限界以下を示した症例数が多く見られたことも影響していると考えられます。(赤字は患者群で有意に低下した化合物を示す。LLD: lower limit of detection, 測定限界以下を示した症例数)
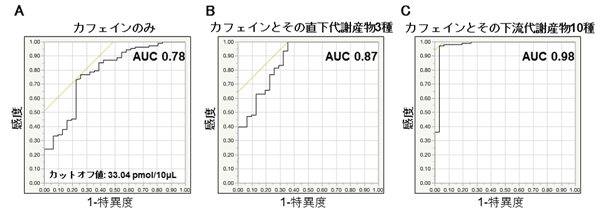
図表2:カフェイン及びその代謝産物濃度を用いたパーキンソン病診断価値の検討
- カフェイン濃度のみを用いたROC(Receiver Operating Characteristics)曲線分析*5では、AUC(Area of under the curve)=0.78と比較的高い確率でパーキンソン病であることを診断できると考えられます。
- カフェイン及びその直下代謝産物3種を用いたROC分析では、AUC=0.87とさらに高い診断確率を得ることができます。
- 今回測定したカフェインを含む全化合物を用いたROC分析では、AUC=0.98とさらに高い診断確率を得ることができます。
用語解説
- *1 パーキンソン病:
- 進行性の中脳黒質神経細胞脱落を特徴とする神経変性疾患で、現在のわが国の患者数は14万人とされるが、高齢になるほど発症率が高まるため、2030年には全世界で3000万人が罹患すると予測されている。
- *2 カフェイン:
- 世界中で最も消費されている精神興奮作用を持つ化合物で、アデノシン受容体(A1およびA2Aサブタイプ)拮抗作用を持ち、本作用により神経細胞への興奮作用を示すとされる。カフェインはヒト体内で合成することはできず、シトクロムP450であるCYP1A2によりその95%が分解される。心血管系への作用、抗腫瘍作用、神経保護作用等が報告されているが、とくに男性パーキンソン病患者での発症予防・症状改善効果が強く示唆されている。
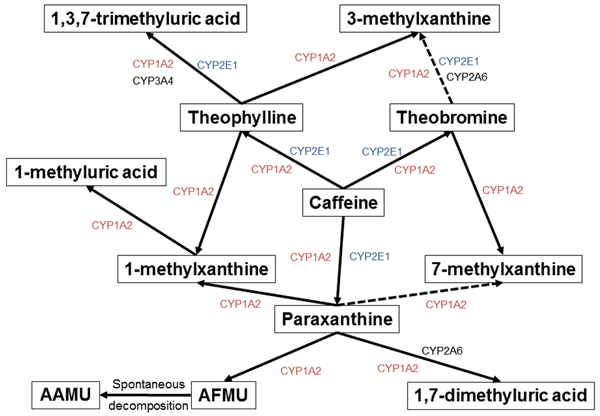
- *3 カフェイン代謝産物と代謝酵素(下図):
- 外界から摂取したカフェインは、その約80%がparaxanthineに、残りの20%がtheophyllineまたはtheobromineに代謝され、それを担う主な酵素がCYP(シトクローム)1A2およびCYP2E1である。Paraxanthine、theopylline、theobromineはさらにCYP酵素によって下流代謝産物に分解される。
- *4 一塩基多型(single nucleotide polymorphisma(SNP)):
- 一つの種におけるゲノムDNAの塩基配列に一塩基が変異した多様性が認められ、その変異頻度が集団内で1%以上認められるとき、この変異を一塩基多型と呼ぶ
- *5 ROC(Receiver Operating Characteristics)曲線分析:
- 縦軸を感度、横軸を偽陽性率(1-特異度)を尺度としてカットオフ値を変動させながらプロットした曲線図。連続変数で得られる検査値の診断価値を評価する際に用いられる。曲線下面積(Area of under the curve)は0.5-1.0の間の値を取り、1に近いほど診断能力が高いと判断される。
論文
本研究成果は、米国科学雑誌の「Neurology」誌のオンライン版(日本時間2018年1月4日6時)で公開されました。
- 英文タイトル:
- Serum caffeine and metabolites are reliable biomarkers of early Parkinson’s disease.
- 日本語訳:
- 血清カフェインとその代謝産物は早期パーキンソン病診断バイオマーカーである
- 著者:
- Motoki Fujimaki, Shinji Saiki, Yuanzhe Li, Naoko Kaga, Hikari Taka, Taku Hatano, Kei-Ichi Ishikawa, Yutaka Oji, Akio Mori, Ayami Okuzumi, Takahiro Koinuma, Shin-Ichi Ueno, Yoko Imamichi, Takashi Ueno, Yoshiki Miura, Manabu Funayama, Nobutaka Hattori Neurology 2018;90:1-8.
- DOI:
- 10.1212/WNL.0000000000004888
謝辞
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出」*(研究開発総括:清水孝雄)における研究開発課題「パーキンソン病の代謝産物バイオマーカー創出およびその分子標的機構に基づく創薬シーズ同定」(研究開発代表者:服部信孝)の一環で行われたと共に、文部科学省私立大学戦略的研究基盤形成支援事業、文部科学省新学術領域研究領域提案型「オートファジーの集学的研究」、およびJSPS科研費(JP15H04843)による支援を受けて行われました。 *本研究開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。 また、本研究に協力頂きました患者さんのご厚意に深謝いたします。
お問い合わせ先
研究内容に関するお問い合せ先
順天堂大学大学院 医学研究科 神経学講座
教授 服部 信孝 (はっとり のぶたか)
E-mail:nhattori"AT"juntendo.ac.jp
准教授 斉木 臣二 (さいき しんじ)
E-mail:ssaiki"AT"juntendo.ac.jp
TEL:03-3813-3111(大代表)
順天堂大学医学部附属順天堂医院 脳神経内科のHP
AMED事業に関するお問い合せ先
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
TEL:03-6870-2224 FAX:03-6870-2243
E-mail:kenkyuk-ask"AT"amed.go.jp
取材に関するお問い合せ先
順天堂大学 総務局 総務部 文書・広報課
担当:長嶋 文乃 (ながしま あやの)
TEL:03-5802-1006 FAX:03-3814-9100
E-mail:pr"AT"juntendo.ac.jp
順天堂大学のHP
※E-mailは上記アドレス"AT"の部分を@に変えてください。
関連リンク
掲載日 平成30年1月4日
最終更新日 平成30年1月4日


