脳情報動態の多色HiFi記録を実現する超高感度カルシウムセンサーの開発に成功
プレスリリース
東京大学
山梨大学
日本医療研究開発機構(AMED)
発表者
井上 昌俊
(研究当時 東京大学大学院医学系研究科 脳神経医学専攻 神経生化学分野特任助教/現在 スタンフォード大学医学研究科 バイオエンジニアリング部門研究員)
竹内 敦也(研究当時 東京大学大学院医学系研究科 機能生物学専攻 神経生理学分野 大学院生)
真仁田 聡(山梨大学大学院総合研究部医学域 神経生理学教室 助教)
喜多村 和郎(山梨大学大学院総合研究部医学域 神経生理学教室 教授)
尾藤 晴彦
(東京大学大学院医学系研究科 脳神経医学専攻 神経生化学分野 教授/東京大学国際高等研究所ニューロインテリジェンス国際研究機構(WPI-IRCN)連携研究者)
発表のポイント
- 神経活動・シナプス活動ダイナミクスを、生きたマウス脳で多色HiFi記録することを実現しました。
- 最高性能の超高速カルシウムセンサーの開発に成功し、協調して神経発火を繰り返す多細胞 種の同時計測技術を樹立し、5感・行動・記憶などの過程を制御する神経細胞活動の測定技術を飛躍的に進展させました。
- 異なる細胞種間の動的相互関係を計測する脳情報動態学を切り拓き、複数細胞種の神経ダイナミクス破綻に起因すると考えられている自閉症等の精神疾患や、てんかんなど神経疾患の病態解明も期待されます。
発表概要
カルシウム(Ca2+)が神経発火に伴い細胞内に流入することを生かして、蛍光Ca2+センサーを用いて脳情報を解き明かす試みが近年急速に広まっています。しかしながら、従来のCa2+センサーは、1)遅い反応動態のため発火パターン(注1)の読み取りが不十分であることと、2)蛍光の色が少なく、用途が制限されていました。特に、脳は複数の異なる神経細胞種の協調的な発火パターンにより正常機能を発揮すると考えられていますが、これを解明するための高性能多色Ca2+センサーの開発が望まれていました。
この度、東京大学大学院医学系研究科の井上昌俊 特任助教(研究当時)、竹内敦也 大学院生(研究当時)、尾藤晴彦 教授らの研究グループは、山梨大学総合研究部医学域の真仁田聡 助教、喜多村和郎 教授らと共同で生きた哺乳類脳の神経発火活動・シナプス活動を計測するための超高感度・超高速Ca2+センサーの青、緑、黄及び赤色の『XCaMP』シリーズを開発しました。その結果、マウス生体内において高頻度発火神経細胞の発火パターンの読み取り及び3種の異なる細胞種の多重計測に成功しました。この成果は、今後生きた哺乳類脳における神経活動およびそのダイナミクスの多重計測を容易にし、精神疾患や学習・記憶障害などの病態解明および治療法の開発につながるものと期待されます。本研究は日本医療研究開発機構(AMED)の「革新的技術による脳機能ネットワークの全容解明プロジェクト(革新脳)」の研究開発課題「革新的プロ-ビングによる神経活動の高速3D測定と活動痕跡の長期可視化」、ならびに文部科学省新学術領域研究「脳情報動態」の支援によって実施されました
発表内容
(1)研究の背景・先行研究における問題点
脳は複数の異なる神経細胞種が協調的な発火をすることにより正常機能を発揮すると考えられています。特に、脳情報は回路網における特定の細胞種の神経発火パターン(周波数、タイミング、数及び異なる細胞同士の同期的な発火)にコードされていると考えられています。近年、この脳情報を読み解くのに、神経発火に伴い細胞内にCa2+が流入することを利用し、蛍光カルシウム(Ca2+)センサーを用いた神経活動イメージング法が急速に普及しつつあります。特定の神経細胞種に発現させることができ、長期観察可能であるため、遺伝子にコードされたCa2+センサー(以下GECIと略)が広く用いられています。しかしながら、従来の生体内で実用的なGECIは、緑色域、あるいは本研究グループが2015年に開発した赤色域(R-CaMP2; Inoue et al., 2015, Nat. Methods)のGECIのみであるため、3種類以上の神経細胞種の協調的発火を同時計測するには不十分でした。加えて、従来のGECIは入力の有無もしくは強度のみを検出しており、どのような入力(発火頻度、回数)であるかを読み取るには不十分でした。この問題点を解決するために①青、緑、黄、赤色の4色、②キネティクスが早く、③発火回数と蛍光変化に線形の関係があり、④広範囲のCa2+濃度を線形的に高感度検出するGECIを開発することが望まれていました(図1)。
②-④の条件を実現するためにCa2+濃度と蛍光強度の変化の関係であるHill係数(注2)が『1』付近のGECIを作出することが必要でした。しかしながら、従来のGECI はHill 係数が2~3付近であることから、複数の発火に対し非線形的に蛍光強度が変化し、かつ、広範囲のCa2+濃度を検出するのが困難でした。そこで、本研究グループはこれらの問題を解決するために、超高速、高感度、Hill係数1かつダイナミックレンジが大きい多色GECI を作成することを目的としました。
(2)研究内容
本研究グループは従来GECIのHill係数の値が2~3で高い非線形性を示し、線形性の指標である1を大幅に上回るのは、CaM結合領域として筋肉由来タンパク質のCa2+結合配列が用いられていたためではないか、と仮説を立てました。そこで、抜本的置換を試み、神経細胞由来タンパク質CaMKKのCaM結合配列を参考にした新規配列を設計し挿入しました。加えて、複数個所に変異を導入しました。これらの結果、Ca2+応答が最速のXCaMP-Gf、及び単一の活動電位(注3)に伴うCa2+応答が最大のダイナミックレンジを持つXCaMP-Gを開発しました。さらにこれを基に、多色化変異を試み、青色のXCaMP-B、黄色のXCaMP-Y及び赤色のXCaMP-Rを創出しました。こうして、Hill係数がおよそ1付近の値をとり、生体内Ca2+計測に威力を発揮する線形GECIシリーズ、XCaMPを世界に先駆けて作成しました。
初めに、Hill係数を1にした効果を検証するために、マウス生体内大脳皮質興奮性錐体細胞(注4)において2光子イメージング法(注5)と電気生理法(注6)を同時に行いました。その結果、全てのXCaMPセンサーが神経発火回数と蛍光強度の変化の間に強い線形の関係を有することを見出し、単一の活動電位を鋭敏に検出することを示しました。次に、世界最速のXCaMP-Gfoを用いることにより、マウス生体内において高頻度発火するパルアルブミン(PV)陽性細胞(注7)の発火パターンを従来のGECIよりも最も精度良く読み取れることを示しました。また、生体内で計測可能な初めての青色GECIのXCaMP-Bを作成したことにより、自由行動下においてXCaMP-GfとXCaMP-Rを組み合わせて、ファイバーフォトメトリー法(注8)を用いてマウス前頭前野(注9)における異なる3種類の神経細胞種(興奮性錐体細胞、抑制性(注10)のPV陽性細胞及びソマトスタチン(SST)陽性細胞(注11))の活動同時計測に初めて成功しました。その結果、抑制性PV陽性細胞がSST陽性細胞に先行して活動し、その相前後に興奮性錐体細胞が活動するという各細胞種が時間的に精緻に制御されていることを初めて示しました。さらに、従来測定可能な色域が限られていたため、樹状突起または軸索の一方のみしか活動計測できなかったため、両者の関係については測定困難でした。XCaMP-YとXCaMP-Rを用いて生体内において初めて興奮性細胞の樹状突起と抑制性細胞の軸索の同時計測に成功し、時空間的な軸索・樹状突起の制御を明らかにしました。最後に、XCaMP-Rが赤色と長波長シフトしているため、光の組織内散乱が少ないことを利用し、可視化対象上部の大脳皮質を一切除去せず、非侵襲的に海馬CA1領域の錐体細胞神経活動の直接計測を実現しました。以上のように、XCaMPを用いることにより、従来計測困難であった神経回路の複雑なダイナミクスが織りなす脳情報動態を明らかにする新規の方法論を提示したと言えます。
(3)社会的意義・今後の予定 など
本研究成果は、生きた動物で多種類の神経細胞種を同時かつ発火パターンを読み取ることが飛躍的に向上したことを示す初めての報告です。今後複数細胞種の神経ダイナミクスの破綻により発症すると考えられる自閉症や統合失調症等の精神疾患の神経基盤を明らかにすることが期待されます。本研究は特に脳神経機能に着目したXCaMP利用法を実証しました。Ca2+は全ての細胞機能に重要であることから、神経・精神疾患以外にもCa2+動態の異常が関連する循環器疾患、アレルギーなどの原因解明や創薬スクリーニングの精度向上につながることが期待されます。
発表雑誌
- 雑誌名:
- 「Cell」2019年5月9日オンライン版(米国東部夏時間)
- 論文タイトル:
- Rational engineering of XCaMPs, a multicolor GECI suite for in vivo imaging of complex brain circuit dynamics
- 著者:
- Masatoshi Inoue*, Atsuya Takeuchi*, Satoshi Manita*, Shin-ichiro Horigane, Masayuki Sakamoto, Ryosuke Kawakami, Kazushi Yamaguchi, Kouhei Otomo, Hiroyuki Yokoyama, Ryang Kim, Tatsushi Yokoyama, Sayaka Takemoto-Kimura, Manabu Abe, Michiko Okamura, Yayoi Kondo, Sean Quirin, Charu Ramakrishnan, Takeshi Imamura, Kenji Sakimura, Tomomi Nemoto, Masanobu Kano, Hajime Fujii, Karl Deisseroth, Kazuo Kitamura, and Haruhiko Bito** (*共同筆頭著者, **責任著者)
- DOI番号:
- doi: 10.1016/j.cell.2019.04.007
- ビデオアブストラクト:
- https://youtu.be/BoyGNBqM9mg
用語解説
- (注1)発火パターン
- 神経細胞の膜電位が活動電位に達することを発火といい、発火することにより上流の神経細胞から下流の神経細胞へ情報を伝達する。高頻度神経発火時と低頻度発火時では下流への情報の伝達量が変化すると考えられている。高頻度神経発火時に記憶が成立するなど特定の情報が伝達されるのに重要な役割を担うと考えられている。
- (注2)Hill係数
- 本研究の場合、Ca2+と蛍光強度変化の協同性を示す指標として用いられる。Hill係数が1より大きいほど協同性が高く、Ca2+に対する蛍光強度は正の協同性が現れ、非線形的な変化を示す。
- (注3)活動電位
- 神経細胞がほかの神経細胞に情報を伝える際に、0.5-1ミリ秒の間だけ神経細胞の膜電位がマイナスからプラスに変化すること。
- (注4)興奮経錐体細胞
- 興奮性神経伝達物質であるグルタミン酸を放出し、ほかの神経細胞の活動を興奮させる神経細胞。
- (注5)2光子イメージング法
- 従来のイメージング技術では生きた動物の内部で起きている現象を困難であった生体深部にある蛍光分子を観察する事ができ、空間解像度にも優れた顕微鏡法。
- (注6)電気生理法
- 神経、脳、筋肉、心臓などの組織または細胞の電気的性質と生理機能との関係を解明する学問。特に神経生理学では電気生理学的手法を用いて、脳機能を解明しようと50年以上前から用いられている手法である。
- (注7)パルアルブミン陽性細胞
- パルブアルブミンは特定の抑制神経細胞を標識するのに用いられる。抑制性神経細胞には、形態や投射相手、発現分子の異なるサブタイプが存在する。パルブアルブミン陽性細胞は高頻度発火を特徴とする大脳皮質の25%程度を構成する一部の抑制性神経細胞である。
- (注8)ファイバーフォトメトリー法
- 生体内で特定の脳領域の蛍光測定を行うためのシステムです。脳内にファイバーケーブルを挿入することにより、自由行動下でのミリ秒単位の高速神経活動計測を可能とすることを特徴とする。
- (注9)前頭前野
- 脳領域は複雑な認知行動の計画、適切な社会的行動の調節に関わっているとされている。この脳領域の基本的な活動は、自身の内的ゴールに従って、考えや行動を編成することにあると考えられる。
- (注10)抑制性神経細胞
- 抑制性神経伝達物質であるGABAを放出し、ほかの神経細胞の活動を抑制する神経細胞。
- (注11)ソマトスタチン陽性細胞
- ソマトスタチンは特定の抑制神経細胞を標識するのに用いられる。ソマトスタチン陽性細胞は大脳皮質の20%程度を構成する一部の抑制性神経細胞である。
添付資料
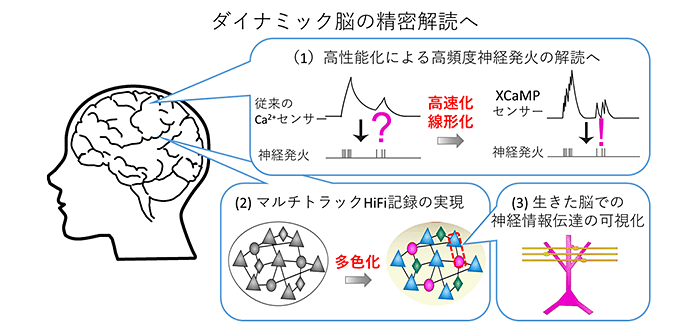
図1:XCaMPセンサー開発による本研究の意義
これにより、行動、記憶の過程における神経回路ネットワークの動作原理をはじめとして精神疾患などの病態を解明することが期待される。また、Ca2+動態の異常が関連する疾患の原因解明や創薬スクリーニングにつながることが期待される。
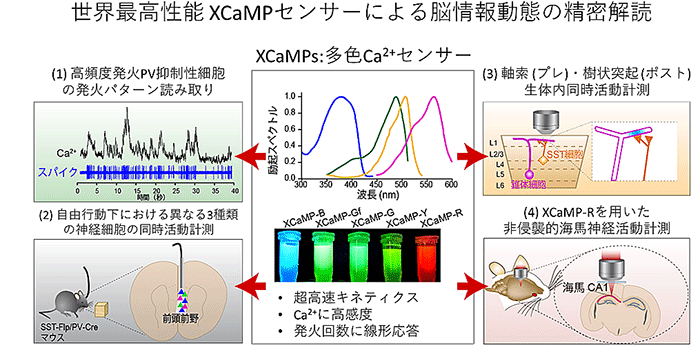
図2:XCaMPセンサー開発により得られた本研究の知見
お問い合わせ
本研究に関するお問い合わせ
国立大学法人 東京大学大学院医学系研究科 脳神経医学専攻 神経生化学分野
教授 尾藤 晴彦(びとう はるひこ)
Tel:03-5841-3559 Fax:03-3814-8154
E-mail:hbito"AT"m.u-tokyo.ac.jp
報道に関するお問い合わせ
国立大学法人 東京大学大学院医学系研究科 総務係
Tel:03-5841-3304 Fax:03-5841-8585
Email:ishomu"AT"m.u-tokyo.ac.jp
国立大学法人 山梨大学 総務部・総務課・広報企画室
Tel:055-220-8005 Fax:055-220-8799
Email:koho"AT"yamanashi.ac.jp
AMED事業について
国立研究開発法人 日本医療研究開発機構(AMED)
戦略推進部 脳と心の研究課
E-mail:brain-pm"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和元年5月10日
最終更新日 令和元年5月10日


