キネシン分子モーターKIF3Bの遺伝子異常は統合失調症の原因となる
プレスリリース
国立大学法人 東京大学
国立研究開発法人 日本医療研究開発機構(AMED)
国立大学法人 筑波大学
発表者
アルサバン ハッサン アシュワック(研究当時:東京大学大学院医学系研究科 分子細胞生物学専攻 特任研究員、現:Department of Biological Science, Faculty of Sciences, King Abdulaziz University, Jeddah, Saudi Arabia)
森川 桃(東京大学大学院医学系研究科 分子細胞生物学専攻 特任研究員)
田中 庸介(東京大学大学院医学系研究科 分子細胞生物学専攻 細胞構築学分野 講師)
武井 陽介(研究当時:東京大学大学院医学系研究科 細胞生物・解剖学教室 准教 授、現:筑波大学 医学医療系 解剖学・神経科学 教授)
廣川 信隆(東京大学大学院医学系研究科 分子細胞生物学専攻 分子構造・動態・病態学分野 特任教授)
発表のポイント
- ヒトの統合失調症患者の遺伝子の検索により、細胞内で物質を輸送するキネシン分子モーターKIF3Bに機能的欠損をもたらす遺伝子変異が同定された。
- Kif3b遺伝子が欠損したマウスには、社会性の低下や驚愕反応の異常など統合失調症の表現型が現れ、Kif3b遺伝子が欠損したマウスの海馬神経細胞には、シナプス形態とその機能に大きな異常が見られた。
- この理由として、シナプス伝達に重要な役割を果たすNMDA型グルタミン酸受容体(NMDAR)のNR2AサブユニットがKIF3Bによって輸送されることを発見した。
発表概要
統合失調症は日本人の100人に1人が罹る精神疾患であるが、その生物学的な病態にはまだ不明な点が多く、それに基づいた治療薬もまだ開発の途上にある。今回、東京大学大学院医学系研究科分子細胞生物学専攻の廣川信隆特任教授、アルサバンアシュワック特任研究員(研究当時)、森川桃特任研究員、田中庸介講師、武井陽介准教授(研究当時、現・筑波大教授)らの研究チームは、キネシン分子モーターKIF3B[注1]の異常が統合失調症の分子的基盤になることを発見した。チームはまず患者さんの遺伝子データから、KIF3Bの遺伝子異常を同定した。次に、KIF3Bの発現が半分に減っているKif3bヘテロ欠損遺伝子操作マウスを作って解析してみると、記憶・学習能力の低下や聴覚驚愕応答のプレパルスによる減弱の低下という統合失調症[注2]に特有の表現型が観察された。さらに、このマウスの神経細胞ではNMDA型グルタミン酸受容体の樹状突起スパイン表面における発現量が減少し、記憶・学習の基盤となるシナプス可塑性[注3]の変化が観察された。そこで、患者さんの変異を導入したKIF3Bタンパク質と野生型のKIF3Bタンパク質をそれぞれKif3bヘテロ欠損神経細胞に導入して活性を調べたところ、確かに患者さんではKIF3Bタンパク質の機能が低下していることがわかった。本研究から、統合失調症に対する新規治療法開発の基盤となる、細胞レベルでの新しい病態が解明された。
発表内容
キネシンスーパーファミリータンパク質(KIFs)は細胞内の物質輸送を担う分子モーターであり、機能分子の局在や活性を制御することで脳の高次機能や個体の発生の基盤となる、細胞の生命や機能を維持する重要なタンパク質群である。KIF3モーターはKIF3A・KIF3B・KAP3の三つのタンパク質からなるユニークな複合体モーターであり、東京大学大学院医学系研究科分子細胞生物学専攻の廣川信隆特任教授のこれまでの研究から、胎児の内臓の左右軸の決定に重要な役割を担っていることが知られていたが、神経・精神疾患との関連はほとんど知られていなかった。今回、廣川特任教授、アルサバン特任研究員(研究当時)、森川特任研究員、田中講師、武井准教授(研究当時)らの研究チームはAMED脳科学研究戦略推進プログラム(融合脳)の支援を受け、ヒトの統合失調症の新たな原因としてKIF3Bタンパク質を変異する遺伝子異常を特定した。
まずチームは、統合失調症患者ゲノムからKIF3Bの654番目のアミノ酸であるアルギニンが終止コドンに変異しているミスセンス変異(p.R654Ter)を同定した。そこでKIF3Bタンパク質の精神疾患への影響を確かめるため、Kif3b遺伝子がヘテロ欠損した遺伝子操作マウスの行動解析を行った。すると、オープン・フィールド試験と高架式十字迷路でKif3b遺伝子ヘテロ欠損マウスは過活動の傾向を示し、スリー・チェンバー社会性実験では他個体への興味の低下を示した。また、バーンズ迷路試験では記憶・学習能力の低下と、記憶の書き換えの柔軟性の低下が見られた。聴覚驚愕応答のプレパルスによる減弱は有意に低下していた。これら全ての行動解析の結果から、Kif3b遺伝子ヘテロ欠損マウスは統合失調症様の表現型を持つことが分かった。
一方、このKIF3複合体の神経細胞における機能に注目して免疫沈降法により結合タンパク質を検索したところ、スパイン表面に局在して可塑性に重要な役割を担うNMDARのサブユニットNR2AとKIF3Bが結合し、樹状突起内を輸送することを発見した。NR2Aの輸送を担う分子モーターの同定は世界で初めての報告である。
さらに、上記の免疫沈降法ではNR2Aの他にAPCやPSD95がKIF3複合体と結合する小胞に含まれていることが予想されたため、Kif3b遺伝子ヘテロ欠損マウスの胎児から海馬初代培養を樹立しセミ超高解像レーザー顕微鏡を用いて免疫細胞化学的な観察を行ったところ、KIF3Bの減少により、スパイン表面におけるNMDARとPSD95の局在量、スパイン内のAPCの量が有意に減少していることが分かり、KIF3複合体がこれらを輸送していることが示唆された。
また海馬初代培養におけるスパインをセミ超高解像レーザー顕微鏡にて観察したところ、KIF3Bの減少によりスパインの数が減少することも分かった。蛍光タンパク質を結合させたNR2Aを海馬初代培養細胞に導入しライブイメージングを行ったところ、Kif3b遺伝子ヘテロ欠損細胞ではNR2Aの輸送が特異的に障害されており、KIF3BがNR2Aの輸送分子モーターとして機能していることが確認された(図)。
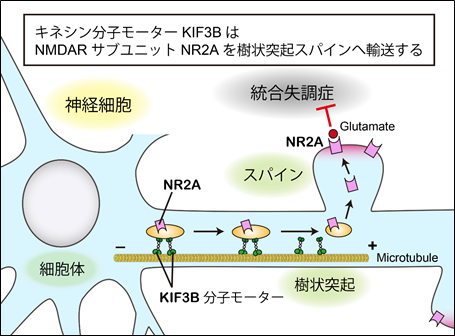
NMDARはシナプス可塑性に重要な役割を担っていることが知られているため、研究チームはKIF3Bの減少が神経回路網にどのような影響をもたらすのかを調べるため、海馬の急性スライスを作成して電気生理学的に解析した。まず海馬の単一神経細胞にてパッチクランプ法を用いてAMPA型グルタミン酸受容体(AMPAR)応答とNMDAR応答の比率を計測することにより、KIF3Bの減少によってNMDARの応答が減弱していることが分かった。これはスパイン表面に発現するNMDARの量がKIF3Bの輸送能低下により減少したためだと推測される。さらに海馬急性スライスで可塑性を誘導する刺激を与えたところ、Kif3b遺伝子ヘテロ欠損海馬では野生型に比べてシナプス長期増強(LTP)が亢進し、シナプス長期抑圧(LTD)が減弱していることが分かった。これらの電気生理学的特徴は、統合失調症の表現型としてこれまでに報告されたものとよく一致し、またNMDARの機能異常は統合失調症に関与していることが提唱されている。
そこでヒトの統合失調症患者のR654Ter遺伝子変異が本当にKIF3Bタンパク質の機能低下をもたらしているかを、Kif3b遺伝子ヘテロマウスから初代培養した神経細胞に、全長のKIF3Bタンパク質を遺伝子工学的に強制発現する手法で調べた。まず、野生型のKIF3Bタンパク質を導入すると、スパイン表面のNR2A量を回復することができ、スパインの数も増加した。ところが、患者さんから同定されたヒト変異を導入したKIF3Bでは、どちらも回復することができなかった。したがってこの変異はまさしくKIF3Bの機能的欠損をもたらしていることが示唆された。
統合失調症は100人に1人が発症すると言われているが、発症メカニズムの全容が解明されていないため、その根本的な治療法はまだ確立していない。廣川特任教授らによる本研究成果は、KIF3複合体がNR2A/APC複合体を輸送することで神経細胞シナプスの形態や可塑性を維持し、その機能的欠損が統合失調症をもたらすという新規の分子メカニズムを提唱するものであり、NMDARが関与する統合失調症患者の治療法開発の基盤となる。
発表雑誌
- 雑誌名:
- The EMBO Journal
- 論文タイトル:
- Kinesin Kif3b mutation reduces NMDAR subunit NR2A trafficking and causes schizophrenia-like phenotypes in mice
- 著者:
- Ashwaq Hassan Alsabban†, Momo Morikawa†, Yosuke Tanaka, Yosuke Takei, and Nobutaka Hirokawa*(†共同第一著者、*責任著者)
- DOI番号:
- 10.15252/embj.2018101090
- アブストラクトURL:
- https://www.embopress.org/doi/10.15252/embj.2018101090
用語解説
- [注1]キネシン分子モーターKIF3B:
- 神経系に多く発現するキネシンスーパーファミリータンパク質の一種。45種類あるキネシン分子モーターは微小管というレールに沿って積み荷を運び、精神疾患をはじめ糖尿病・発がん・胎児の発生などにさまざまな重要な役割を果たしている。
- [注2]統合失調症:
- 統合失調症は、思考や行動、感情などを1つの目的に沿ってまとめていく能力、つまり「統合」する脳の機能が破綻することで幻覚や妄想による異常行動の発現を主症状とし、意欲・自発性の低下などの機能低下、認知機能低下なども引き起こす精神疾患である。現代では100人に1人が統合失調症を発症すると言われているが、その発症分子メカニズムが完全には解明されていないため、根本的な治療法はまだ確立していない。そのため抗精神病薬による薬物対症療法と、心理社会療法により症状の緩和を図っているのが現状である。しかし、一旦統合失調症を発症すると慢性的な経過をとり、患者のクオリティーオブライフは著しく低下するため、根本的な治療法の開発が待たれている。
- [注3]シナプス可塑性:
- 神経活動に依存して、シナプスにおける神経細胞間のシナプス伝達物質の伝達効率が長期にわたって増加(長期増強、LTP)または低下(長期抑圧、LTD)する現象のこと。記憶や学習、精神活動といった脳の高次脳機能の細胞レベルでの基盤となる。NMDARを介するものと、代謝型グルタミン酸受容体(mGluR)を介するものが存在するが、どちらもAMPARが神経活動依存的にスパイン表面から細胞内へ取り込まれ、スパイン表面におけるその数が増加(LTP)または減少(LTD)するとともに、樹状突起のスパインの形態がダイナミックに変化することがその分子的な実体であるが、その制御メカニズムにはまだ不明な点も多い。
お問い合わせ先
東京大学大学院医学系研究科 分子細胞生物学専攻 分子構造・動態・病態学分野
特任教授 廣川 信隆(ひろかわ のぶたか)
Tel:03-5841-3326
E-mail:hirokawa"AT"m.u-tokyo.ac.jp
事業に関する問合せ先
国立研究開発法人 日本医療研究開発機構
〒100-0004 東京都千代田区大手町1-7-1 読売新聞ビル
戦略推進部 脳と心の研究課
E-mail:brain"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和元年11月20日
最終更新日 令和元年11月20日


