体に優しいオメガ3脂肪酸を動かし肥満を抑える新しい脂質代謝酵素の発見
プレスリリース
東京大学
日本医療研究開発機構
東京大学大学院医学系研究科 村上 誠 教授らは、脂質を代謝する酵素の生理的役割に関する研究から、白色脂肪組織に常在するM2マクロファージ*1から分泌される脂質分解酵素がオメガ3(ω3)脂肪酸*2を作り出し、脂肪の燃焼を促進して肥満の進行を遅らせることを発見しました。この成果は、肥満や糖尿病などの生活習慣病の新規予防・治療法の開発につながると期待されます。
この研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出」研究開発領域(研究開発総括:清水 孝雄)における研究開発課題「PLA2メタボロームによる疾患脂質代謝マップの創成とその医療展開に向けての基盤構築」(研究開発代表者:村上誠)、革新的先端研究開発支援事業ステップタイプ(FORCE)、ならびに日本学術振興会科研費(新学術領域研究、基盤研究)の一環として行われました。この研究は、2020年5月5日(米国東部時間午前11時)に米国科学誌『Cell Reports(セル・リポーツ)』にオンライン掲載されます。
研究の背景
生活習慣の欧米化に伴い、肥満や2型糖尿病などの生活習慣病の増加が社会問題となっています。脂肪組織には、脂肪を蓄える白色脂肪細胞*3と、脂肪を燃焼する褐色脂肪細胞*4が存在し、カロリーの貯蔵と消費のバランスを取っています。飽食による糖や脂肪の過剰摂取、運動不足によるエネルギー消費の低下が生活習慣病の背景にあることは疑いの余地がありませんが、最近では、白色脂肪組織の慢性炎症に加え、褐色脂肪細胞の機能低下による脂肪燃焼の減少が生活習慣病と関連することが注目されています。個体は寒冷にさらされると交感神経の刺激により褐色脂肪細胞が活性化するとともに、白色脂肪組織(特に皮下脂肪)にベージュ脂肪細胞*5が誘導され、脂肪を分解して熱へと変換します。この適応応答が損なわれると脂肪の燃焼が低下するため、脂肪の蓄積すなわち肥満へとつながります。魚油に豊富に含まれるエイコサペンタエン酸(EPA)やドコサヘキサエン酸(DHA)などのω3脂肪酸は、「体によい脂肪」として一般に広く認知されています。ω3脂肪酸は脂肪組織の慢性炎症を抑制するとともに、ω3脂肪酸受容体であるGPR120*6を介して白色脂肪細胞のベージュ化を促進することで、肥満症を抑える効果があると言われています。また、栄養素として摂取された外因性のω3脂肪酸は細胞膜を構成するリン脂質に取り込まれ、必要時にリン脂質分解酵素ホスホリパーゼA2 (PLA2)*7 の作用によりリン脂質から遊離されます。しかしながら、脂肪組織においてリン脂質からω3脂肪酸が内因的に動員されるメカニズムとその生理的意義は不明なままでした。
研究の概要
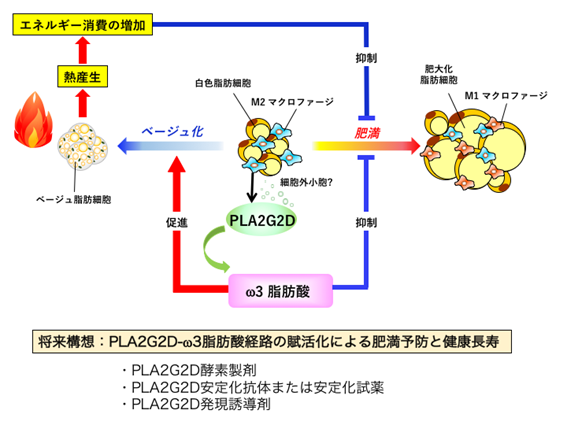
今回、本研究グループは、肥満の調節に関わる新たな脂質代謝関連分子を探索する目的で、マウスの白色脂肪組織の遺伝子発現プロファイリング解析を行った結果、肥満に伴い発現が著しく減少する遺伝子として、分泌性PLA2(sPLA2)の一つであるPLA2G2Dを同定しました。PLA2G2Dは脂肪組織のM2マクロファージに構成的に発現しており、炎症の進行に伴い発現が低下しました。全身性及びマクロファージ特異的PLA2G2D欠損マウスでは、高脂肪食負荷による肥満(図1A)とインスリン抵抗性、さらに脂肪組織の慢性炎症が野生型マウスと比べて増悪していました。また、PLA2G2D欠損マウスは高脂肪食を与える前から酸素消費量(=エネルギー消費量を反映)が野生型マウスと比べて低く、さらに興味深いことに、寒冷曝露時、あるいはβ3アゴニスト*8投与時(交感神経刺激を模倣)において、白色脂肪細胞のベージュ化が著しく損なわれていました(図1B)。PLA2G2Dはリン脂質分解酵素であることから、PLA2G2D欠損マウスの白色脂肪組織において減少している遊離脂肪酸を脂質の網羅分析(リピドミクス*9)により探索した結果、PLA2G2Dはリン脂質からω3脂肪酸を選択的に遊離していることがわかりました。さらに、ω3脂肪酸に富む魚油含有食をPLA2G2D欠損マウスに与えると、白色脂肪細胞のベージュ化の低下及び肥満進行の表現型が消失しました。このことから、M2マクロファージから分泌されるPLA2G2Dは白色脂肪組織中にω3脂肪酸を供給し、脂肪細胞のベージュ化を促進することで、肥満の進行を遅らせる役割を持つものと考えられます(図2)。本研究は、ω3脂肪酸の肥満予防効果に新たな学術的理解を与えるとともに、脂肪組織の微小環境においてω3脂肪酸が内因的に動員されるメカニズムの一端を解明したものです。
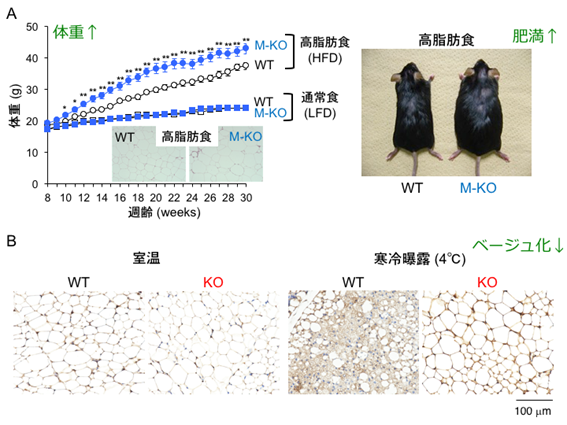
B.PLA2G2D欠損マウス(KO)とその対照マウス(WT)の皮下脂肪組織をUCP1に対する抗体で免疫染色した時の画像。室温ではWT、KOともに大きな単一脂肪滴で満たされた典型的な白色脂肪細胞が見られ、双方に差は認められない。寒冷曝露すると、WTではUCP1陽性(褐色に染色)で小型脂肪滴を豊富に含むベージュ脂肪細胞が出現する。一方、KOではWTと比べて脂肪細胞のベージュ化が抑制されていることがわかる。
今後の展望
PLA2G2D-ω3脂肪酸経路を賦活化する戦略は、肥満や糖尿病などの生活習慣病の新規予防・治療法の開発につながることが期待されます。PLA2G2Dそのものを薬として投与する、PLA2G2Dを抗体あるいは薬剤で安定化させる、PLA2G2Dの発現を増強させるなどの方策が将来の創薬構想として考えられます(図2)。
用語の解説
- *1 M2マクロファージ
- マクロファージは性質の違いにより様々な亜群に分類されるが、肥満研究の領域では、炎症促進性のM1マクロファージと炎症抑制性のM2マクロファージに分類されることが多い。M2マクロファージはIL-4やIL-13などのTh2サイトカインの刺激により分化し、肥満に伴う慢性炎症を抑える役割を担うほか、組織修復、血管新生、腫瘍増殖などに関わるといわれている。M2マクロファージは脂肪細胞のベージュ化を促進する因子を放出することが報告されていたが、一方で異論もあった。本研究はM2マクロファージ由来のPLA2G2Dが脂肪細胞のベージュ化促進因子として働くことを示している。
- *2 ω3脂肪酸
- 二重結合を複数含む多価不飽和脂肪酸の分類の一つであり、ω末端(脂肪酸のメチル基末端)から3番目の炭素に二重結合を持つ。代表例としてエイコサペンタエン酸(EPA)、ドコサヘキサエン酸(DHA)があり、これらは魚油に多く含まれる。抗炎症作用、抗動脈硬化作用を持つことがわかっており、「体によい脂肪酸」として一般に広く認知されている。
- *3 白色脂肪細胞と*4 褐色脂肪細胞
- 脂肪細胞は大きく2種類のタイプに分けられ、脂肪を貯蔵する白色脂肪細胞と脂肪を燃焼する褐色脂肪細胞に分類される。白色脂肪細胞は単一の巨大脂肪滴を持ち、局在部位に応じて内臓脂肪と皮下脂肪に分けられる。内臓脂肪の蓄積は生活習慣病の要因となる。褐色脂肪細胞は肩甲骨近傍の褐色脂肪組織に分布し、細胞質に小型の脂肪滴を豊富に含み、ミトコンドリアに富む。褐色脂肪細胞は脂肪を活発に分解し、ミトコンドリア内膜に存在する脱共役タンパク質UCP1を使って熱を産生する。
- *5 ベージュ脂肪細胞
- 寒冷曝露などの交感神経刺激に応じて白色脂肪細胞から変換され、熱を産生する特殊な脂肪細胞として、寒冷環境での体温維持に寄与している。白色脂肪組織(特に皮下脂肪)にベージュ脂肪細胞が誘導されるプロセスを脂肪細胞のベージュ化と呼ぶ。交感神経から分泌されるノルエピネフリン(ノルアドレナリン)が白色脂肪細胞のβ3アドレナリン受容体に作用することでベージュ化が刺激される。褐色脂肪細胞と同様に、ベージュ脂肪細胞も活発に脂肪を分解してUCP1依存的に熱を産生し、エネルギーを消費することから、肥満・生活習慣病の治療標的として関心が高まっている。
- *6 GPR120
- Gタンパク質共役受容体の一つで、オメガ3脂肪酸を内因性のリガンドとする。
- *7 ホスホリパーゼA2 (PLA2)
- リン脂質のsn-2位の不飽和脂肪酸を加水分解して脂肪酸とリゾリン脂質を産生する酵素群の総称。哺乳動物では30種類以上の分子種が存在し、それぞれが特有の生命応答に関わることが明らかとなってきている。このうち細胞外に分泌されるPLA2はsPLA2(secreted PLA2)と呼ばれ、本研究ではsPLA2アイソザイムのひとつ(PLA2G2D)を取り扱っている。
- *8 β3アゴニスト
- 交感神経末端から分泌される神経伝達物質ノルエピネフリンは、アドレナリン受容体に作用してシグナルを伝達する。アドレナリン受容体には複数のサブタイプがあり、β3受容体はその一つである。寒冷刺激に伴い交感神経から放出されたノルエピネフリンは褐色細胞やベージュ脂肪細胞に発現しているβ3受容体を活性化して熱産生応答を高める。β3受容体を活性化する薬物をβ3アゴニストと呼ぶ。
- *9 リピドミクス
- ゲノミクス(遺伝子)、プロテオミクス(タンパク質)、グライコミクス(糖)に対応する、脂質を対象とした網羅的解析を指す。それぞれの脂質分子種の分子量が異なることを利用して、組織や細胞などの検体に存在する多種多様な脂質分子種を質量分析により一斉に同定、定量する。最近の質量分析の高感度化により、微量の脂質分子種を容易に定量検出することが可能となった。
論文情報
- タイトル:
- “Secreted phospholipase PLA2G2D contributes to metabolic health by mobilizing omega-3 polyunsaturated fatty acids in white adipose tissue”
- 著者:
- Hiroyasu Sato, Yoshitaka Taketomi, Yoshimi Miki, Remi Murase, Kei Yamamoto, Makoto Murakami
お問い合わせ先
東京大学医学部総務チーム(総務担当)
〒113-0033 東京都文京区本郷7-3-1
TEL:03-5841-3304
Email:hazama.rie"AT"mail.u-tokyo.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課
〒100-0004東京都千代田区大手町1−7−1 読売新聞ビル
TEL:03-6870-2224
Email:kenkyuk-ask"AT"amed.go.jp
※Emailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和2年5月6日
最終更新日 令和2年5月6日


