精子の成熟を調節する鍵分子を発見―不妊症の原因究明と治療に新たな視点―
プレスリリース
大阪大学
日本医療研究開発機構
研究成果のポイント
- 精子の成熟(※1)機構のスイッチをオンにするタンパク質NELL2を発見した。
- NELL2はルミクライン(※2)と呼ばれる組織間情報伝達で機能することを発見した。
- 男性不妊の診断・治療薬や避妊薬への応用、組織間情報伝達を担う新規のメカニズムとして様々な生命科学分野で研究の応用が期待される。
概要
大阪大学微生物病研究所の淨住大慈助教、伊川正人教授(東京大学医科学研究所・特任教授兼任)らの研究グループは、精巣タンパク質NELL2が精巣上体(※3)に働き、精子の成熟機構のスイッチをオンにするメカニズムを世界で初めて明らかにしました(図1)。
精巣で作られたばかりの精子は受精能力を有していません。これは精子を成熟させる機能が精巣には備わっていないためです。精巣で作られた精子は、精巣上体へ送られ、「成熟」することで受精能力を獲得します。これまで、精子形成機構は盛んに研究されてきましたが、精巣上体の成熟および、精巣上体における精子の成熟機構についてはほとんど研究が進んでいませんでした。
今回、伊川教授らの研究グループは、性成熟の過程で精巣の精細胞(※4)がNELL2タンパク質を分泌することで、幼少期には未熟な精巣上体を刺激して分化誘導し、精子の成熟機構をオンにしていることを明らかにしました。さらに、40年以上前に提唱された「ルミクライン」という管腔内因子を介した組織間情報伝達の存在とメカニズムを明らかにしました(図2)。
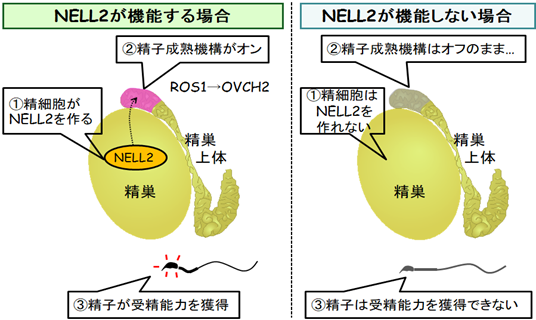
本研究成果は、 精巣因子NELL2による精巣上体の分化誘導、および精巣上体による精子成熟の制御機構を明らかにし、不妊症の病因解明に新たな視点を加えました。また本研究で存在を明らかにした組織間情報伝達システムである「ルミクライン」は、さまざまなライフステージで生命現象を制御する機構として働いている可能性があり、生命現象の基本的理解に貢献することが期待されます。
本研究成果は、米国科学誌「Science」に、2020年6月5日(金)16時(日本時間)に公開されます。
研究の背景
精子は精巣にある精細管(※5)の内側(管腔)で作られますが、精巣で作られたばかりの精子は受精能力を有していません(泳げないし、卵とも融合できない)。これは精子を成熟させる機能が精巣には備わっていないためです。それゆえ精巣で作られた精子は精細管の管腔を通って精巣上体へ送られ、そこで2週間という長い時間をかけて「成熟」することでようやく受精能力を獲得します。これまで、精子形成機構が盛んに研究される一方で、性成熟期に精巣上体が分化するしくみや、精巣上体が精子を成熟させるしくみについては研究がほとんど進んでいませんでした。研究グループは、精巣と精巣上体が管で繋がっていること、精巣から切り離された精巣上体が未分化な状態に戻ることなどから、40年以上前に提唱された、管腔を通る因子を介した組織間相互作用、「ルミクライン」システムに着目し、研究を開始しました。
研究の内容
研究グループは、遺伝子発現解析と、遺伝子改変マウスを組み合わせて研究を進めました。まず、性成熟期にかけてNELL2タンパク質が精巣の精細胞で作られること、管腔を通して運ばれたNELL2タンパク質に精巣上体のROS1タンパク質が応答して精巣上体が分化することを確認しました(図1)。次に、ゲノム編集(※6)より遺伝子を破壊したマウスを作ったところ、精巣のNELL2、精巣上体のROS1、いずれを無くした場合でも精巣上体が分化せず、精子が成熟できないため雄性不妊となりました(図2①②)。さらに同様の実験を重ね、分化した精巣上体がタンパク質分解酵素(OVCH2)を分泌することで、精子を成熟させることも見出しました(図2③)。
このように管腔の中を通る因子を介した組織間情報伝達は「ルミクライン」と呼ばれ、その存在が40年以上前から示唆されていましたが、肝心の情報伝達を担う因子が見つかっていませんでした。本研究によって、NELL2がルミクライン因子であることが世界で初めて明らかになりました。
本研究成果が社会に与える影響(本研究成果の意義)
約6組に1組のカップルが不妊に悩んでいます。そのうち、男性側に原因があると考えられるケースは約半数と言われていますが、特に精子の成熟に関わる因子はほとんどわかっていません。今後、NELL2による精子成熟の制御機構を明らかにしていくことで、加齢による生殖能力の低下との関連研究、不妊症の診断や治療薬、男性避妊薬の開発に繋がると期待されます。
また、これまで仮説であった「ルミクライン」という組織間情報伝達システムが解明されたことで、ライフステージを通してさまざまな生命現象を理解するための新たな視点が加わりました。
特記事項
本研究成果は、2020年6月5日(金)16時(日本時間)に米国科学誌「Science」(オンライン)に掲載されます。
- タイトル:
- “NELL2-mediated lumicrine signaling through OVCH2 is required for male fertility”
- 著者名:
- Daiji Kiyozumi, Taichi Noda, Ryo Yamaguchi, Tomohiro Tobita, Takafumi Matsumura, Kentaro Shimada, Mayo Kodani, Takashi Kohda, Yoshitaka Fujihara, Manabu Ozawa, Zhifeng Yu, Gabriella Miklossy, Kurt M. Bohren, Masato Horie, Masaru Okabe, Martin M. Matzuk, and Masahito Ikawa.
なお、本研究は、山梨大学・幸田尚教授、大塚製薬・堀江正人博士らとの国内共同研究であり、大阪大学の国際共同研究促進プログラムの支援を受けたベイラー医科大学のMartin M. Matzuk (マーティン M. マツック)教授らの研究グループとの国際共同研究により行われました。また日本学術振興会(科研費)、武田科学振興財団、アメリカ国立衛生研究所、ビル&メリンダ・ゲイツ財団、国立研究開発法人日本医療研究開発機構(AMED) 「老化メカニズムの解明・制御プロジェクト」の支援を受けて行った研究成果です。
用語説明
- ※1 精子の成熟:
- 精巣で作られた精子が受精するために必要な能力を獲得すること。
- ※2 ルミクライン(ルミクリン):
- 上皮細胞がつくる管の内側(管腔)を通る因子を介して組織間で情報を伝達するシステム。
- ※3 精巣上体:
- 精巣から連なった、高度にコイル化した一本の上皮組織の管が詰まった器官。幼少期は細い管が、加齢に伴い精子形成する時期になると肥厚する。この管の中を通過する間に精子は成熟し、輸精管を通って体外に出る。
- ※4 精細胞:
- 精子になる途中段階の細胞。
- ※5 精細管:
- 精巣の中にある細胞が作る管状の組織。精子は精細管の内側(管腔)で作られており、精巣と精巣上体は管腔でつながっている。
- ※6 ゲノム編集:
- ゲノム(遺伝子を含む遺伝情報)上の任意の場所で、欠失・挿入などの変異を導入できる遺伝子改変技術のひとつ。
お問い合わせ先
本件に関する問い合わせ先
大阪大学 微生物病研究所
教授 伊川正人(いかわまさひと)
TEL:06-6879-8375 FAX: 06-6879-8376
E-mail: ikawa"AT"biken.osaka-u.ac.jp
AMED事業(老化メカニズムの解明・制御プロジェクト)について
国立研究開発法人日本医療研究開発機構
疾患基礎研究事業部 疾患基礎研究課
TEL:03-6870-2225 FAX:03-6870-2243
E-mail:aging"AT"amed.go.jp
※e-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年6月5日
最終更新日 令和2年6月5日


