日本人におけるミトコンドリア肝症の臨床像・遺伝学的特徴を初めて解明
プレスリリース
千葉県こども病院
国立研究開発法人日本医療研究開発機構
概要
千葉県こども病院遺伝診療センター・代謝科の志村優医員、村山圭部長、国立成育医療研究センター臓器移植センター笠原群生センター長、埼玉医科大学大竹明教授、順天堂大学医学部岡﨑康司教授、津山中央病院小児科梶俊策主任部長、済生会横浜市東部病院小児肝臓消化器科乾あやの部長らの研究グループが、本邦における重症型のミトコンドリア肝症*1である脳肝型ミトコンドリアDNA枯渇症候群(MTDPS)*2と診断された23症例を対象に、その臨床的特徴、分子学的特性、長期経過、肝移植予後の検証を行い、その結果を論文報告しました。
本報告は、我が国だけでなくアジアにおいて初めて取りまとめられたミトコンドリア肝症の予後に関する大規模な報告であり、今後の創薬開発研究や、国内外の臨床試験に必要なエビデンスを提供するものと期待されます。本研究成果は、希少難病を扱う欧州の科学雑誌『Orphanet Journal of Rare Diseases』に掲載されます。
※本研究は、国立研究開発法人日本医療研究開発機構(AMED)「難治性疾患実用化研究事業」の研究費を用いて行われました。
研究成果のポイント
- ミトコンドリア肝症はミトコンドリア病*3全体の約1割を占めており、そのうち23例が重症型のミトコンドリア肝症(MTDPS)だった。
- 初発症状は約半数の症例が乳児期早期から成長障害を呈しており、乳児期の黄疸を21例(91%)で認めた。
- MTDPSにおける原因遺伝子が23例中18例(78%)で同定され、MPV17が13例、DGUOK3例、POLG1例、MICOS13が1例だった。
- 肝移植は12例に対して行われ、うち5例が2020年3月時点で生存していた。
- MPV17異常症において、肝移植前に重篤な神経筋症状を示さず、c.149G>Aまたはc.293C>Tを有する症例は比較的生命予後が良いことが明らかになった。
研究の背景
千葉県こども病院遺伝診療センター・代謝科/千葉県がんセンター研究所の研究グループ(代表村山圭)は、2007年から埼玉医科大学小児科(大竹明教授)、順天堂大学難病の診断と治療研究センター(岡崎康司教授・センター長)と共同で、ミトコンドリア病の診療基盤構築(診断システムの確立、診断基準や診療マニュアルの策定、レジストリ構築)を行ってきました。その中で、津山中央病院(小児科梶俊策医師)とも連携し、ミトコンドリア肝症の分子遺伝学的診断やレジストリ構築を進めてきました。
肝障害を主症状とするミトコンドリア病(ミトコンドリア肝症)は、これまでほとんど知られていませんでした。ミトコンドリア肝症は、ミトコンドリア病と生化学診断された小児の10~20%程度を占めます。なかでも重症型の脳肝型ミトコンドリアDNA枯渇症候群(MTPDS)はミトコンドリアDNA(mtDNA)*4の維持や複製に関わる蛋白の欠損により発症し、乳児期早期に肝不全を発症しうる、最重症の病型であることが知られています。
ミトコンドリア肝症に対する治療は、他のミトコンドリア病と同様に十分なエビデンスをもつ治療法が存在しないため、対症療法が中心となっています。しかしながら、本症では内科的治療でコントロールできない肝不全に対し、肝移植術が考慮されます。本邦での小児の肝移植後の5年生存率は85%以上ですが、海外の報告におけるミトコンドリア肝症に対する肝移植後生存率は、術後の肝外症状の悪化等により30%にとどまることが知られており、欧米のガイドラインでは肝移植の適応は、術前に肝外症状が存在しない症例にのみ考慮されています。そのため、ミトコンドリア病に対する肝移植治療の報告数は限られ、さらに症例毎に予後が大きく異なることが問題となっていました。
最近の動物モデルの研究により、MTDPSの原因遺伝子の一つであるMPV17はDNAやRNA等の核酸の複製に必要なデオキシヌクレオチド3リン酸(dNTP)の供給に関与していることが明らかになりました。MPV17異常症はミトコンドリア内のdNTPが不足することでmtDNAが枯渇することが知られており、海外においては核酸補充療法(dNTP補充療法)がMPV17異常症の新規治療候補として注目を集めています。
今回、本邦で初めてとなるミトコンドリア肝症の大規模な後方視的検討*5を行い、その研究結果を多施設共同研究の成果として発表するに至りました。
研究の内容
対象・方法
2020年6月現在1140例のミトコンドリア病を診断し、約1割にあたる107例がミトコンドリア肝症です(図1)。そのなかで、重症型ミトコンドリア肝症である脳肝型ミトコンドリアDNA枯渇症候群と診断された23例の臨床的特徴、遺伝学的特性、肝移植の実施状況、長期予後を調査しました。
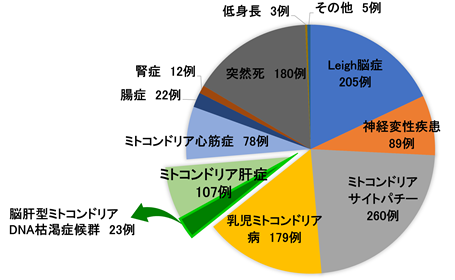
(Murayama K, et al. J Hum Genet 2019.を改変)
結果
重症型ミトコンドリア肝症23例の患者プロフィールを表1に示します。性別は男子11例、女子12例でした。初発症状として成長障害を13例、嘔吐8例、黄疸を4例で認めました。これらの初発症状は20例(87%)で乳児期早期から出現していました。ミトコンドリア呼吸鎖酵素活性(表1の障害酵素)は22例で解析し(No.8以外の症例)、複数の呼吸鎖酵素活性の低下が19症例において認められました。mtDNA定量検査では、mtDNAコピー数の低下は0.5~31.7%でした。遺伝子検査の結果、23症例中18例で病因となる遺伝子変異が同定されました(図2)。MPV17遺伝子が13例、DGUOK遺伝子が3例、POLG遺伝子1例、MICOS13遺伝子が1例で同定されました。
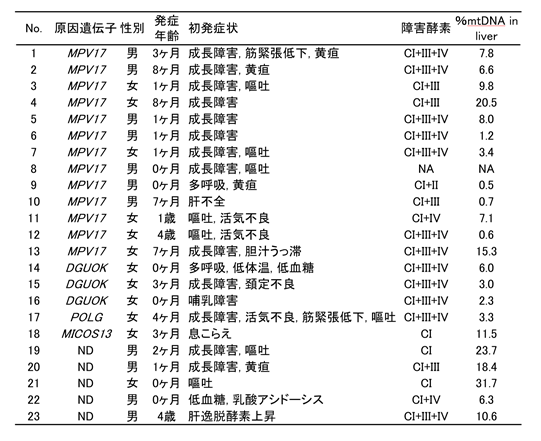
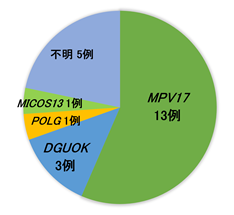
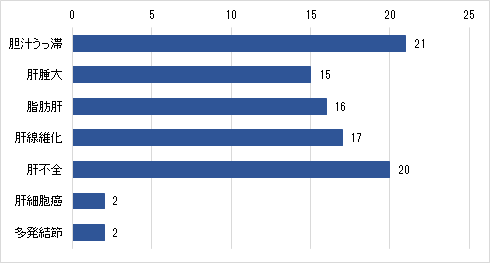
経過中に認められた肝症状を表2に示します。最も頻度の高い症状は胆汁うっ滞で21例で認め、肝腫大、脂肪肝、肝線維化はそれぞれ15、16、17例で認めました。また、経過中に肝不全を20例で認め、MPV17異常症の2症例が肝細胞癌を発症しました。
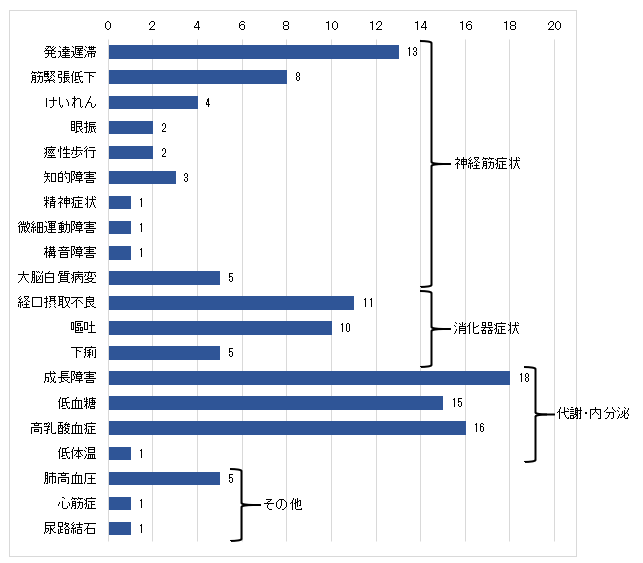
ミトコンドリア病はATPをミトコンドリアに依存するさまざまな臓器を障害するため、ミトコンドリア肝症においても肝症状だけでなく、神経筋症状や心臓合併症など、様々な肝外症状を示します。最も頻度の高い肝外症状として成長障害を18例で認め、続いて高乳酸血症を16例、低血糖を15例で認めました(表3)。神経筋症状のうち高頻度にみられたものは、発達遅滞13例、筋緊張低下8例、けいれんを4例で認めました。また頭部MRI検査で大脳白質病変を5例に認めました。神経筋症状を認めない症例は5例存在しました。消化器症状として経口摂取不良を11例、嘔吐10例、下痢を5例に認めました。また、肺高血圧症を5例に認めました(MPV17:4例、DGUOK:1例)。
遺伝子検査結果の詳細、肝移植の実施状況、予後を表4に示します。MPV17遺伝子に変異をもつ13例中8例において、c.451dupCが同定されました。c.451dupCをもつMPV17異常症は2016年に韓国からも報告がありますが、それ以外の国からの報告はないため、日本を含む東アジアの高頻度変異の可能性が考えられます。c.143-307_170del335はDGUOK異常症の3症例において同定されました。MICOS13異常症では、これまで報告のなかった新規変異c.13_29delが同定されました。
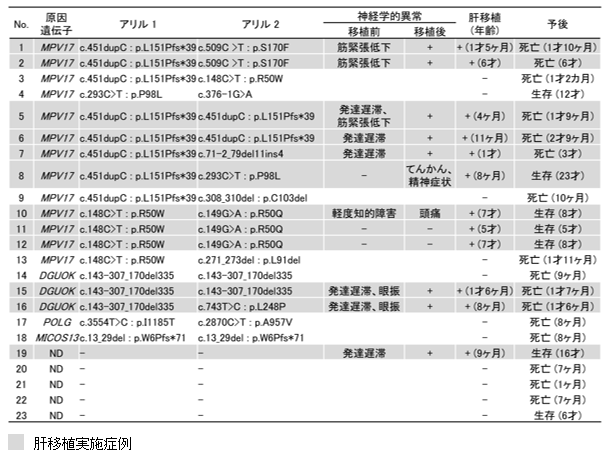
肝移植術は、MPV17異常症9例、DGUOK異常症2例を含む12症例において実施されました。肝移植の原因は、8例は肝不全、2例は肝細胞癌、2例は多発結節でした。肝移植後、MPV17異常症4症例を含む5症例(41.7%)が生存していました。また、肝移植を必要とせず生存している症例はMPV17異常症の1例を含む2例が生存していました。移植前に神経筋症状を合併していた9例中2例が2020年3月時点において術後生存していた一方で、移植前に神経筋症状を認めなかった3症例は全例生存しており、術前に神経筋症状を伴わない症例では、移植予後が良いことが明らかとなりました。しかしながら、術前に神経筋症状を認めなかった1症例においては、移植後5年経過してからてんかんや精神症状等の症状が出現していました。発症年齢別に移植予後を検討してみると、生後6カ月未満で発症した8症例のうち2症例が生存(25%)、一方生後6か月以降に発症した4症例中3症例が生存しており(75%)、発症年齢が遅い方が予後が良いことが分かりました。
最も頻度の多かったMPV17異常症の遺伝子変異毎の予後を検討すると、c.451dupCを少なくとも1本のアリルにもつ8症例においては、1例のみが生存していました。特にc.451dupCを2本もつ2症例は1歳未満で肝不全を発症し、肝移植を受けましたが、術後2年以内に死亡しました。同じ変異をもつ韓国の兄弟例も生後6か月で肝不全により死亡しており、c.451dupCを2本持つ症例は予後不良であることが示唆されました。一方で、c.149G>Aまたはc.293C>Tを少なくとも1本のアリルにもつ5症例(1症例は肝移植なし)は、全例が生存しており、これらの変異をもつ症例は比較的軽症な表現型を示すことが分かりました。
MPV17異常症に対する肝移植術は過去に論文報告された症例を検討すると、本邦の9症例を含めて計20症例に対して実施されていました。そのうち生存しているのは9症例(45%)であり、うち8症例がc.149G>Aまたはc.293C>Tを少なくとも1つ持っていました。また、肝移植後死亡した11症例中8例は移植前に神経筋症状を発症していた一方で、肝移植後生存している9症例中1例のみ移植前に神経筋症状を示していました。しかしながら、生存している9例中7例が肝移植後に何らかの神経筋症状を発症していました。以上より、MPV17異常症においては、術前に重篤な神経筋症状を示さず、c.149G>Aまたはc.293C>T変異をもつ症例は、比較的生命予後が良好であることが明らかになりました。
まとめ
これまでの報告通り、重症型のミトコンドリア肝症に対する肝移植の成績は他の疾患と比較し不良であり、特に術前に神経筋症状を有している症例では生命予後が不良でした。発症年齢が6か月以降の症例では、それ以前に発症する症例と比較し予後が良いことがわかりました。またMPV17異常症においては肝移植前に重篤な神経筋症状を示さず、c.149G>Aまたはc.293C>Tを有する症例は比較的予後が良いことが明らかになりました。
本研究成果は、重症型のミトコンドリア肝症の臨床像、分子遺伝学的特徴、また肝移植術の長期予後を明らかにしたことで、本症の早期診断、治療法の選択やその適応の検討に役立つだけでなく、治療薬の開発や国内外の臨床試験に必要な基礎的・臨床的エビデンスを提供するものとなります。
論文情報
- 論文タイトル
- Clinical and molecular basis of hepatocerebral mitochondrial DNA depletion syndrome in Japan: evaluation of outcomes after liver transplantation
日本における脳肝型ミトコンドリアDNA枯渇症候群の臨床像と分子学的基礎、及び肝移植後の評価 - 著者
- Masaru Shimura, Naomi Kuranobu, Minako Ogawa-Tominaga, Yohei Sugiyama, Tomohiro Ebihara, Takuya Fushimi, Keiko Ichimoto, Ayako Matsunaga, Tomoko Tsuruoka, Yoshihito Kishita, Shuichiro Umetsu, Ayano Inui, Tomoo Fujisawa, Ken Tanikawa, Reiko Ito, Akinari Fukuda, Jun Murakami, Shunsaku Kaji, Mureo Kasahara, Kazuo Shiraki, Akira Ohtake, Yasushi Okazaki, Kei Murayama
- 雑誌名
- Orphanet Journal of Rare Diseases
- DOI:
- 10.1186/s13023-020-01441-5
本研究に係わる学会発表
志村優、乾あやの、谷川健、白木和夫、梶俊策、笠原群生、村山圭、他。日本人におけるミトコンドリア肝症の臨床像・遺伝学的特徴の解明。第47回日本小児栄養消化器肝臓学会、2020年10月23-25日、東京。
用語解説
- *1 ミトコンドリア肝症
- 肝障害・肝不全を主症状とする酸化的リン酸化(OXPHOS)の障害であり、小児期発症のミトコンドリア病の10-20%を占めます。およそ40%は新生児期に発症し、急性または慢性的な肝不全を呈します。症状が肝臓のみにとどまる場合もありますが、多くは経過中にけいれん、脳症、退行などの神経筋症状が出現します。特殊なミトコンドリア肝症として、肝不全状態を持ちこたえると、自然に肝障害が改善するTRMU異常症(可逆性ミトコンドリア肝症)が知られています。
- *2 ミトコンドリアDNA枯渇症候群
- ミトコンドリアDNA(mtDNA)の複製や核酸供給機構の異常などの原因で、mtDNAの量が過度に減少(枯渇)し、ミトコンドリアのエネルギー代謝が阻害され機能障害の起こる疾患を総称して、ミトコンドリアDNA枯渇症候群と呼びます。症状から筋型、脳筋型、脳肝型に分類され、脳肝型の原因遺伝子として、DGUOK、MPV17、POLG、SUCLG1、TWNKが知られています。
- *3 ミトコンドリア病
- ミトコンドリア病とは、ミトコンドリアの働きが低下することが原因で起こる病気の総称で、エネルギー代謝系の先天代謝異常症です。出生 5,000人に1人の割合で発症し、いかなる症状、いかなる臓器・組織、何歳でも、いかなる遺伝形式でも発病します。特に幼少時期発症例は症状が多彩で重篤致死の症例が多いです。根治的治療法がなく、対症療法にとどまります。
- *4 ミトコンドリアDNA(mtDNA)
- ミトコンドリアDNAは16569塩基対を有し、13個の呼吸鎖のサブユニットを含む37個の遺伝子をコードします。各ミトコンドリアには2~10コピーのミトコンドリアDNAがあります。
- *5 後方視的検討
- ある特定の集団に対して、研究開始時点からさかのぼって診療録等のデータを用いて調査する方法を、後方視的検討といいます。
お問い合わせ先
本件に関するお問い合わせ先
千葉県こども病院
事務局医事経営課
Tel:043-292-2111
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構
ゲノム・データ基盤事業部 医療技術研究開発課
難治性疾患実用化研究事業担当
E-mail:nambyo-r”AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年7月24日
最終更新日 令和2年7月24日


