細胞の運命を司る転写因子GATA3のDNA結合メカニズムの解明―乳がんなどの疾患の原因解明への糸口に―
プレスリリース
東京大学定量生命科学研究所
日本医療研究開発機構
発表者
胡桃坂仁志(東京大学定量生命科学研究所 クロマチン構造機能研究分野 教授)
滝沢由政(東京大学定量生命科学研究所 クロマチン構造機能研究分野 准教授)
田中大貴(東京大学定量生命科学研究所 クロマチン構造機能研究分野 特任研究員)
高久誉大(米国ノースダコタ大学 Assistant Professor)
ポイント
- 遺伝子の読み取りを制御することで細胞の運命決定を司る転写因子が、染色体中で標的となるDNA配列を探索し結合するメカニズムは不明であった。
- 転写因子GATA3がヌクレオソームを認識して結合するメカニズムを明らかにした。
- GATA3の遺伝子変異は乳がんなどの疾患に関与していることから、これらの疾患の原因解明や治療法確立への応用が期待される。
概要
胡桃坂仁志教授ら東京大学定量生命科学研究所のグループは、遺伝子の読み取り(転写)のオン・オフを制御する転写因子GATA3が染色体中で標的DNA配列を認識して結合するメカニズムを明らかにしました。
転写因子は特定のDNA配列を認識してゲノムDNAに結合し、遺伝子の転写を制御することで細胞の形態や性質といった運命決定に関わります。細胞内において、遺伝子の本体であるDNAは、ヌクレオソーム(注1)構造を基本単位とした染色体として折りたたまれ、転写因子の結合を阻害します。一方で、パイオニア転写因子と呼ばれる特殊な転写因子群は、標的DNA配列がヌクレオソームによって折りたたまれている場合でもDNAに結合することができ、遺伝子の転写を活性化することが報告されています。それによって、細胞の分化が誘導され、さまざまな組織や臓器が形成されていくことが明らかになっています。しかし、パイオニア転写因子がどのようにヌクレオソーム上の標的DNA配列を探索し結合するのかは、立体構造に基づく知見が乏しく、謎に包まれていました。
本研究グループは、パイオニア転写因子GATA3に着目し、最新のクライオ電子顕微鏡(注2)を使った立体構造解析と、試験管内解析、ゲノム解析を行いました。その結果、GATA3がヌクレオソームを認識して結合する際には、ヌクレオソーム上での標的DNA配列の位置が重要であること、GATA3が2つあるDNA結合領域を巧みに利用することでヌクレオソームに安定に結合することを明らかにしました。
本成果は、パイオニア転写因子がヌクレオソームに結合し、その後の転写制御を担うメカニズムを解明する上で、重要な知見を与えます。また、GATA3の遺伝子変異は乳がんや遺伝病であるHDR症候群(注3)に関与することから、今回の発見はこれらの疾患の原因解明や治療法確立のための基盤となることが期待されます。
本研究は、東京大学定量生命科学研究所のグループと、米国国立衛生研究所のPaul Wade博士および米国ノースダコタ大学の高久誉大博士との共同研究として行われました。
本研究成果は、2020年8月18日(英国時間)に英国科学誌「Nature Communications」のオンライン版に掲載される予定です。
本成果は、主に以下の事業・研究領域・研究課題などによって得られました。
- 科学技術振興機構(JST) 戦略的創造研究推進事業 ERATO
研究プロジェクト:「胡桃坂クロマチンアトラスプロジェクト」
(研究総括:胡桃坂仁志 東京大学定量生命科学研究所 教授) - 日本医療研究開発機構(AMED) 創薬等ライフサイエンス研究支援基盤事業(BINDS)
研究プロジェクト:「エピジェネティクス研究と創薬のための再構成クロマチンの生産と性状解析」
(補助事業代表:胡桃坂仁志 東京大学定量生命科学研究所 教授) - 日本学術振興会(JSPS) 新学術領域「遺伝子制御の基盤となるクロマチンポテンシャル」
研究プロジェクト:「ヌクレオソーム高次構造とダイナミクスの解析によるクロマチン潜在能の解明」
(計画研究代表:胡桃坂仁志 東京大学定量生命科学研究所 教授)
研究の背景と経緯
転写因子は特定の標的DNA配列を認識してDNAに結合するタンパク質であり、遺伝子の転写のオン・オフを制御することで、細胞の形態や性質といった運命決定に関わります。転写因子GATA3はDNAの「GATA」からなる標的DNA配列に結合し、遺伝子のオン・オフを制御することで、さまざまな細胞への分化の過程で重要な役割を果たします。GATA3が結合しうる標的DNA配列はヒトのゲノムDNA上には700万ヶ所以上存在しますが、実際にはGATA3は細胞内でおよそ5万ヶ所にしか結合しません。このことは、転写因子GATA3のゲノムDNAへの結合は、細胞内では、染色体によるゲノムDNA折りたたみ構造によって制御されていることを示唆しています。この染色体でのDNAの折りたたみ構造を「クロマチン」と呼びます。
クロマチンの基盤構造であるヌクレオソームは、4種類のヒストンタンパク質からなるヒストン8量体にDNAが1.7回巻きつくことで形成されています。ゲノムDNA上に形成されるヌクレオソームは、転写因子のDNAへの結合を阻害することが知られていました。しかし近年、ヌクレオソームに結合できる転写因子として「パイオニア転写因子」群の存在が明らかになり、ヌクレオソームに折りたたまれたDNA上で標的DNA配列を探索するメカニズムの解明が注目されています。パイオニア転写因子であるGATA3は、ヌクレオソームに結合した後、周辺のクロマチン構造を変化させることで転写を活性化させることが知られていますが、これらの詳細な分子メカニズムは謎に包まれています。
研究の内容
東京大学定量生命科学研究所の胡桃坂仁志教授らの研究グループは、米国国立衛生研究所のPaul Wade博士および米国ノースダコタ大学の高久誉大博士と共同で、パイオニア転写因子であるGATA3に着目し、最新のクライオ電子顕微鏡による立体構造解析を中心に、ゲノム解析と試験管内解析とを組み合わせることで、生体内でGATA3が標的とするヌクレオソームと結合する詳細な分子メカニズムを明らかにすることに成功しました。
まず本研究では、ゲノム解析を行うことで、GATA3が標的とするヌクレオソームの正確な形成位置を決定しました(図1左上)。これらの情報に基づいて、GATA3の標的DNA配列を持つヌクレオソームを試験管内で再構成することで作りだし、GATA3とヌクレオソームの詳細な結合試験を行いました(図1右上)。その結果、GATA3のヌクレオソームへの結合は、その標的DNA配列のヌクレオソーム上での位置に強く依存していることが明らかになりました。
そして、クライオ電子顕微鏡を用いた立体構造解析を行うことにより、GATA3とヌクレオソームとの複合体の3次元構造を得ることに世界で初めて成功しました(図1下)。得られた立体構造より、GATA3は2つあるDNA結合領域を巧みに利用することで、ヌクレオソーム自体の構造を大きく変化させることなく安定にヌクレオソーム中の標的DNA配列に結合することが明らかになりました。
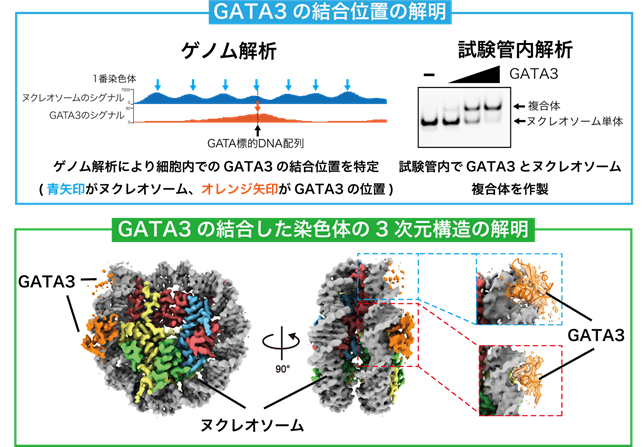
また、試験管内解析と立体構造解析の結果から、GATA3が安定にヌクレオソームに結合するためには、ヌクレオソームDNA上にGATA3の標的DNA配列が、6-7塩基対の間隔で並行して存在していることが重要であることもわかりました。実際に細胞内でのGATA3の結合領域をゲノム解析により探索すると、2つのGATA3標的DNA配列が、試験管内解析と立体構造解析の結果と同様に、6-7塩基対の間隔で配置されていることがわかりました。
今後の展開
今回の研究から、細胞の中でGATA3がヌクレオソームに結合する際には、認識DNA配列がヌクレオソーム中の特定の位置にあり、2つのGATA3標的DNA配列が特定の間隔で配置されていることが重要であることを発見しました。今回得られたGATA3とヌクレオソームの複合体の構造は、GATA3が転写を活性化する前段階の状態であると考えられ、GATA3の結合によって引き起こされる周辺領域のクロマチンの構造変換メカニズムの解明に重要な足がかりを与えました。
またGATA3の遺伝子変異は、乳がんや遺伝病であるHDR症候群において報告されています。これらの疾患では、GATA3のヌクレオソームへの結合に必要な2つのDNA結合領域に多くの変異が見られます。これらの変異がGATA3の細胞内でのヌクレオソーム結合活性や転写制御能力にどのように影響を及ぼすか、さらには乳がんなどの疾患とどのように関わるのかは現時点では不明ですが、今回の研究成果はこれらの疾病の原因解明や治療法確立に向けて重要な情報を提供します。
用語解説
- (注1)ヌクレオソーム
- 真核生物のゲノムDNAを折りたたむ基盤となる構造。4種類のヒストンタンパク質からなるヒストン8量体に、DNAが1.7回巻きついた円盤状の構造体。
- (注2)クライオ電子顕微鏡
- 液体窒素冷却下で電子線を照射し、試料を原子レベルで観察することのできる装置。タンパク質などの生体分子を急速凍結することにより、溶液状態に近い構造を観察できる。2017年にノーベル化学賞の対象になった技術で、近年の目覚ましい技術革新により、高分解能でのタンパク質の立体構造解析が可能になった。
- (注3)HDR症候群
- 副甲状腺機能低下、難聴、腎形成不全を特徴とする、常染色体優性遺伝形式の疾患。GATA3遺伝子の変異が原因となることが報告されている。
論文タイトルと著者
- タイトル:
- Interaction of the pioneer transcription factor GATA3 with nucleosomes
- 著者:
- Hiroki Tanaka, Yoshimasa Takizawa, Motoki Takaku, Daiki Kato, Yusuke Kumagawa, Sara A. Grimm, Paul A. Wade, and Hitoshi Kurumizaka
- 掲載誌:
- Nature Communications
- DOI番号:
- 10.1038/s41467-020-17959-y
お問い合わせ先
研究に関すること
胡桃坂仁志(クルミザカヒトシ)
東京大学 定量生命科学研究所 教授
〒113-0032 東京都文京区弥生1-1-1
TEL:03-5841-7826 FAX:03-5841-1468
E-mail:kurumizaka“AT”iqb.u-tokyo.ac.jp
報道担当
東京大学定量生命科学研究所 総務チーム
〒113-0032 東京都文京区弥生1-1-1
TEL:03-5841-7813
E-mail:soumu“AT”iqb.u-tokyo.ac.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
AMEDの事業に関すること
創薬等ライフサイエンス研究支援基盤事業(BINDS)担当
日本医療研究開発機構 創薬事業部 医薬品研究開発課
〒100-0004 東京都千代田区大手町1-7-1 読売新聞ビル
TEL:03-6870-2219 FAX:03-6870-2244
E-mail:20-ddlsg-16“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年8月18日
最終更新日 令和2年8月18日


