低分子化合物との併用による PD-1阻害抗体がん免疫治療効果の大幅な増強
成果情報
国立大学法人京都大学
国立研究開発法人日本医療研究開発機構
京都大学大学院医学研究科の 本庶 佑(ほんじょ たすく)客員教授、茶本 健司(ちゃもと けんじ)特定講師、理化学研究所統合生命医科学研究センター Fagarasan Sidoniaチームリーダーの研究グループは、PD-1阻害による抗腫瘍効果を大幅に増強する併用治療法を発見した。ミトコンドリアを活性化する低分子化合物をPD-1阻害抗体と併用すると、キラーT細胞のミトコンドリア活性の増強に伴い、マウスに移植したがんが急速に退縮し、生存期間が大幅に延長した。この研究成果は、米国科学アカデミー紀要(Proceedings of the National Academy of Sciences of the United States of America)で発表された。
1.背景と目的
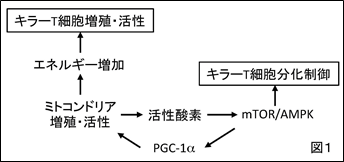
免疫のブレーキ分子であるPD-1はキラーT細胞上に発現し、がん細胞などが発現するPD-L1と結合するとキラーT細胞のがんに対する細胞傷害活性を減弱させる。本庶研究室ではPD-1とPD-L1の結合を阻害することで、がん反応性T細胞を再活性化しがんを縮退する方法を2002年に発見した。現在ではヒトの各種がんでPD-1阻害抗体治療法が実用化されている。本グループはPD-1を欠損するマウスでT細胞のミトコンドリアが活性化していることを発見した。ミトコンドリアは細胞内において非常に効率的にエネルギーを産生するため、T細胞の分化・活性化に大きく影響を与える。これらの事実に基づき、ミトコンドリアを活性化させる薬剤とPD-1阻害抗体とを併用すると、がん反応性T細胞がさらに活性化し、抗腫瘍効果を増強できるのではないかという仮説を立て検証した。
2.方法と結果
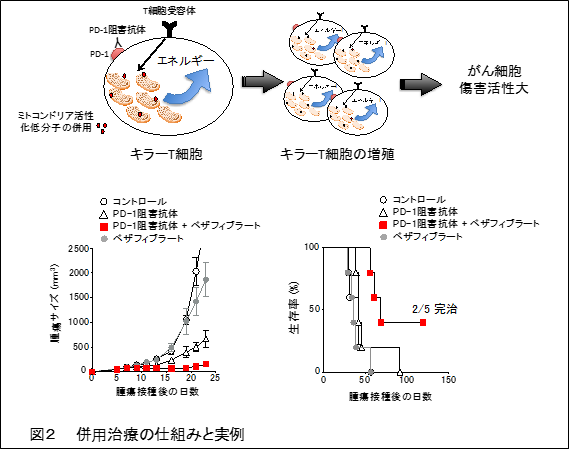
3.まとめ
- がん反応性キラーT細胞は所属リンパ節で増殖し、がん局所に移行する。リンパ節切除が外科手術で行われているが免疫治療には有害である可能性がある。
- ミトコンドリアを活性化する低分子化合物、即ち承認薬であるベザフィブラートとPD-1阻害抗体の併用で腫瘍縮退効果が著しく増強した。
- ミトコンドリア活性化マーカーがPD-1阻害治療法の有効性判定マーカーになり得る。
4.研究プロジェクトについて
本成果は、以下の研究費によって得られた。
- AMED 145208、16770835、唐奨 研究代表者:本庶 佑 研究期間:2014年4月~現在
- 若手研究(A)16748159, 細胞科学財団 研究代表者:茶本 健司 研究期間:2015年4月~現在
- AMED-CREST 14532135 研究代表:Fagarasan Sidonia 研究期間:2014年4月~現在
(本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出」研究開発領域(研究開発総括:清水 孝雄)における研究開発課題「腸内細菌叢制御による代謝・免疫・脳異常惹起メカニズムの解明と治療応用」(研究開発代表者:Fagarasan Sidonia/ファガラサン・シドニア)の一環で行われた。なお、本研究開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものである。)
論文タイトルと著者
掲載誌:PNAS
お問い合わせ先
研究に関する連絡先
〒606-8501 京都市左京区吉田近衛町京都大学医学部A棟1階129号室
京都大学医学部医学研究科免疫ゲノム医学 茶本健司
AMEDに関する連絡先
国立研究開発法人日本医療研究開発機構(AMED)戦略推進部 研究企画課
最終更新日 平成29年2月7日


