タンパク質結晶から自動でデータ収集する「ZOOシステム」を開発―誰でも簡単に構造解析に必要な高品質データを取得可能に―
成果情報
理化学研究所
高輝度光科学研究センター
日本医療研究開発機構
理化学研究所(理研)放射光科学研究センター生命系放射光利用システム開発チームの平田邦生専任技師、山下恵太郎基礎科学特別研究員(研究当時)、山本雅貴チームリーダーらの共同研究チーム※は、大型放射光施設「SPring-8」[1]のビームラインを利用して、タンパク質結晶から自動的にX線結晶構造解析[2]に必要な高品質のデータを収集する「ZOOシステム」を開発しました。
本研究成果は、放射光施設を利用したデータ収集を容易にするものであり、今後、結晶さえ準備できれば誰でも簡単にタンパク質の詳しい構造を知ることが可能になると期待できます。
これまで平田専任技師らは、1~10マイクロメートル(μm、1μmは1,000分の1mm)の高フラックス微小X線ビーム[3]を利用したビームラインBL32XUでのタンパク質の微小結晶構造解析のために、種々の測定技術を開発してきました。例えば、試料結晶への放射線損傷[4]を低減することで高品質なデータを収集する技術(KUMA)、目視で確認できない結晶を微小X線で走査・検出するための高速二次元走査システム、走査システムから出力される大量の回折画像を解析して結晶位置を特定するシステム(SHIKA)、回折データをほぼ自動的に構造解析に利用するデータとして出力する技術(KAMO)などです。
今回、共同研究チームは、これらの要素技術を組み合わせた自動データ収集システムZOOを開発し、タンパク質結晶から自動(無人)でデータ収集することに成功しました。
本研究は、英国の科学雑誌『Acta Crystallographica Section D』の掲載に先立ち、オンライン版(2019年1月28日付け)に掲載されました。
※共同研究チーム
- 理化学研究所 放射光科学研究センター 利用システム開発研究部門
- 生物系ビームライン基盤グループ 生命系放射光利用システム開発チーム
- 専任技師 平田 邦生(ひらた くにお)
- 基礎科学特別研究員(研究当時)山下 恵太郎(やました けいたろう)(現 客員研究員)
- 専任技師 上野 剛(うえの ごう)
- 専任技師 河野 能顕(かわの よしあき)
- チームリーダー 山本 雅貴(やまもと まさき)
- 高輝度光科学研究センター タンパク質結晶解析推進室
- チームリーダー 長谷川 和也(はせがわ かずや)
- 室長 熊坂 崇(くまさか たかし)
研究支援
本研究は、科学技術振興機構(JST)さきがけ「超薄膜を利用した膜タンパク質の迅速・高分解能構造解析手法の開発(代表・平田邦生)」、日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業「創薬等ライフサイエンス研究のための相関構造解析プラットフォームによる支援と高度化(SPring-8/SACLAにおけるタンパク質立体構造解析の支援および高度化)(研究代表者:山本雅貴)」および日本学術振興会(JSPS)科学研究費補助金 研究活動スタート支援「多数の微小結晶を用いた結晶構造解析手法および自動化システムの開発(研究代表者:山下恵太郎)」などの支援を受けて行われました。
背景
タンパク質の構造をより詳しく知ることは、そのタンパク質の働きを正しく理解する上で重要です。放射光施設を利用したタンパク質のX線結晶構造解析は、その目的を果たす強力な手法のうちの一つといえます。しかし、膜タンパク質[5]やタンパク質複合体のように単離・精製しにくく、結晶化が非常に難しい場合もあります。また、仮に結晶が得られたとしても、結晶が非常に小さくデータ収集が困難となることもしばしばあります。
大型放射光施設「SPring-8」は、高フラックス微小X線ビームを利用できる世界有数の施設です。なかでも、理研ターゲットタンパクビームラインBL32XUでは、サイズが10マイクロメートル以下の結晶からでも良質なデータを収集できるように、各辺が1~10μmに集光されたX線ビームを利用できます。
この微小ビームの性能を最大限に活用すべく、平田専任技師らは2010年以降、さまざまな測定技術および測定システム(INOCC、SHIKA、KUMA、HEBI、HITO、KAMOなど)の開発を進めてきました。
今回、共同研究チームは、これらのシステムを組み合わせることで、ビームラインで行うX線回折実験の自動化を試みました。
研究手法と成果
共同研究チームは、ビームラインBL32XUを利用して、タンパク質結晶から自動的にX線結晶構造解析に必要な高品質のデータを収集する「ZOOシステム」を開発しました(図1)。まず、その構成要素と役割を説明します。
「INOCC(イノシーシー)」は、結晶ホルダー(ループ)センタリングプログラムで、ゴニオメータ上にマウントされたループの外形を認識して、X線照射位置へ移動させ、X線で二次元走査する領域を決定します。「SHIKA(シカ)」は、ループをX線で走査した結果得られた画像を解析し、回折点の有無を判定することで結晶位置を特定します。「KUMA(クマ)」は、結晶の大きさ、X線の強さと波長、取得するデータ量などから、データ収集中に重篤な放射線損傷が起きないよう露光時間を自動決定します。「HEBI(ヘビ)」は、X線に対して試料の位置調整・放射線損傷予測が難しいヘリカルデータ収集[6]を自動実行します。「HITO(ヒト)」は、ループ中にある大小異なるサイズの複数結晶について、サイズや空間的配置を考慮し、適切な測定スキーム(ヘリカルデータ収集もしくは複数部分データ集積[7])を選定して、データを収集します。これら五つの要素を「ZooNavigator」が管理し、結果の集約と命令の実行を行います。「KAMO(カモ)」は、得られたデータを自動的に処理し、さらに複数結晶から得られたデータをグルーピング(階層的クラスタリング)し、データ取捨選択も容易にほぼ全自動で行います。
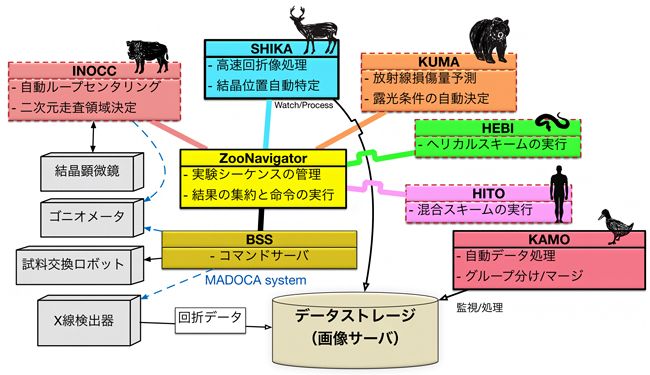
図1 自動データ収集システム「ZOOシステム」の構成図
ZOOシステムを利用すれば、放射光施設でこれまで行われてきた測定スキームを全て自動で行うことができます。例えば、最も簡単な単結晶・単点露光実験の自動測定の工程を図2に示しました。①ロボットによるループの準備、②ループの形状を認識してX線で走査する領域を決定、③X線でループを走査して結晶を探索、④結晶を回してもX線に当たり続けるように位置を決定、⑤放射線損傷を回避するよう実験条件を設定してデータ収集、これを繰り返します。
測定スキームには、ほかに「ヘリカルデータ収集」「複数部分データ集積法」「混合スキーム(ヘリカルデータ収集+複数部分データ集積)」「SSROXデータ[8]収集」が利用できます。
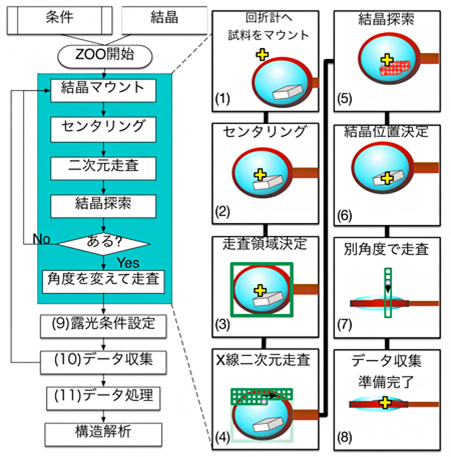
図2 ZOOシステムを利用した自動測定スキームの一例(単点露光実験の工程)
ZOOシステムの利点は、①データ測定やデータ処理に要する時間を大幅に短縮できる、②測定やデータ処理は自動(無人)でできるため、実験に人手がいらない、③データ品質を均一かつ高く保持しながらデータを収集できることです。また、すでにZOOシステムを利用した構造決定が行われています注1)。
注1)
- Morimoto, K., et al. “Crystal structure of the endogenous agonist- bound prostanoid receptor EP3”, Nat Chem Biol. 63, 1–8 (2018).
- Toyoda, Y., et al. “Ligand binding to human prostaglandin E receptor EP4 at the lipid-bilayer interface”, Nat Chem Biol. 111, 1–15(2018).
- Asada, H., et al. “Crystal structure of the human angiotensin II type2 receptor bound to an angiotensin II analog”, Nat. Struct. Mol. Biol. 25, 1–11(2018).
- Suno, R., et al. “Structural insights into the subtype-selective antagonist binding to the M2 muscarinic receptor”, Nat Chem Biol. 63, 1–13(2018).
- Shihoya, W., et al. “Crystal structures of human ETB receptor provide mechanistic insight into receptor activation and partial activation” Nat. Commun. 9, 1–11. (2018).
- Shihoya, W., et al. “X-ray structures of endothelin ETB receptor bound to clinical antagonist bosentan and its analog”, Nat. Struct. Mol. Biol. 24, 758–764(2017).
今後の期待
ZOOシステムを利用すれば、結晶さえ準備できれば専門的な知識がなくても、構造解析のための高品質データ収集が実現できます。つまり誰でも簡単に放射光施設を利用してタンパク質の高分解能データ収集ができるようになります。したがって、より多くの研究者がタンパク質の高分解能結晶構造解析を推進できるようになったといえます。当該分野への入門をご希望される方々にはぜひZOOシステムの利用を検討して頂きたいです。
また、ZOOシステムの利用実例から、データ測定の量的変化が解析の質的変化を生み出しているともいえます。微小結晶に限らず複数結晶から得られるデータを足し合わせることにより、各データに観測されている微弱な回折シグナルが積算され、1データセットだけの分解能より高分解能の構造解析が実現可能な場合が多いです。そして、ZOOシステムを利用して短時間で良質なデータ収集をより多く行えば、これまで分解能向上が見込めなかった試料でも結晶の数さえ準備すれば、簡便かつ迅速に分解能向上を目指すことも容易になったといえます。
原論文情報
Kunio Hirata, Keitaro Yamashita, Go Ueno, Yoshiaki Kawano, Kazuya Hasegawa, Takashi Kumasaka and Masaki Yamamoto, "ZOO: an automatic data-collection system for high-throughput structure analysis in protein microcrystallography", Acta Crystallographica Section D,
URL:https://doi.org/10.1107/S2059798318017795
補足説明
- [1]大型放射光施設「SPring-8」
- 理研が所有する、兵庫県の播磨科学公園都市にある世界最高性能の放射光を生み出す施設。SPring-8の名前はSuper Photon ring-8 GeVに由来。放射光(シンクロトロン放射)とは、電子を光とほぼ等しい速度まで加速し、電磁石によって進行方向を曲げたときに発生する細くて強力な電磁波のこと。SPring-8では、遠赤外から可視光線、軟X線を経て硬X線に至る幅広い波長域で放射光を得ることができるため、原子核の研究からナノテクノロジー、バイオテクノロジー、産業利用や科学捜査まで幅広い研究が行われている。
- [2]X線結晶構造解析
- 対象とする分子などの結晶を作製し、その結晶にX線を照射して得られる回折データを解析することにより、物質内部の原子の立体的な配置を調べる方法。この方法によって、タンパク質などの複雑な分子の立体構造を詳細に知ることができる。
- [3]高フラックス微小X線ビーム
- 明るくて小さなX線ビームのこと。例えばミクロンオーダーの微小な領域に多くの光子(1012光子/秒)を含むX線ビームのこと。
- [4]放射線損傷
- X線の持つエネルギーによって、X線と相互作用した分子が壊れること。X線との相互作用で分子が壊れる場合だけでなく、分子が壊れる過程で生じる電子や、壊れた分子から生成する反応性の高い分子が観察対象の分子と化学反応する場合もある。一般的にタンパク質結晶の放射線損傷は、X線と水の相互作用をきっかけに、X線照射後ピコ秒(1ピコ秒は1兆分の1秒)の時間スケールで、水から生成する反応性の高い分子がタンパク質と化学反応することで起きる。
- [5]膜タンパク質
- 細胞膜を構成しているタンパク質で、全ゲノムがコードするタンパク質の3分の1を占める。細胞膜の表面にあるタンパク質と内部に埋もれたタンパク質がある。細胞外のシグナルを捕える受容体、細胞膜を介して物質の出入を担うチャネルやポンプ、細胞同士の結合に関わる接着分子など、生命活動に重要な役割を果たす。疾病に関連しているものも多く創薬の重要なターゲットとされるが、結晶化が難しく構造解析が最も進んでいない。
- [6]ヘリカルデータ収集(法)
- 回折データは結晶を回転させながらX線を照射して測定する。ヘリカルデータ収集では放射線損傷を低減するためにデータ収集中に結晶を回転+並進させる(X線の照射位置を変えながら)。結晶サイズがX線ビームサイズよりも大きい場合に有効であることが多いが、放射線損傷の見積もりが難しいという難点があった。
- [7]複数部分データ集積(法)
- 一つの結晶から構造解析に必須な回折データ(例えば180°分)をすべて収集するのではなく、部分的な(例えば10°分)回折データを複数の結晶から収集し、足し合わせて完成させる方法。
- [8]SSROXデータ
- ホルダー上の結晶を二次元走査で探索せず、ホルダーを並進・回転させながら微小X線を高強度で照射しながらまんべんなく回折像を取得する方法。結晶探索工程の試料への損傷が重篤である場合に利用することもある。Serial Synchrotron Rotation Crystallographyの略称。
お問い合わせ先
発表者
理化学研究所 放射光科学研究センター 利用システム開発研究部門 生物系ビームライン基盤グループ 生命系放射光利用システム開発チーム
専任技師 平田 邦生(ひらた くにお)
基礎科学特別研究員(研究当時)山下 恵太郎(やました けいたろう)(現 客員研究員)
チームリーダー 山本 雅貴(やまもと まさき)
報道担当
理化学研究所 広報室 報道担当
TEL:048-467-9272 / FAX:048-462-4715
お問い合わせフォーム | 理化学研究所
高輝度光科学研究センター 利用推進部 普及情報課
TEL:0791-58-2785 / FAX:0791-58-2786
E-mail:kouhou[at]spring8.or.jp
産業利用に関するお問い合わせ
お問い合わせフォーム | 知的財産・産学連携等に関するお問い合わせ | 理化学研究所
AMED事業に関するお問い合わせ
日本医療研究開発機構 創薬戦略部 医薬品研究課
TEL:03-6870-2219 / FAX:03-6870-2244
E-mail:20-DDLSG-16[at]amed.go.jp
※上記の[at]は@に置き換えてください。
関連リンク
掲載日 平成31年2月15日
最終更新日 平成31年2月15日


