特発性基底核石灰化症のリン酸代謝改善で発症予防や進展抑制へ期待
成果情報
岐阜薬科大学
日本医療研究開発機構
概要
岐阜薬科大学薬物治療学を中心とする研究グループ(保住教授)では神経変性疾患である特発性基底核石灰化症(idiopathic basal ganglia calcification: IBGC)*1の原因遺伝子・家系・機能の解析を行ってきました。その解析を進めている過程で、SLC20A2遺伝子 *2の一つの変異でリン酸の輸送活性が約30%まで低下していても、IBGCの脳内石灰化*3や症状を全く呈していないことを、偶発的に見出しました。この事実は、IBGC患者のリン酸トランスポーター(PiT-2)を部分的にでも改善させることで、IBGCの発症予防や進展抑制ができる可能性を示唆します。本研究におけるこの発見は、今後のIBGCの治療戦略を考える上で重要な知見であると考えられます。
その成果は、2019年11月21日に英国科学誌「Scientific Reports」
『Partial reduced Pi transport function of PiT-2 might not be sufficient to induce brain calcification of idiopathic basal ganglia calcification』に公開されました。
ポイント
- 神経難病の一つであるIBGCの患者から、原因となる遺伝子SLC20A2に新たな変異を同定しました。
- SLC20A2遺伝子に変異を導入した変異型PiT-2の安定的な発現株を樹立し、リン酸の輸送活性を測定し、その低下を確認しました。
- IBGCの家系内において、脳内石灰化や症状の認められない方(非発症例)で見出したSLC20A2遺伝子の変異では、リン酸の輸送活性が正常コントロール(野生型)の約30%と部分的に保持されていました。
- この発見は、PiT-2のリン酸の輸送活性を完全ではなくても、部分的に上昇させることがIBGCの治療につながる可能性を示し、IBGCの新たな治療戦略を考える上で重要な知見と考えられます。
研究の背景
IBGCは、脳内に石灰化をきたす原因となる二次的な疾患がなく、原発性に両側の大脳基底核*4、小脳歯状核*5などに病的な石灰化を示す神経難病です。2012年に中国の研究グループが家族性IBGC(FIBGC)の原因となる遺伝子として、無機リン酸を細胞内へ輸送するリン酸トランスポーター(PiT-2)をコードするSLC20A2遺伝子の変異を報告しました。その後PDGFRB 、PDGFB 、XPR1 、MYORG と5つの原因となる遺伝子が継続して報告されています。SLC20A2遺伝子の変異は家族性IBGC患者の約半数(40~50%)を占め、最も頻度が高い原因遺伝子です。本研究室では以前にIBGC患者の全体、特にSLC20A2遺伝子の変異をもつ患者の脳脊髄液中のリン酸濃度が、健常者に比べ有意に増加していることを見出しています。このような知見から、SLC20A2遺伝子の変異によってPiT-2のリン酸の輸送能が障害され、細胞内外のリン酸代謝の恒常性の破綻が契機となり、脳内石灰化を含むIBGCの病態を引き起こすと考えられています。しかし、現在、IBGCの根本的な治療薬はまだ見つかっておらず、IBGCのさらなる病態の解明と根本的な治療法の開発が求められています。
研究の成果
本研究グループは、先ずIBGC患者と患者家族の血液から遺伝子を抽出し、4つのSLC20A2遺伝子の変異を同定しました (図1)。
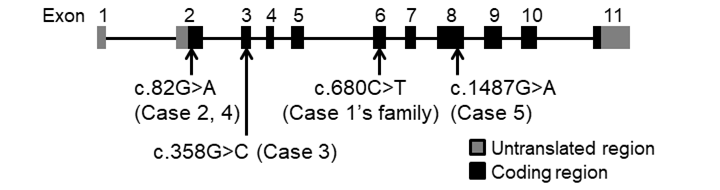
これらの変異が与える影響を変異解析ソフトPolyphen-2にて解析したところ、4つ全ての変異においてタンパク質の機能に障害を及ぼす可能性が示唆されました。次に、変異遺伝子の機能解析として、正常コントロール(野生型、WT)のPiT-2、変異型のPiT-2をそれぞれ安定的に発現するChinese Hamster Ovary (CHO)細胞を樹立しました。樹立した安定的な発現株を用いてPiT-2のリン酸の輸送活性を測定したところ、IBGC発症者の遺伝子変異型PiT-2が発現した細胞では、リン酸の輸送活性が著しく低下していた一方で、IBGC家系内の脳内石灰化や症状が認められない方(非発症例)で見出した遺伝子変異においては、野生型PiT-2の約30%のリン酸の輸送活性が保持されていることを見出しました(図2)。以上の結果から、PiT-2のリン酸の輸送活性が変異によって部分的に低下しても、IBGCの病態を引き起こさない可能性が示唆されました。
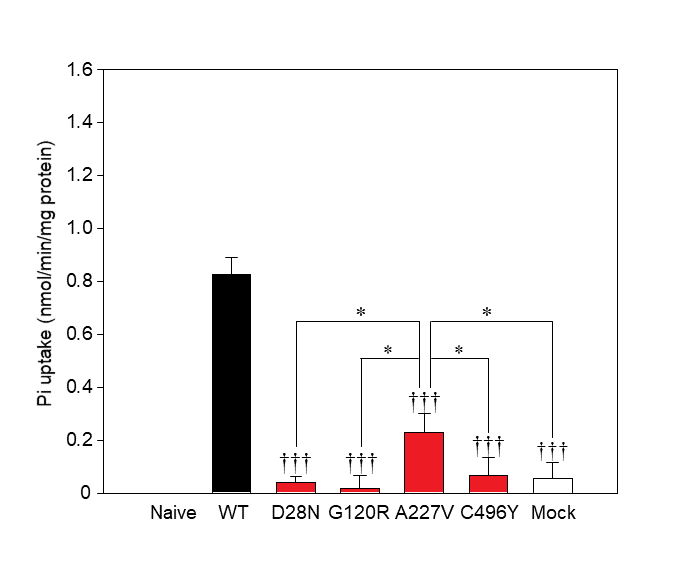
今後の展開
本研究から、PiT-2が持つリン酸の輸送活性の部分的な低下では、IBGCの病態を示さないことが明らかとなりました。すなわち、この事実はリン酸の輸送活性を完全ではなくとも部分的に上昇させることで、IBGCの病態の改善に繋がるのではないかと期待できます。しかし、治療法を考える上で解決すべき課題も多く残っています。IBGC患者においてSLC20A2遺伝子の変異は常染色体優性遺伝*6であり、野生型PiT-2と変異型PiT-2の両方が発現していると考えられています。そのため、変異型PiT-2が野生型PiT-2に対して示す優性阻害効果*7、あるいはハプロ不全*8によるPiT-2の発現量の相対的な低下によって、IBGCが発症しているかどうかについてはまだ議論が続いています。さらなるIBGCの解明に向けて、岐阜薬科大学薬物治療学研究室を中心に、東京大学、京都大学、新潟大学脳研究所などと連携して、現在、IBGC患者から樹立した疾患特異的なiPS細胞や遺伝子変異の疾患モデルマウスを作製して、より詳細な発症機構の解明や治療薬の開発について研究を行っています*9。
用語解説等
- *1 特発性基底核石灰化症 ( IBGC )
- 脳内の大脳基底核や小脳歯状核(以下で説明)などに原因不明の石灰化を認め、様々な進行性の神経症状を呈する神経変性疾患です。パーキンソン病様症状、小脳症状、精神症状、認知症といったさまざまな症状を呈しますが、中には無症状の方もいます。日本では現在、約300症例が登録されています。詳しい家系調査はされていませんが、多くは孤発例です。
- *2 SLC20A2遺伝子
- Ⅲ型Na依存性リン酸トランスポーターであるPiT-2をコードしている遺伝子で、生体内のリン恒常性を維持しています。2012年にIBGCの原因遺伝子として同定された後、世界中の研究グループから多数の変異が報告されています。。
- *3 石灰化
- 軟部組織にカルシウム(Ca)などのミネラル(鉱物)が沈着する病態です。IBGCでは毛細血管周囲や小動脈血管の中膜平滑筋に認められます。これはリン酸代謝の恒常性が破綻し、無機リン酸とCaを主体とした重金属との錯体で形成されると考えられます。石灰化(calcification)よりむしろ鉱物化(mineralization)がより厳密な病態を表現しています。
- *4 大脳基底核
- 大脳の深い所にあり、皮質と視床、脳幹を結びつけている神経核(神経細胞の集団)です。線条体、淡蒼球、視床下核、黒質があります。その障害によってさまざまな運動障害や姿勢障害などが生じます。
- *5 小脳歯状核
- 小脳の深い所にある4対の神経核(神経細胞の集団)の一つです。運動機能と認知機能などに関係する信号を出力します。
- *6 常染色体優性遺伝
- メンデルの遺伝形式では、子供は両親のどちらか一方から受け継いだ遺伝形質を発現します。どちらか一方に特徴が出やすい遺伝子(優性)があった場合、その表現型(症状)を発現します。
- *7 優性阻害効果
- タンパク質が多量体を形成して機能するときなど、変異タンパク質の存在によって正常タンパク質の機能が阻害されてしまう現象です。
- *8 ハプロ不全
- 一対の遺伝子のうち片方に変異が起こり、野生型遺伝子から産生されるタンパク質の量では、変異型遺伝子によるタンパク質の不足分を補填できずに機能不全を起こす現象です。
- *9 参考論文
-
- 1) Functional evaluation of PDGFB-variants in idiopathic basal ganglia calcification, using patient-derived iPS cells.
- Sekine SI, Kaneko M, Tanaka M, Ninomiya Y, Kurita H, Inden M, Yamada M, Hayashi Y, Inuzuka T, Mitsui J, Ishiura H, Iwata A, Fujigasaki H, Tamaki H, Tamaki R, Kito S, Taguchi Y, Tanaka K, Atsuta N, Sobue G, Kondo T, Inoue H, Tsuji S, Hozumi I.
- Sci Rep. 2019 Apr 5;9(1):5698.
- https://www.nature.com/articles/s41598-019-42115-y.pdf
- 2) SLC20A2 variants cause dysfunctional phosphate transport activity in endothelial cells induced from Idiopathic Basal Ganglia Calcification patients-derived iPSCs.
- Sekine SI, Nishii K, Masaka T, Kurita H, Inden M, Hozumi I.
- Biochem Biophys Res Commun. 2019 Mar 5;510(2):303-308.
論文情報
- 発表雑誌
- Scientific Reports
2019 Nov 21;9(1):17288 - DOI
- 10.1038/s41598-019-53401-0
- URL
- https://www.nature.com/articles/s41598-019-53401-0.pdf
- 論文タイトル
- Partial reduced Pi transport function of PiT-2 might not be sufficient to induce brain calcification of idiopathic basal ganglia calcification.
- 著者
- Nishii K, Shimogawa R, Kurita H, Inden M, Kobayashi M, Toyoshima I, Taguchi Y, Ueda A, Tamune H, Hozumi I.
(西飯 和哉、下川 梨津子、栗田 尚佳、位田 雅俊、小林 道雄、豊島 至、田口 芳治、植田 晃広、田宗 秀隆、保住 功)
研究支援
本研究は岐阜薬科大学薬物治療学のIBGC研究グループ(西飯 和哉、下川 梨津子、栗田 尚佳、位田 雅俊、保住 功)が中心となり、国立病院機構あきた病院神経内科 小林 道雄先生、豊島 至先生、富山大学病院神経内科(現 たぐちクリニック)田口 芳治先生、藤田医科大学神経内科 植田 晃広先生、東京都立多摩総合医療センター 精神神経科 田宗 秀隆先生との共同研究によって成されたものです。
これらの研究成果はAMED難治性疾患実用化研究事業(特発性基底核石灰化症の基盤にあるリン酸ホメオスターシス異常を改善する特殊環状ペプチドダイマーを活用した治療薬の開発、および特発性基底核石灰化症の診療、病態解明、創薬のためのエビデンス創出研究)、日本学術振興会科学研究費助成事業 基盤研究(B)(脳内石灰化症の分子病態の解明と新規治療法の開発)、厚生労働科学研究費 難治性疾患等政策研究事業(神経変性疾患領域における基盤的調査研究(分担、(代表 中島 健二))などの研究費を受けてまとめられた研究成果です。
お問い合わせ先
研究に関する問い合わせ先
岐阜薬科大学薬物治療学
教授 保住 功
〒501-1196岐阜市大学西1丁目25-4
TEL:058-230-8121
E-mail:hozumi”AT”gifu-pu.ac.jp
AMED事業に関する問い合わせ先
日本医療研究開発機構 戦略推進部 難病研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2223
E-mail:nambyo-info”AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年1月10日
最終更新日 令和2年1月10日


