脂肪酸を分解する代謝経路活性を生きた細胞で可視化することに成功―細胞代謝の理解と創薬研究の前進に期待―
成果情報
国立大学法人九州大学
国立研究開発法人日本医療研究開発機構
概要
九州大学薬学研究院の王子田彰夫教授、内之宮祥平助教、大戸茂弘教授、松永直哉准教授らの研究グループは、脂肪酸を分解する代謝経路である脂肪酸β酸化の活性を生細胞で蛍光イメージングすることが可能な蛍光プローブの開発に成功しました。
本研究の成果は2020年2月12日に英国王立化学会誌「Chemical Communications」のオンライン版で公開されました。
研究の背景
代謝経路とは複数の酵素による連鎖的な反応であり、解糖系などの多様な代謝経路が生命活動の維持に重要な役割を果たしています。これら代謝経路の活性はガンを始めとする病態細胞において通常細胞と比較して変化していることから、代謝経路の活性を検出可能な技術の開発は疾病メカニズムの解明や創薬研究に大きく貢献できると期待されます。従来、代謝経路の活性の検出には安定同位体標識※1した化合物の代謝挙動を質量分析によって追跡する手法などが用いられてきましたが、生きた細胞で検出することや1細胞ごとの違いを解析することは困難でした。一方、近年では酵素活性を生きた細胞で蛍光イメージングするための蛍光プローブ※2の開発が盛んに行われています。しかし、従来の蛍光プローブの応用は単一の酵素反応の検出に限定されており、複数の酵素が連鎖的に関与している代謝経路全体の活性を生きた細胞で検出可能な蛍光プローブの開発例はありませんでした。
研究の概要
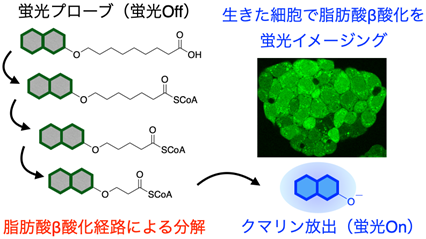
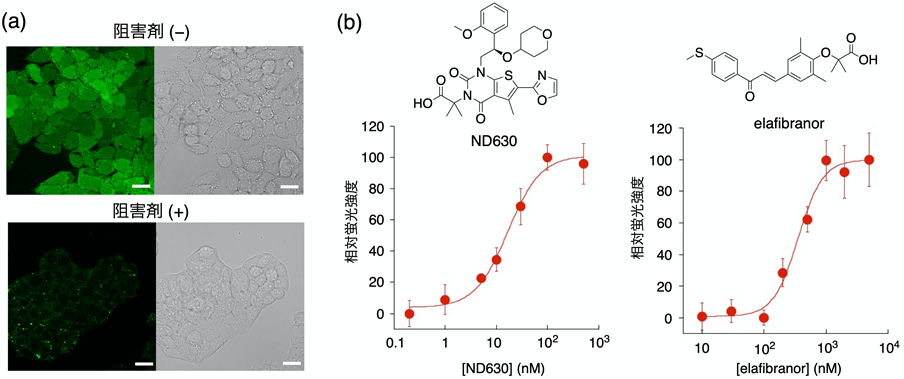
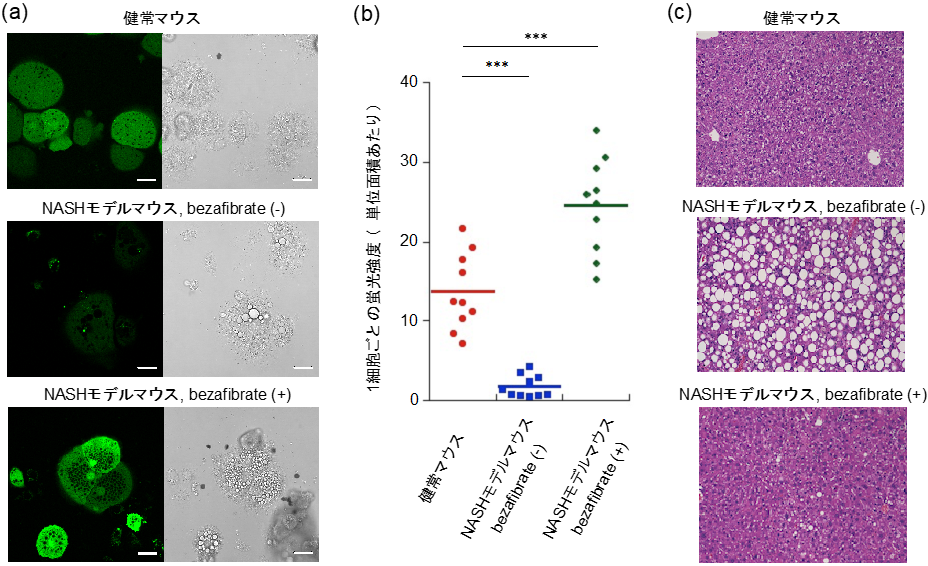
本研究では、代謝経路の1つである脂肪酸β酸化を生きた細胞で蛍光イメージングするための新しい蛍光プローブを開発しました。脂肪酸β酸化は、ミトコンドリアなどで脂肪酸を分解することでATP生産に用いられるアセチルCoAなどを供給する重要なエネルギー生産経路の1つであり、その異常は非アルコール性脂肪肝炎(NASH)や心疾患などの疾病とも深く関連していることが報告されています。今回我々は、蛍光色素(クマリン)に脂肪酸を導入した蛍光プローブを新たに設計しました。この蛍光プローブは反応前では蛍光Off状態となっていますが、蛍光プローブに導入されている脂肪酸鎖が生細胞内で脂肪酸β酸化の酵素群によって分解反応を受けると、クマリンが放出され蛍光On状態となります(図1)。本蛍光プローブを用いて、肝臓ガン由来の細胞株であるHepG2細胞など様々な細胞株で脂肪酸β酸化活性を蛍光検出することに成功しました(図2a)。また、脂肪酸β酸化活性を変化させる薬剤(ND630、elafibranor)を細胞に添加したところ薬剤濃度依存的にクマリン蛍光強度が増加したことから、薬剤添加に伴う脂肪酸β酸化活性の変化を追跡可能であることを明らかとしました(図2b)。さらに我々は、マウスの肝臓から単離した初代培養細胞での脂肪酸β酸化活性の蛍光イメージングが可能であることを見出しました(図3)。特にNASHモデルマウスに対しbezafibrate※3を経口投与した場合、クマリン蛍光が大きく増加することが分かりました(図3a, 3b)。肝臓のヘマトキシリン・エオジン(HE)染色からは脂肪滴と思われる構造体が消失していることから(図3c)、薬剤投与と脂肪酸β酸化活性変化の相関を蛍光イメージングによって検出している事が示されました。
今後の期待
本研究によって開発された蛍光プローブは、重要なエネルギー生産経路の1つである脂肪酸β酸化の活性を生きた細胞で蛍光イメージングすることが可能な初めてのケミカルツールです。また、細胞の主要代謝経路全体の活性を検出可能な初めての蛍光プローブの例となります。本蛍光プローブは今後に脂肪酸β酸化経路を標的とした薬剤探索などの創薬研究への応用が期待されます。
本研究の成果は、国立研究開発法人日本医療研究開発機構(AMED)創薬等先端技術支援基盤プラットフォーム(BINDS)「グリーンファルマを基盤にした創薬オープンイノベーションの推進(研究代表者:大戸茂弘)」、日本学術振興会科研費新学術領域研究「分子夾雑の生命化学(領域代表者:浜地格)」(課題番号JP17H06349)などの支援を受けて実施されました。
用語説明
- ※1 安定同位体標識
- 化合物に13Cや15Nなどの安定同位体を導入すること。安定同位体で標識された化合物は天然の化合物と性質は同じだが質量が異なるため、標識化合物の挙動を質量分析によって選択的に検出することが可能となる。
- ※2 蛍光プローブ
- 特定の生体分子と選択的に反応することで、蛍光特性が変化する化合物。生細胞など、様々な生体分子が共存する環境下で、標的生体分子の挙動や活性などを蛍光イメージングによって選択的に検出することができる。
- ※3 bezafibrate
- 核内受容体であるperoxisome proliferator-activated receptor(PPAR、ペルオキシソーム増殖剤活性化レセプター)α/δのアゴニスト。BezafibrateがPPARα/δを活性化することで、脂肪酸β酸化関連のタンパク質の発現量が増加する。
掲載論文
- 雑誌名:
- Chemical Communications
- 論文名:
- Fluorescence Detection of Metabolic Activity of Fatty Acid Beta Oxidation Pathway in Living Cells
- 著者名:
- Shohei Uchinomiya, Naoya Matsunaga, Koichiro Kamoda, Ryosuke Kawagoe, Akito Tsuruta, Shigehiro Ohdo and Akio Ojida*(* 責任著者)
- 掲載日時
- 2020年2月12日
- DOI:
- 10.1039/C9CC09993J
お問い合わせ先
研究に関すること
九州大学大学院薬学研究院創薬ケミカルバイオロジー分野
TEL:092-642-6596
E-mail:ojida"AT"phar.kyushu-u.ac.jp
AMED事業に関すること
国立医療研究開発法人日本医療研究開発機構(AMED)創薬戦略部 医薬品研究課
TEL:03-6870-2219
E-mail:20-DDLSG-16"AT"amed.go.jp
※Emailは上記アドレス"AT"の部分を@に変えてください。
掲載日 令和2年3月10日
最終更新日 令和2年3月10日


