自閉症や統合失調症、薬物依存など、様々な精神疾患に関わるAUTS2遺伝子がシナプスの形成や恒常性維持に関わることを発見
成果情報
国立研究開発法人国立精神・神経医療研究センター
国立研究開発法人日本医療研究開発機構
国立研究開発法人国立精神・神経医療研究センター(NCNP)神経研究所病態生化学研究部の堀啓室長および星野幹雄部長らの研究グループは、自閉症や統合失調症、薬物依存など、様々な精神疾患に関わるAUTS2遺伝子1)が中枢神経のシナプス形成やその恒常性維持に関わることを明らかにしました。
AUTS2遺伝子は、自閉症スペクトラム障害や統合失調症、ADHD、薬物依存症、てんかんなど様々な精神・神経疾患に広く関連することが分かっていました。この遺伝子がコードするAUTS2タンパク質(以下、AUTS2と略す)は、胎児期や乳児期の脳の中で神経細胞の形態や動きを制御したり、脳の発達に関わる様々な遺伝子の発現を調節したりするなど、多様な働きを持つタンパク質であることが示されていました。一方で、AUTS2は成熟した成人の脳にも存在しますが、その働きについてはほとんど分かっておらず、この遺伝子の異常がどのようにして様々な精神疾患を引き起こすのかも明らかにされていませんでした。
このたび、星野・堀らの研究グループは、生後、脳が発達していく過程で活発に作られたり取り除かれたりする「シナプス(神経細胞同士の結合部分)」に着目し、AUTS2がシナプス形成2)に果たす新たな役割を明らかにしました。脳内の神経細胞は、神経活動を促す「興奮性シナプス」と、逆にそれを抑え込む「抑制性シナプス」で繋がっており、これらの数がバランスよく保たれることで、健やかな精神活動が営まれます。本研究グループは、AUTS2が興奮性シナプスの新規形成を抑え、刈り込み2)を促進することで、結果的に興奮性シナプスの数が増えすぎないように調整していることを見出しました。一方で、抑制性シナプスに対してはこのような働きがありません。AUTS2の機能が失われると、興奮性シナプスの数は増えますが抑制性シナプスは変わらないため、興奮性/抑制性のバランスが破綻してしまい、脳が常に興奮した状態になってしまいます。今回の発見から、AUTS2遺伝子の変異を持つ患者さんでは、脳内の興奮性/抑制性シナプスバランスが破綻した結果、てんかんや各種精神症状が引き起こされることが示唆されました。今回の成果は、神経接続の基本単位であるシナプスの数を制御するメカニズムを明らかにしただけでなく、各種精神疾患やてんかんなどの発症機構の理解にもつながるものだと考えられます。
本研究成果は日本時間2020年6月26日13時(報道解禁日時:米国東部時間6月26日午前0時)に、米国のオンライン総合学術雑誌「iScience」に掲載されました。
研究の背景
AUTS2遺伝子(Autism Susceptibility Candidate 2)は、2002年に自閉症と関係のある遺伝子として初めて報告されました。また、その後、この遺伝子の異常が自閉症だけでなく、統合失調症や知的障害、ADHD(注意欠如・多動症)、薬物依存、てんかんなど、様々な精神・神経疾患患者でも見つかり、AUTS2遺伝子が精神発達障害に広く関わることが示唆されてきました。この遺伝子から生み出されるAUTS2タンパクは神経細胞の核や細胞質に存在していますが、長い間その働きについてはほとんどわかっておらず、この遺伝子の異常がどのように精神疾患を引き起こすのかは明らかにされていませんでした。
2014年に星野・堀らの研究グループは、細胞質に存在するAUTS2が、細胞の形態や動きを制御する細胞骨格系タンパク質に働きかけることで、胎児期から乳児期の正常な脳内で起こる神経細胞の移動や神経突起の伸展などを調節するタンパク質であることを明らかにしてきました。また、他の研究グループからは、核に存在するAUTS2が、様々な遺伝子の発現を調節する転写調節因子としても働くことが報告されてきました。一方で、AUTS2は出生後や成熟した成人の脳においても存在しています。また、AUTS2は大脳の前頭野や海馬といった、脳の中でも特に高いレベルでの精神機能(記憶、学習、意思決定やコミュニケーションなど)に関わる脳部位に強く発現しています。しかしながら、生後の脳発達や成熟した脳においてAUTS2がどのような働きをしているのか、また、なぜAUTS2遺伝子に異常があると自閉症などの精神疾患を発症するのかは不明のままでした。そこで、マウス遺伝学を用いた実験によって、神経系ネットワークの基本単位である「シナプス」に着目し、この遺伝子の異常によって引き起こされる精神疾患の病理に迫りました。
研究の概要
神経細胞同士を繋ぐ「シナプス」は、乳児期から思春期にかけて活発に作られ、脳神経系ネットワークを形成していきます。成人の脳でも記憶や学習、あるいはストレスといった身体内外からの刺激に応答してその数は増減しますが、正常な脳ではある一定数に保たれるように調節されています。中枢神経系のシナプスは大まかに、「興奮性シナプス」と「抑制性シナプス」に分けられます。身体内外からの刺激や情報を受け取って活性化した(興奮した)神経細胞は、その情報を「興奮性シナプス」を介して次の神経細胞へと伝えます。一方で、「抑制性シナプス」は、情報を伝え終えた神経細胞の活動を低く抑えたり、あるいは情報が間違った神経ネットワーク内に入り込まないようブロックしたりするような役目を担っています。これら2種類のシナプスの数は厳密にコントロールされており(これを「シナプス恒常性」といいます)、神経系ネットワークの興奮性/抑制性のバランスを保つことで、正常な精神活動が営まれます。逆に、このシナプス恒常性に変調をきたすと、様々な精神疾患が引き起こすことが知られています。
今回の研究で星野・堀ら研究グループは、Auts2遺伝子を破壊したマウス(ノックアウトマウス)では、大脳前頭野や海馬などの脳領域において新規に作られる興奮性シナプスの数が増大し、逆に不要な興奮性シナプスを刈り込む機能が低下していることを見出しました(図1)。
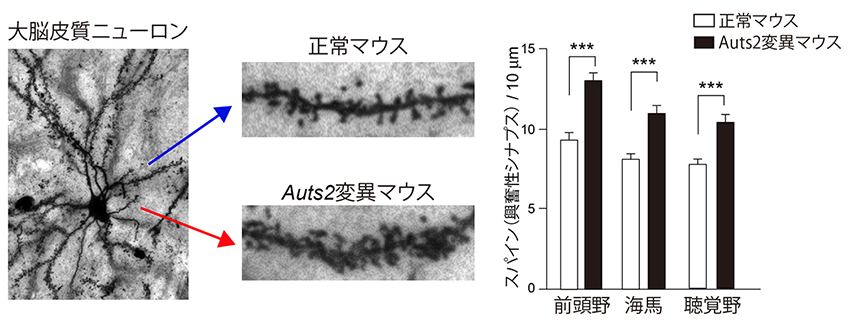
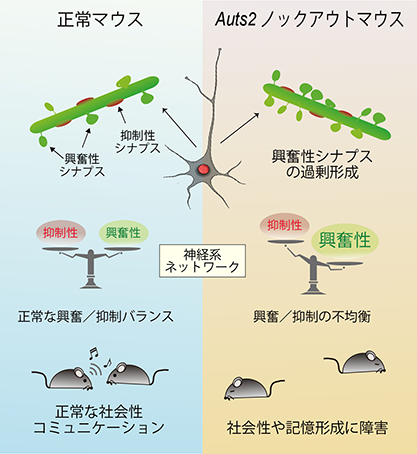
本研究から、AUTS2遺伝子の異常がシナプス恒常性の破綻を引き起こし、様々な精神疾患を惹起する基盤となっているということが示唆されました。
今後の展望
上記のように、AUTS2遺伝子は様々な精神疾患に関わります。これまで自閉症や統合失調症などの精神疾患は、臨床症状が異なることから、それぞれ異なる種類の障害によって引き起こされると考えられてきました。しかし、AUTS2遺伝子の変異によって惹起されるシナプスの異常という病理が、様々な精神疾患の発症に広く共有されている可能性があることを示唆しています。
今回の研究で作製したAuts2ノックアウトマウスで見られる神経ネットワークの障害が、精神疾患患者でも同じように引き起こされていると考えられることから、このモデル動物をさらに詳しく調べていくことで、有効な治療法の開発につなげることができると大いに期待されます。
用語の説明
- 1)AUTS2遺伝子
- ヒト第7染色体上の全長約120万塩基にもおよぶ広い領域に存在する遺伝子。2002年に自閉症との関連が指摘されたが、その後、ADHD、知的障害、統合失調症、薬物依存症、などの幅広い精神疾患と関わることがわかってきた。AUTS2遺伝子領域は比較的脆弱で、破壊されやすいとされている。この遺伝子のコードするAUTS2タンパクには、これといった分子モチーフが無く、その働きは長らく謎のままであった。過去に我々は、AUTS2タンパクの細胞質における働きを明らかにしたが、このタンパク質が細胞核においても何らかの役割を果たしている可能性があると考えている。
- 2)シナプス形成と刈り込み
- 神経細胞同士を繋ぐシナプスは、胎生後期から思春期にかけて活発に形成されるが、その後、不要となった余剰のシナプスは積極的に取り除かれる(これを「シナプス刈り込み」という)。興奮性シナプスの情報の受け手側(後シナプス)は、神経細胞の樹状突起からちょうど、棘のように突き出た様な形をしていることからスパイン(棘)とも呼ばれる。成人の脳でも学習や経験などの刺激に応じてシナプス数は増減するが、正常な脳ではある一定数に保たれている。主に死後脳を用いた解析から、精神疾患患者の脳ではスパインの形態異常や数の増減が起こっていることが、最近の研究から分かってきた。
原著論文情報
- 論文名:
- AUTS2 regulation of synapses for proper synaptic inputs and social communication.
- 著者:
- Kei Hori, Kunihiko Yamashiro, Taku Nagai, Wei Shan, Saki F. Egusa, Kazumi Shimaoka, Hiroshi Kuniishi, Masayuki Sekiguchi, Yasuhiro Go, Shoji Tatsumoto, Mitsuyo Yamada, Reika Shiraishi, Kouta Kanno, Satoshi Miyashita, Asami Sakamoto, Manabu Abe, Kenji Sakimura, Masaki Sone, Kazuhiro Sohya, Hiroshi Kunugi, Keiji
- 掲載誌:
- iScience 2020
- doi:
- 10.1016/j.isci.2020.101183
研究経費
本研究結果は、以下の日本学術振興会・科学研究費補助金、日本医療研究開発機構「脳科学研究戦略推進プログラム」および国立精神・神経医療研究センター精神・神経疾患研究開発費の支援を受けて行われました。
お問い合わせ先
研究に関するお問い合わせ
星野幹雄(ほしのみきお)
国立精神・神経医療研究センター 神経研究所
病態生化学研究部
〒187-8502 東京都小平市小川東町4-1-1
TEL:042-346-1722(代表) FAX:042-346-1752
E-mail:hoshino“AT”ncnp.go.jp
報道に関するお問い合わせ
国立精神・神経医療研究センター 総務課広報係
〒187-8551 東京都小平市小川東町4-1-1
TEL:042-341-2711(代表) FAX:042-344-6745
E-mail:ncnp-kouhou“AT”ncnp.go.jp
AMED事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構
疾患基礎研究事業部 疾患基礎研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2286 FAX:03-6870-2243
E-mail:brain-pro“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和2年7月13日
最終更新日 令和2年7月13日


