細胞老化の多様性とそのメカニズムを提唱―代謝とエピゲノムによるバリエーションの形成―
成果情報
熊本大学
日本医療研究開発機構
ポイント
- 細胞老化※1は持続的な増殖停止の状態であり、炎症性タンパク質などを多量に合成・分泌するため、身体全体の個体老化※2の重要な要素である
- 細胞老化には開始期(増殖停止)、早期(抗炎症)、完成期(炎症と代謝増加)、後期(炎症と代謝減少)の少なくとも4つの表現型バリエーション※3がある
- 細胞内代謝※4とエピゲノム※5(遺伝子のON/OFF制御)の変換が協調的に行われる「細胞老化のプログラム」によって、老化細胞のバリエーションが形成される
- 細胞老化の表現型バリエーションという新しい観点から、老化過程のメカニズムの理解、加齢性疾患の制御・予防法の促進が期待される
概要説明
熊本大学発生医学研究所細胞医学分野の中尾光善教授の研究グループは、細胞老化を防ぐ酵素の探索によって、エピゲノムの修飾酵素「SETD8メチル基転移酵素」※6と「NSD2メチル基転移酵素」※7がそれぞれ特定の遺伝子群の働きを調節して細胞老化を防ぐこと、また、細胞老化の過程でこれらの酵素が著しく減少する結果、老化細胞※1が生じることを報告してきました。これらの成果及び他研究グループの報告をもとに、今回、細胞老化のメカニズムや老化細胞に多様性があることを新たに提唱するものです。
現在、細胞老化と個体老化について数多くの研究が国際的に行われており、細胞老化は個体老化(身体全体の老化)の重要な要素であることが明らかとなってきています。モデル動物を用いて、老齢個体には老化細胞が蓄積すること、また老化細胞を除去すると加齢による機能低下が抑えられることなど、新しい知見が発表され続けています。他方、老化細胞はこうしたマイナスの面だけでなく、組織の形成・維持や再生に働いていること、がん化を阻止する防御機構であることなどのプラスの面があります。しかしながら、老化細胞を検出するバイオマーカーは老化特異的なものではなく、細胞老化の過程をどのように理解したらよいかが科学的に問われています。
本論文は、細胞から放出される生理活性物質サイトカイン※8の合成・分泌の特徴から、細胞老化には少なくとも4つの段階(4つの表現型バリエーション)が存在すること、このバリエーションは代謝とエピゲノムの協調的な変換で生じること、細胞老化のバリエーションという新たな観点から老化過程を理解することが加齢性疾患の制御・予防法につながることを提唱するものです。質的に異なる細胞老化の状態を特徴づけて分類することで、加齢や老化過程を新たな視点で理解できると期待されます。
本研究成果は、文部科学省科学研究費補助金、日本医療研究開発機構(AMED)革新的先端研究開発支援事業、内藤記念振興財団研究助成などの支援を受けて、科学雑誌「Trends in Cell Biology」(電子版)に米国時間の令和2年9月23日に掲載されました。
説明
我が国の高齢化は、世界に類を見ないスピードで進展し、今後も高齢人口の増加が予測される中、“健康を維持しながら老いる”ことが重要な課題となっています。身体を構成する多くの細胞は、分裂を繰り返すと、やがてその機能が低下して増殖を停止します。この状態を「細胞老化」と呼び、健康と寿命に関わる重要な要素と考えられています(図1)。細胞老化は、放射線や紫外線、薬剤などのストレスによってゲノムDNAが損傷を受けると促進されることが知られていますが、細胞老化のメカニズムはまだ十分には分かっていません。また、細胞老化には良い点も悪い点もあります。例えば、細胞ががん化を始めると、細胞老化が生じてがんの発生を防ぐ役割をもちます。他方で、細胞老化によってさまざまな加齢性の病気が起こりやすくなります。したがって、細胞老化を理解して適切に制御することが大切です。
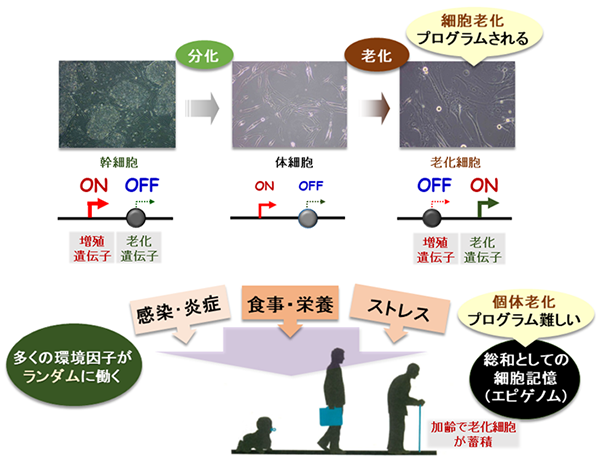
(下段図は「体質と遺伝子のサイエンス」(中尾光善著、羊土社)から転載・一部修正)
老化細胞は増殖能を失っていますが、近年、老化細胞がさまざまなタンパク質を分泌して周囲の細胞に働きかけることにより、慢性的な炎症やがん細胞の増殖を促進することが注目されています。これを老化関連性分泌表現型(SASP)とよびます。このように、老化細胞はアクティブに働いているため、細胞老化は、身体全体の「個体老化」の原因になると考えられています(図1)。例えば、老齢マウスの体内には老化細胞が蓄積していきますが、これらを除去すると全身の老化が抑えられる、また、老化細胞が分泌するタンパク質を阻害することが効果的であるという報告があります。つまり、細胞老化を制御できれば、全身の老化の進度を調節できる可能性があります。
本研究グループは、「エピジェネティクス」とよばれる学問の観点から、細胞老化のメカニズムについて研究を進めています。エピジェネティクスは、すべての遺伝子の働き方(遺伝子のON/OFF制御)を明らかにする研究分野であり、生命現象や病気の発症、さらに老化にも密接に関わると考えられます。ヒトの設計図に当たるゲノムには、約2万5千個の遺伝子(タンパク質をつくる)があります。これまでの研究成果として、ヒト線維芽細胞(すべての組織・器官に存在する細胞種)の老化に関わる因子を幅広くスクリーニングして、「SETD8メチル基転移酵素」、「NSD2メチル基転移酵素」などが細胞老化を防ぐ役割をもつことを報告しました。
しかしながら、老化細胞に特異的なバイオマーカーは今なお発見されておらず、細胞老化の過程をどのように理解したらよいかが科学的に問われています。このため、この過程を細胞老化として一括りに扱うのはなく、現在までの知見を総じて、その時間経過とタンパク質分泌SASPの特徴から考察することとしました。その結果、細胞老化には、①開始期(増殖停止)、②早期(炎症を抑える)、③完成期(炎症と代謝増加)、④後期(炎症と代謝減少)の少なくとも4つの段階(4つの表現型バリエーション)があることを提示しました(図2)。それぞれの時期の分子レベルの変化に着目して、細胞内代謝とエピゲノム(遺伝子のON/OFF制御)の変換が協調的に行われる「細胞老化のプログラム」によって、細胞老化のバリエーションが形成される可能性を指摘しました。
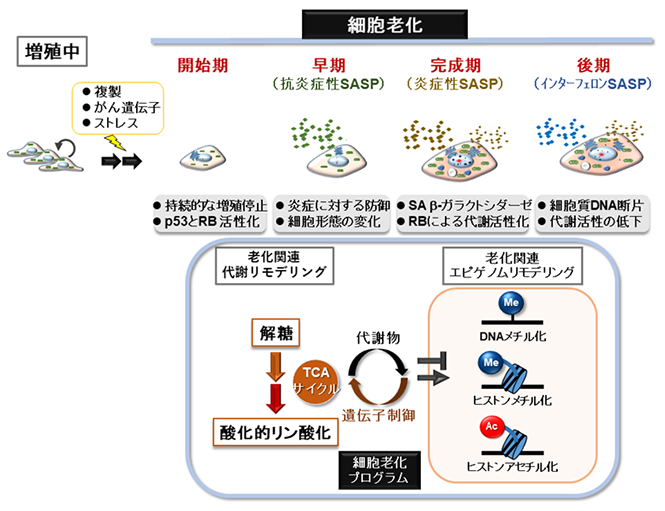
さらに、細胞老化の過程で重要な機能を果たす遺伝子において、その発現制御に働く転写因子※9とエピゲノム修飾酵素に注目しました。まず、開始期では、細胞増殖を促す遺伝子の働きが抑制されて、逆に、増殖を阻止する遺伝子が働きます。これにはがん抑制タンパク質のp53とRBが主な役割を果たすことが知られています。次に、早期では、細胞形態が大きく変化するとともに、炎症を抑える性質のサイトカインが働きます。これは、この後に続く炎症反応に対する防御になる可能性があります。完成期では、炎症性サイトカインの遺伝子が強く働いて炎症反応を生じます。これとともに、前述したRBは、代謝に関わる遺伝子とタンパク質を合成する遺伝子の発現を増加させます。タンパク質を合成・分泌するためには、代謝でエネルギーを産生する必要があると考えられます。後期では、炎症反応や代謝が低下しますが、細胞質内に放出されたゲノムDNAの断片やミトコンドリアDNAに反応して、インターフェロン(サイトカインの一種)の合成・分泌が生じます。現在、これら一連のメカニズムや意義はまだ解明されていませんが、細胞老化では質的に異なる炎症反応が連動していることが理解できます。
今回の学術的な考察は、細胞老化の表現型バリエーションという観点から、細胞老化と個体老化のメカニズムを新たに理解して、健康長寿や加齢性疾患の新たな制御・予防法の創出を促す契機になることが期待できます。
用語解説
- ※1:細胞老化
- DNA損傷、がん遺伝子の活性化、ストレスなどで誘導される持続的な細胞増殖の停止。持続的に増殖を停止した細胞を「老化細胞」という。炎症性タンパク質などを合成・分泌し、慢性の炎症をおこす。
- ※2:個体老化
- 加齢によって生じる身体全体の変化。主に老齢個体の状態。
- ※3:表現型バリエーション
- 細胞・組織・個体などがもつ特徴を「表現型」と呼ぶ。例えば、同じ細胞が異なる特徴をもつように変化した場合、バリエーションとよぶ(多様性とほぼ同義)。
- ※4:細胞内代謝
- 細胞が糖・タンパク質・脂質などを利用して、ミトコンドリアを中心にエネルギーと代謝物を産生・消費する仕組み。代謝経路には数多くの酵素が連動しており、これらの遺伝子の発現をエピゲノムが制御している。
- ※5:エピゲノム
- アセチル化やメチル化など、化学修飾されたゲノムを「エピゲノム」とよぶ。主には、DNAが巻き付いているヒストンというタンパク質が修飾される。修飾基(アセチル基、メチル基など)は細胞内の代謝物に由来している。
- ※6:SETD8メチル基転移酵素
- タンパク質を構成する特定のリジン(アミノ酸)にメチル基を付ける修飾酵素。SETD8はヒストンのうちの1つ「ヒストンH4」の20番目のリジンをメチル化し、タンパク質合成遺伝子の働きを抑制する。
- ※7:NSD2メチル基転移酵素
- タンパク質を構成する特定のリジン(アミノ酸)にメチル基を付ける修飾酵素。NSD2は「ヒストンH3」の36番目のリジンをメチル化し、増殖遺伝子の働きを促進する。
- ※8:サイトカイン
- 多くの細胞で合成されて、主に炎症応答に働く分泌性タンパク質。抗炎症性(TGF-b)、炎症性(インターロイキン6、8など)、インターフェロンなどがある。
- ※9:転写因子
- 遺伝子の近傍にある特異的な塩基配列に結合して、転写の活性化又は不活性化をおこすタンパク質。エピゲノム因子を特定の遺伝子近傍にリクルートする役割を果たす。
論文情報
- 論文名
- Cellular senescence variation by metabolic and epigenomic remodeling
- (代謝とエピゲノムの変換による細胞老化の表現型バリエーション)
- 著者名
- Mitsuyoshi Nakao*, Hiroshi Tanaka, and Tomoaki Koga(*責任著者)
- 掲載誌
- Trends in Cell Biology (Cell Press)
- DOI
- 10.1016/j.tcb.2020.08.009
- URL
- https://www.cell.com/trends/cell-biology/fulltext/S0962-8924(20)30170-7
お問い合わせ先
内容に関するお問い合わせ
熊本大学発生医学研究所 細胞医学分野
担当:教授 中尾光善(なかおみつよし)
TEL・FAX:096-373-6804
E-mail:mnakao“AT”kumamoto-u.ac.jp
AMEDの事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構
シーズ開発・研究基盤事業部 革新的先端研究開発課
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年10月7日
最終更新日 令和2年10月7日


