新型コロナウイルス検出酵素試薬の開発―独自酵素開発酵素によるOne-step real-time RT-PCR法―
成果情報
大阪府立病院機構
大阪母子医療センター研究所免疫部門
京都大学大学院農学研究科食品生物科学専攻
関西学院大学生命環境学部生物科学科
阪大微生物病研究会
日本医療研究開発機構
研究成果のポイント
- 独自酵素によるone-step real-time RT-PCR(注1)法を開発した
- 増幅時間が短く、検出感度が高い
- 新たな感染症や、変異型に対しても迅速に対応できる
- 緊急時の研究用試薬として、大阪府立病院機構において数万テスト分を常備
- 新型コロナウイルス研究用試薬として利用可能
概要
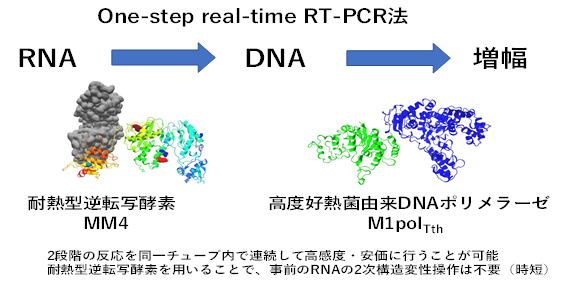
このほど、大阪母子医療センター・柳原格部長を中心とする研究チーム(※1)は、改良した耐熱性逆転写酵素(注2)、独自のDNAポリメラーゼ(注3)の組み合わせで、高感度に新型コロナウイルスの核酸を検出するキットを開発しました(図)。この方法で、溶液中5分子の新型コロナウイルスRNAを1時間以内に検出できました。また、大阪府立病院機構における研究(※2)において、保険収載された既存の新型コロナウイルス核酸増幅キットと比較した場合、本開発キットの感度は99.44%、特異度は100%でした。核酸増幅酵素試薬キットについての研究成果は、2021年6月5日付科学誌PLOS ONEに発表されました。
※1:大阪母子医療センター研究所免疫部門 免疫部長 柳原格、京都大学大学院農学研究科食品生物科 教授 保川清、関西学院大学生命環境学部生物科学科 教授 藤原伸介、一般財団法人阪大微生物病研究会 主査 鈴木孝一朗
※2:大阪はびきの医療センター感染症内科 主任部長 田村嘉孝、大阪急性期総合医療センター総合内科 主任部長 大場雄一郎、大阪母子医療センター臨床検査科 主任部長 位田忍、大阪母子医療センター集中治療科 主任部長 竹内宗之
研究背景・内容
感染症診断において核酸増幅法の重要性が増しています。感染症の迅速な診断法の確立は、その後の感染症対策及び患者の生命予後を左右します。また、2020年COVID-19のパンデミックは、世界的な医療資材、病原体検出用試薬の枯渇をもたらしました。医療崩壊を招かない為にも、そして感染症制御の観点からも、病原体検出用試薬の確保をしておくことの重要性が改めて浮き彫りにされました。
本研究グループでは、SARS-CoV-2をモデルとして高感度に病原体RNAを検出するのに適したone-step real-time RT-PCR法を開発しました。逆転写酵素には、保川らが開発したMolony murine leukemia virus由来の逆転写酵素に4カ所の変異を導入し耐熱性を付与した逆転写酵素(MM4)を用いました。また、逆転写反応後続くPCR反応には、藤原らが鹿児島県トカラ列島の熱水域から分離したThermus thermophilus M1株のDNAポリメラーゼM1polTth、Thermotoga petrophila K4株由来のDNAポリメラーゼに変異を加えたK4polL329A、Thermococcus kodakarensis KOD1株のKOD DNAポリメラーゼに既報の変異を導入したRTXの3種類のDNAポリメラーゼを、患者由来のRNAで反応を行う事を想定した5種類の異なる反応溶液で比較検討しました。これらの、逆転写反応及びPCR反応を連続反応として同一チューブ内で行った結果、5種類の反応溶液条件の中でも幅広く10,000コピーのSARS-CoV-2 RNAの増幅が可能であったのは、MM4とM1polTthの組み合わせで、幅広い溶液中での核酸増幅は、臨床サンプルを用いる場合には適していると考えられました(図1)。
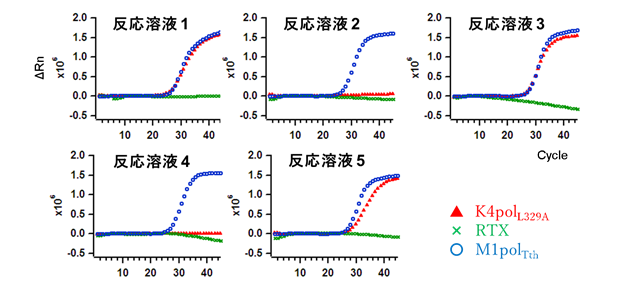
MM4とRTXの組み合わせでは、標的配列の増幅が確認できなかった。
MM4とM1polTthの組み合わせでは、全ての反応溶液で標的配列の増幅が確認された。
次にこの5種類の反応溶液における検出限界(注4)を検討したところ、反応溶液4(詳細は論文中に記載)の中で、リアルタイムPCR法のほぼ限界と同等の、合成したSARS-CoV-2RNA5分子が検出できました(図2)。
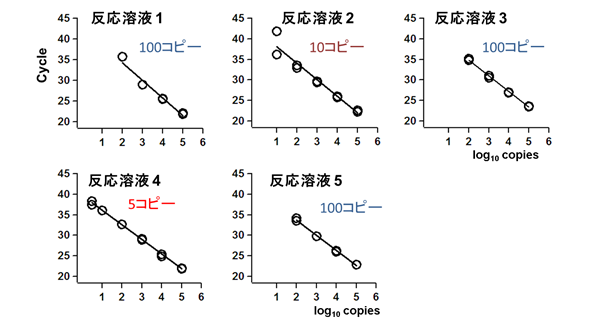
反応溶液2では10コピーが、反応溶液4では5コピーの標的RNAが検出された。
また、213例のCOVID-19患者由来のRNAサンプルを用い、開発した方法(MoCOキット)と市販の診断キットとの性能を比較したところ、感度は99.44%、特異度は100%でした(図3)。
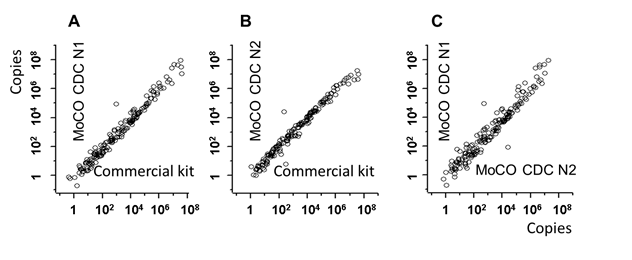
- CDC N1プライマーとプローブセットを使用したMoCOキットと、CDC N1およびN2プライマーとプローブを使用した市販キットの比較
- CDC N2プライマーとプローブセットを使用したMoCOキットと、CDC N1およびN2プライマーとプローブを使用した市販キットの比較
- CDC N1プライマーとプローブセットを使用したMoCOキットと、CDC N2プライマーとプローブセットを使用したMoCOキットの比較
COVID-19の病初期には非常に多いウイルスが産生されることが知られています。今回の開発酵素の組み合わせでは、1テストあたり107コピーを超えるウイルス量の検出も可能であり、臨床現場で利用可能な研究用試薬として十分な性能を発揮しました。
今後の展開
本開発キットは、新たな感染症や、遺伝子の違い(変異)にも柔軟に対応することが出来ます。すでに柳原らは研究用試薬として新型コロナウイルスの変異株のスクリーニングに日常的に利用しています。解析で得られた情報は、次世代シーケンスによるゲノム情報とあわせて、厚労省「積極的疫学調査及び変異株に関する情報提供等への協力」要請に基づき、大阪府感染症対策企画課を通じて厚労省へ提供すると共に、SARS-CoV-2のゲノムデータベースにもその情報を提供しています。また、開発キットは緊急時の研究用試薬として大阪府立病院機構に保存しています。
研究費
AMED 新興・再興感染症に対する革新的医薬品等開発推進研究事業(柳原、保川、藤原、鈴木)
日本学術振興会科研費(柳原)
中谷医工計測技術振興財団(特別研究助成)(柳原、保川、藤原)
一般財団法人阪大微生物病研究会(共同研究費)(柳原、保川、藤原)
大阪府新型コロナウイルス感染症検査機関等設備整備事業(大阪府立病院機構)
大阪府立病院機構研究活動等支援(柳原)
論文情報
- 掲載雑誌
- PLoS One. 2021 Jun 4;16(6):e0252789.
- タイトル
- Development of an efficient one-step real-time reverse transcription polymerase chain reaction method for severe acute respiratory syndrome-coronavirus-2 detection
- 著者名
- Yukiko Nakura1, Heng Ning Wu1, Yuya Okamoto2, Muneyuki Takeuchi3, Koichiro Suzuki4, Yoshitaka Tamura5, Yuichiro Oba6, Fumiko Nishiumi1, Nobuaki Hatori4, Shinsuke Fujiwara7, Kiyoshi Yasukawa8, Shinobu Ida2, Itaru Yanagihara1,2*
- 所属
- 1Department of Developmental Medicine, Research Institute, 2Department of Laboratory Medicine, 3Department of Intensive Care Medicine, Osaka Women’s and Children’s Hospital, Izumi-city, Osaka, Japan
4The Research Foundation for Microbial Diseases of Osaka University, Suita-city, Osaka, Japan
5Department of Clinical Laboratory, Osaka Habikino Medical Center, Habikino-city, Osaka, Japan
6Department of General Medicine, Osaka General Medical Center, Osaka-city, Osaka, Japan
7Department of Biosciences, School of Biological and Environmental Sciences, Kwansei-Gakuin University, Sanda-city, Hyogo, Japan
8Division of Food Science and Biotechnology, Graduate School of Agriculture, Kyoto University, Kyoto-city, Kyoto, Japan
*Corresponding author - doi
- 10.1371/journal.pone.0252789
用語説明
- (注1)One-step real-time reverse transcription PCR
- One-step real-time RT-PCRは1本鎖cDNA合成(逆転写)反応とPCR反応を同じチューブ内で連続して行う定量PCRの事をいう。病原体解析においてはより操作の少ない本定量法は、より安全性が高いと共に、操作上の偽陽性、偽陰性を減らすこともできる。
- (注2)逆転写酵素
- RNAを鋳型としてそれに相補的なDNAを合成する酵素。RNA依存性DNAポリメラーゼ(RNA dependent DNA polymerase)とも呼ばれる。
- (注3)DNAポリメラーゼ
- DNAポリメラーゼ(DNA polymerase; -ポリメレース)は1本鎖の核酸を鋳型として、それに相補的な塩基配列持つDNA鎖を合成する酵素をさす。
- (注4)検出限界
- 検出できる最小量(値)のこと。定量が可能な最小量を示す定量下限とは異なる。
本件に関する問い合わせ先
研究に関すること
大阪府立病院機構 大阪母子医療センター
研究所免疫部門 部長 柳原格(やなぎはら いたる)
TEL:0725-56-1220(内5301)
報道に関すること
大阪府立病院機構 大阪母子医療センター
事務局 総務人事グループ 中野嘉子(なかの よしこ)
TEL:0725-56-1220(内3272)
AMED事業に関する問い合わせ先
日本医療研究開発機構(AMED)
創薬事業部 創薬企画・評価課
新興・再興感染症に対する革新的医薬品等開発推進研究事業
TEL:03-6870-2226
E-mail:shinkou-saikou“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和3年7月30日
最終更新日 令和3年7月30日


