再生医療等データ登録システム
 再生医療等データ登録システム(NRMD)の構築
再生医療等データ登録システム(NRMD)の構築
戦略推進部 再生医療研究課
再生医療の臨床研究から製品市販後調査までのデータを横断活用
一般社団法人日本再生医療学会は、再生医療の臨床研究と製品開発の促進、安全性・有効性の保証などを目的として、「再生医療等臨床研究データ登録システム(NRMD)」を構築しました。今後、大きな発展が予想される再生医療などの開発を支えるため、再生医療などに特化した信頼性の高いデータをオールジャパンで一元管理することを目指しています。
取り組み
再生医療は、これまで有効な治療法のなかった疾患の治療ができるようになるなど期待が高い一方で、新しい医療であることから、安全性を確保しつつ慎重かつ迅速に研究開発を進める必要があります。再生医療の進展を受けて、国は、2014年11月、医薬品医療機器法に新たに「再生医療等製品」を追加するとともに、「再生医療等の安全性の確保等に関する法律」を定めました。再生医療の臨床研究も今後ますます増加していくと思われますが、従来の医薬品や医療機器の臨床研究データベースは「再生医療等製品や細胞加工物を用いた研究」の評価に必要なデータを登録できる形式ではないことや、これまで限られた研究機関でしか実施されていないため、経験・ノウハウ・臨床データが共有されていないことが課題となっていました。
日本再生医療学会(JSRM)は、AMEDの再生医療臨床研究促進基盤整備事業「再生医療等臨床研究を支援する再生医療ナショナルコンソーシアムの実現」において、「臨床研究等支援」「教育」「データベース構築」という3本柱で研究開発を推進しています。その一環として、再生医療などに特化した信頼性の高いデータをオールジャパンで一元管理することを目指し、「再生医療等臨床研究データ登録システム(NRMD)」を構築しました。厚生労働省、医薬品医療機器総合機構(PMDA)と連携しながら運用していきます。
臨床研究から市販後までの長いフェーズをカバーするため、臨床研究に対応する「再生医療等臨床研究データ登録システム(NRMD/CR)」、市販後調査に対応する「再生医療等製品使用データ登録システム(NRMD/PMS)」という2つのデータベースを構築。登録されたデータは、臨床試験の段階から再生医療安全性確保法が求めるCSV(Computerized System Validation)に準拠した品質で管理され、データの信頼性を確保した再利用が可能です。
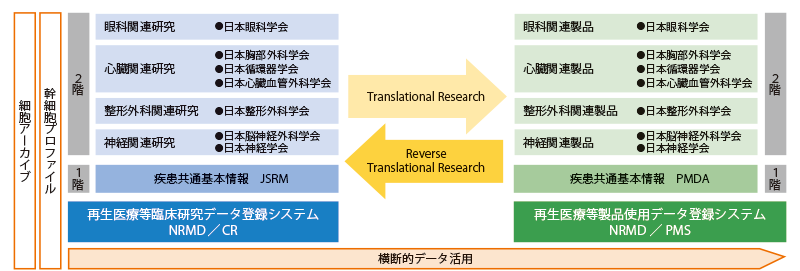
成果
NRMD/CRは2017年10月に登録を、NRMD/PMSは2018年3月に運用を開始しました。各医療機関の臨床データのほか、細胞データを集めた「幹細胞プロファイル」、臨床研究の細胞加工物を冷凍保存する「細胞アーカイブ」もシステム内に構築。臨床研究から治験までの「疾患共通基本情報」については、再生医療学会が中心となり、日本眼科学会、日本心臓血管外科学会、日本整形外科学会などと連携して開発を進めています。
展望
再生医療の臨床研究の経験やノウハウ、臨床データの共有を図ることにより、再生医療に関する優れた研究を患者さんに安全かつ迅速に届けることを目指します。再生医療ナショナルコンソーシアムは、このような研究シーズを臨床研究、実用化へと前進させるための仕組みとして、臨床研究のサポート、登録項目のチェック、臨床培養士の育成などのサポート機能も充実させ、それぞれが連携し合うことで新しい再生医療製品や治療法の開発を推進していきます。
最終更新日 平成30年11月15日


