肺がんにおける分子標的薬耐性克服に向けた新規治療法の開発
 ROS1融合遺伝子陽性肺がんにおける耐性の克服にむけて
ROS1融合遺伝子陽性肺がんにおける耐性の克服にむけて
がん研究会の片山量平部長の研究グループは、非小細胞肺がん(NSCLC, non-small cell lung cancer)に見られる様々なチロシンキナーゼ(TK)の遺伝子異常に対する治療薬の耐性化機構に着目し、頻度の高いROS1遺伝子のG2032R変異(2032番目のアミノ酸のグリシンがアルギニンに変わること)による耐性化に対して有効な薬剤を、企業との共同研究により見いだしました。本成果は、ROS1融合遺伝子陽性肺がんの将来的な治療開発に貢献しうると考えられます。
取り組み
本邦において肺がんは死亡率1位のがん種であり、肺がんの約8割以上を占める非小細胞肺がんでは、様々なチロシンキナーゼを異常に活性化する変異や融合遺伝子など、がんの進展で重要な役割を果たすドライバー遺伝子が同定され(図1)、これらの遺伝子産物(異常活性化したTK)を標的とする多くのTK阻害剤(TKI)が治療薬として承認されています。多くの症例で顕著な腫瘍縮小効果を認めますが、数年以内に薬剤耐性化し、がんが再発することが問題となっています。特に、ALKとROS1は相同性が非常に高く、複数のALK阻害薬がROS1阻害薬としても開発され、立体構造上ほぼ同じ位置に薬剤耐性の変異として多剤耐性のALK-G1202R変異やROS1-G2032R変異が報告されています。ALK-G1202R変異に有効な第3世代ALK阻害薬ロルラチニブは、ROS1に対して非常に高い阻害活性を有することが示されていましたが、ROS1-G2032Rに対する阻害活性はほとんどありませんでした。
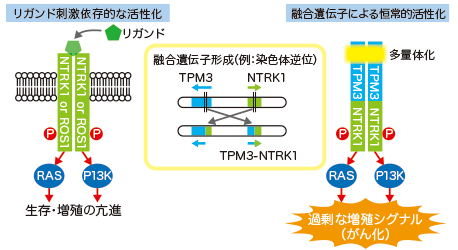
このような薬剤耐性変異による耐性克服法の探索研究を、企業との共同研究により進め、新規ROS1/NTRK阻害薬の候補化合物であるDS-6051bが、ROS1-G2032R変異および他のクリゾチニブ耐性変異を阻害できる可能性があることを見出しました。
成果
DS-6051bは、ROS1を1nM以下の低濃度で、NTRK1、2、3(Neurotrophic Tropomyosin Receptor Kinase)を10nM以下の濃度でキナーゼ阻害活性を有することをin vitroで確認しました。また、ROS1、NTRK以外に、ALKやACK(Activated Cdc42 kinase)の阻害活性も見られましたが、他のキナーゼへの阻害活性は弱く、選択性の高いROS1/NTRK阻害薬であると分かりました。次に、人工的に作製したROS1融合遺伝子(CD74-ROS1融合遺伝子)発現細胞と複数の患者(インフォームド・コンセント取得済み)から樹立したROS1融合遺伝子陽性肺がん細胞株に対する感受性試験では、DS-6051bはロルラチニブに次いで2番目に低い濃度で阻害活性を示し、クリゾチニブよりも約3倍程度低い数nMの濃度で増殖抑制することが分かりました。さらに、ROS1融合遺伝子陽性肺がん患者由来の腫瘍を移植された担がんマウスに、連日DS-6051bを経口投与すると、腫瘍が縮小する様子が観察されました。NTRK1融合遺伝子を有する大腸がん細胞株KM12での検討でも、10nM以下の濃度で細胞の増殖抑制と、KM12細胞の担がんマウスモデルでの抗腫瘍効果を確認しました。
クリゾチニブ耐性を示す5種類のROS1変異(L1951R, S1986F,L2026M, G2032R, D2033N)型CD74-ROS1をBa/F3細胞に発現させて薬剤感受性を評価した結果、DS-6051bは、D2033N以外の変異型CD74-ROS1発現Ba/F3細胞の増殖を20nM以下の低濃度で阻害し、特にG2032Rに対しては、他のROS1阻害薬と比較し、最も低い濃度で細胞増殖抑制とリン酸化ROS1の減少を認めました。CD74-ROS1-G2032R発現Ba/F3細胞の担がんマウスモデルで、DS-6051bの経口投与により腫瘍の縮小を認めました。ROS1融合遺伝子陽性肺がん細胞株HCC78細胞にG2032R変異型ROS1融合タンパク質を過剰発現した細胞を移植した担がんマウスモデルで、DS-6051bの経口投与により、長期の腫瘍縮小維持が確認されました(図2)。
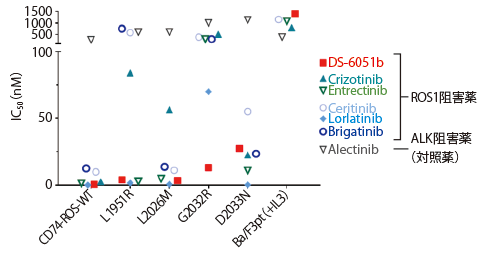
展望
本成果は、ROS1融合遺伝子陽性またはNTRK融合遺伝子陽性肺がんの将来的な治療開発に貢献しうると考えられます。DS-6051bは本邦、米国を中心にROS1融合遺伝子陽性またはNTRK融合遺伝子陽性がんを対象に臨床試験が行われています。また、本研究を基盤とする薬剤耐性変異のメカニズムの解明と耐性克服の研究を今後進めていく予定です。
関連リンク
最終更新日 令和3年8月13日


