神経核内封入体病の原因遺伝子を同定
 ロングリード・シークエンサーにより遺伝性疾患の原因遺伝子を解明
ロングリード・シークエンサーにより遺伝性疾患の原因遺伝子を解明
曽根淳(国立病院機構鈴鹿病院 第二脳神経内科医長)、松本直通(横浜市立大学大学院医学研究科 教授)、祖父江元(名古屋大学大学院医学系研究科 特任教授)らは、ロングリード・シークエンサーを用いた新しい解析手法により神経核内封入体病の原因遺伝子を同定しました。また、辻省次(東京大学医学部附属病院 特任教授)、石浦浩之(同助教)、森下真一(同大学大学院新領域創成科学研究科 教授)らは新規の解析手法を駆使し、神経核内封入体病を含む3疾患の原因遺伝子を同定しました。
取り組み
神経核内封入体病(NIID)は、全身の様々な臓器の細胞核に広く「封入体」と呼ばれる異物の存在が認められる疾患で、近年、認知症を示す神経変性疾患の一つとして注目されています。発症年齢は幼少期から高齢まで幅広く分布し家族性の発症もあることが知られていましたが、原因遺伝子は明らかではありませんでした。今回、2つの研究グループは,臨床像の類似性から特定のリピート配列の伸長の予測に基づくアプローチ、あるいは、ロング・リードシークエンサー(LRS)を用いて伸長リピート配列の探索を行うなど、異なるアプローチにより、リピート配列の伸長変異を発見しました。両グループは、それぞれ、LRSを駆使することにより、伸長リピート配列のゲノム構造を正確に決定しました。2つのグループは、LRSを有効に活用し、それぞれ独自のアプローチに基づき、神経核内封入体病の原因の解明を実現しました。
成果
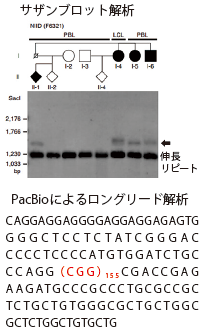
曽根らのグループは大家系の連鎖解析から責任領域を1p22.1-q21.3領域まで絞り込んだ後、LRSを用いて全ゲノム解析を行い同領域の異常を探索、神経核内封入体病の原因がNOTCH2NLC遺伝子のDNA塩基配列GGC繰り返し配列の異常伸長(リピート伸長)であることを発見しました(図1)。さらにCRISPR/Cas9を用いたゲノム編集技術と、ナノポアシークエンサー(LRSの一つ)を用いてリピート伸長を詳細に解析したところ、認知症を主症状とする場合はGGCのみのリピート伸長がみられるのに対して、末梢神経症状を主症状とする場合はGGCの繰り返しに加えてGGA配列が含まれることを明らかにしました(図2)。
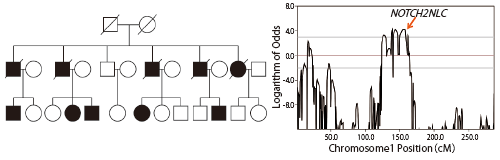

これは、リピート配列の違いにより主症状が異なる可能性を示唆するものです。
辻らのグループはショートリード・シークエンサーの解析データから未知のリピート伸長を効率良く検出できるプログラム(TRhist)を開発し、神経核内封入体病の原因がNOTCH2NLC遺伝子のCGGリピート伸長であることを見出し、LRSによりその構造を決定しました。さらに、白質脳症を伴う眼咽頭型ミオパチー(OPML)、眼咽頭遠位型ミオパチー(OPDM)においても、原因遺伝子を特定し、神経核内封入体病と同様にCGGリピートの異常伸長を突き止めました。これは、臨床像に共通点が認められる疾患において、伸長CGGリピートによってもたらされる共通した病態が存在することを示す画期的な発見でした(図3、4)。
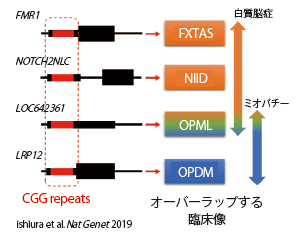
展望
世界に先駆けて、国内2つの研究グループが神経核内封入体病の原因遺伝子を同定し、遺伝性疾患の原因遺伝子解明におけるLRSの有用性を示しました。共通の症状をもつ異なる疾患に同じリピート配列の異常伸長がみられること、さらに同一疾患であってもリピート配列の一部の違いが症状の多様性につながることが示されました。この成果は、依然数多く残されている原因不明の神経筋疾患の解決に向けた大きな一歩となると期待されます。
最終更新日 令和3年8月13日


