マウス胎盤形成期前後の胚で生じるグルコース代謝経路の再編成の解明
プレスリリース
国立大学法人東京大学
国立研究開発法人日本医療研究開発機構
発表者
山口 良文 (東京大学大学院薬学系研究科 薬科学専攻 准教授)
三浦 正幸 (東京大学大学院薬学系研究科 薬科学専攻 教授)
発表のポイント
- 網羅的な代謝産物プロファイリングを行うことで、マウスの胎盤形成期前後の胚でグルコース代謝経路の再編成が生じることを明らかにしました。
- 質量分析法(注1)を用いた分子イメージング技術を用い、胚の中での代謝物の分布を可視化することに成功しました。
- マウスの胎盤形成期前後に生じるグルコース代謝経路の再編成を、発生タイミング制御に関わるとされるLin28a遺伝子の一過的な過剰発現により阻害することで、この再編成が出生後の生存に必須である可能性を示しました。
発表概要
細胞が外部から取り込んだ栄養分を代謝し、エネルギーを抽出するエネルギー代謝は、生命活動の根幹となる仕組みです。なかでもグルコース(糖)代謝は、生命活動に必要なエネルギーを供給するエネルギー代謝経路としての側面だけでなく、体を構成する核酸やアミノ酸などの生体構成因子の合成にも関わる生存に必須な経路です。近年の研究から、増殖が活発ながん細胞においてグルコース代謝経路制御の重要性が示唆されています。しかし一方で、同じく増殖が非常に活発な発生期の胎児(胚)で、グルコース代謝経路がいかに制御されるのかについては、理解が進んでいませんでした。
東京大学大学院薬学系研究科の宮沢英延元特任研究員、山口良文准教授、三浦正幸教授らは、慶應義塾大学医学部の杉浦悠毅専任講師、末松誠客員教授らと共同で、質量分析法の技術を用いた代謝産物プロファイリングにより、哺乳類研究のモデル生物であるマウスの胎盤形成期前後の胚で生じるグルコース代謝経路の再編成を明らかにしました。また、質量分析装置を用いた分子イメージング技術を用いることで、胚体内における代謝産物の空間分布パターンの可視化にも成功し、解糖系(注2)代謝産物である乳酸の分布が局所で高いことも明らかにしました。さらに遺伝学的手法を用いた解析から、胎盤形成期に生じるグルコース代謝経路の再編成が新生仔の生存に重要な役割を担う可能性も示唆されました。母体糖尿病に伴う高グルコースやある種の栄養欠乏など、細胞の代謝状態を撹乱するような因子に胎児がさらされると、胎盤形成時に形成される脳のもととなる神経管形成等にも異常を示します。本研究で明らかになった成果は、そのような非遺伝的母体環境要因により引き起こされる先天異常の発症機構解明にも有用と期待されます。
発表内容
研究背景
哺乳類の胎盤形成期には、母体と胚との間のガスや栄養供給形式が大きく変化するとともに、胎児の劇的な成長および様々な組織での細胞分化が同時進行します。また母体糖尿病に伴う高グルコースなど、細胞のエネルギー代謝状態を撹乱するような因子に胚がさらされると、胎盤形成期に進行する神経管閉鎖過程等に異常を示すことが知られています。このように、哺乳類胎盤形成期の胚で生じるグルコース代謝状態の変化を解明することは生物学的、医学的に重要な課題であると考えられることから、質量分析法の技術を用いることでこの点の解明を目指しました。
研究内容
今後の展望
本研究により、マウスの胎盤形成期の胚においてグルコース代謝経路の再編成が生じることが明らかとなりました。このような発生過程と協調したグルコース代謝経路の再編成が、胎盤形成による母体と胚との間のガス・栄養供給形式の変化により誘導されるものなのか、あるいはそのような外的要因とは独立した内因性の発生プログラムによって制御されているものなのかは興味深い点です。また、胎盤形成期の代謝状態変化が胚発生過程において担う役割の解明も今後の研究課題です。ショウジョウバエを用いた研究では、特定の発生時期に糖代謝が急激に活性化されることで、その後の劇的な体のサイズの増大が可能になると示唆されています。マウスをはじめ哺乳類の胎盤形成期はちょうど胚の劇的な成長と様々な組織での細胞分化が始まる時期にあたるため、今回明らかになったグルコース代謝経路の再編成と酸化的リン酸化への切り替えは、胎児の体サイズの制御と組織の機能的分化に重要な役割を果たす可能性があります。
本研究は、文部科学省科学研究費補助金基盤研究(S)「発生頑強性を規定する細胞死シグナルの解明」および「細胞外コミュニケーションを発動する死細胞からの分泌機構」(研究代表者:三浦正幸)、文部科学省科学研究費補助金新学術領域研究「細胞死を起点とする生体制御ネットワークの解明」(研究代表者:山口良文)、国立研究開発法人日本医療研究開発機構革新的先端研究開発支援事業(AMED-CREST)の研究開発領域「生体恒常性維持・変容・破綻機構のネットワーク的理解に基づく最適医療実現のための技術創出」(研究開発総括:永井良三)における研究課題「個体における組織細胞定足数制御による恒常性維持機構の解明」(研究代表者:三浦正幸)の一環で行われました※。なお、本AEMD-CREST研究開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。
※共同研究先の慶應義塾大学には、AMED-CRESTの研究費は支出されておりません。
発表雑誌
- 雑誌名:
- Development (2017) 144, 63-73 doi: 10.1242/dev.138545
- 論文タイトル:
- Rewiring of embryonic glucose metabolism via suppression of PFK-1 and aldolase during mouse chorioallantoic branching.
- 著者名:
- Hidenobu Miyazawa, Yoshifumi Yamaguchi*, Yuki Sugiura, Kurara Honda, Koki Kondo, Fumio Matsuda, Takehiro Yamamoto, Makoto Suematsu, and Masayuki Miura*
お問い合わせ先
研究内容に関するお問い合わせ先
東京大学大学院薬学系研究科 薬科学専攻
准教授 山口 良文(やまぐち よしふみ)
教授 三浦 正幸(みうら まさゆき)
〒113-0033 東京都文京区本郷7-3-1
Tel:03-5841-4863/4860
E-mail:bunbun“AT”mol.f.u-tokyo.ac.jp/miura“AT”mol.f.u-tokyo.ac.jp
事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 研究企画課
Tel:03-6870-2224 Fax:03-6870-2243
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
用語解説
- (注1)質量分析法:
- 分子やイオンの質量電荷比(m/z)を測定する分析法。それぞれの分子はそれぞれ固有の質量電荷比をもつことから、分子種の特定が可能となる。
- (注2)解糖系:
- グルコースをピルビン酸へと分解する一連の生化学反応。エネルギー産生に関わるとともに、その中間代謝産物はアミノ酸・核酸合成の前駆体として用いられる。解糖系は酸素の非存在下でも進行することから嫌気的呼吸とも呼ばれ、酸素非存在下ではピルビン酸は最終的に乳酸へと分解される。
- (注3)酸化的リン酸化:
- グルコース等の基質が解糖系やTCA回路で代謝される過程で抽出された電子の力を利用して、ミトコンドリアでエネルギー(ATP)を生成する過程。酸化的リン酸化は酸素を必要とすることから、好気的呼吸とも呼ばれる。
添付資料:
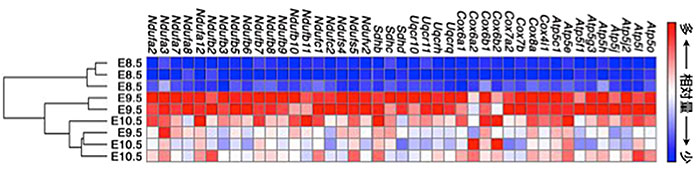
図1.ミトコンドリア電子伝達系遺伝子群の胎生8.5、9.5、10.5日胚の各ステージでの発現パターン。横軸に並んだミトコンドリア電子伝達系の各遺伝子のステージ間での相対的発現量の多寡を、赤青と濃淡で示している。胎生8.5日胚に比べ9.5日以降の胚では電子伝達系遺伝子群の発現上昇が見られる。縦の各列は各ステージの異なる胚を示す。階層的クラスタリングにより8.5日胚とそれ以降の胚が明確に区別されることがわかる。
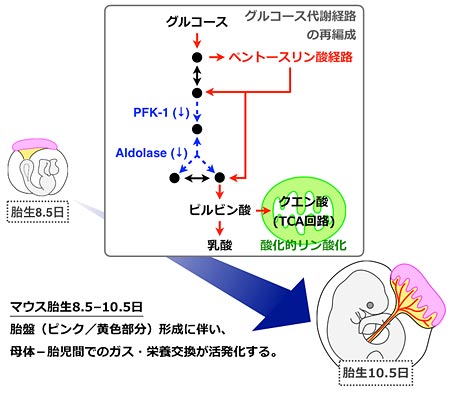
図2.マウス胎盤形成期の胚で生じるグルコース代謝経路の再編成。胎生8.5日から10.5日の間に、グルコース代謝経路のうちPFK-1とAldolaseの発現・酵素活性が減少すると共に、酸化的リン酸化が活性化する。にもかからわずグルコースからの乳酸の生成は増加しており、グルコースがペントースリン酸経路を経て代謝されることが示唆される。
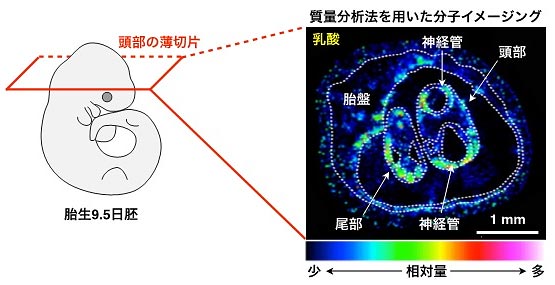
図3.質量分析法を用いた分子イメージングによる胚体内の代謝産物(乳酸)の可視化
胎生9.5日胚の組織切片(右図)で、乳酸は神経管の背側など一部の組織に多く分布することが明らかとなった。
掲載日 平成29年1月5日
最終更新日 平成29年1月5日


