アトピー性皮膚炎発症に関わる痒み物質の産生に重要なタンパク質を発見―新しい痒み治療薬の開発に期待―
プレスリリース
国立大学法人九州大学
国立研究開発法人日本医療研究開発機構
九州大学生体防御医学研究所の福井宣規主幹教授、大学院医学研究院の古江増隆教授、大学院4年生の山村和彦らの研究グループは、アトピー性皮膚炎における痒み惹起物質であるIL-31の産生に、EPAS1というタンパク質が重要な役割を演じることを世界に先駆けて発見し、その作用機序を解明しました。
アトピー性皮膚炎は国民の7~15%が罹患している国民病であり、「痒み」に伴い生活の質が著しく損なわれることから、その対策は急務となっています。IL-31は、アトピー性皮膚炎発症に重要な痒み物質で、主にヘルパーT細胞(※1)から産生されますが、その産生制御機構は不明でした。研究グループは、DOCK8という分子を欠損した患者さんが重篤なアトピー性皮膚炎を発症することに着目し、このタンパク質の機能を解析しました。その結果、DOCK8が発現できないように遺伝子操作したマウスでは、IL-31の産生が著しく亢進し、重篤な皮膚炎を自然発症することを見いだしました。さらにそのメカニズムを詳細に解析したところ、DOCK8の下流でEPAS1が作動し、IL-31産生を誘導していることを突き止めました。IL-31産生におけるEPAS1の重要性は、アトピー性皮膚炎患者さんにおいても確認できました。このためEPAS1は、アトピー性皮膚炎の痒みを根元から断つための新たな創薬標的になることが期待されます。
本研究成果は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業インキュベートタイプ(LEAP)および創薬基盤推進研究事業、厚生労働科学研究委託費の成果で、2017年1月9日(月)午前10時(英国時間)に英国科学雑誌「Nature Communications」に掲載されます。
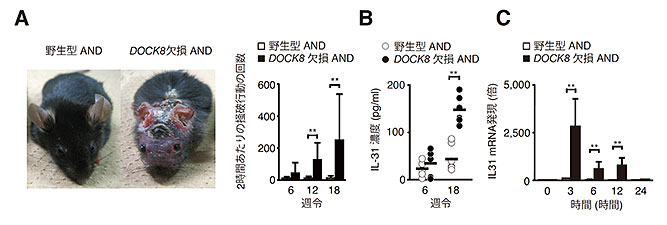 (図1)DOCK8欠損AND Tgマウスは血清IL-31の上昇を伴うアトピー様皮膚炎を自然発症する
(図1)DOCK8欠損AND Tgマウスは血清IL-31の上昇を伴うアトピー様皮膚炎を自然発症する
A:DOCK8欠損AND Tgマウス(写真右)は、掻破行動を伴う重篤な皮膚炎を自然発症する。
B:DOCK8欠損AND Tgマウスでは、血清IL-31が異常高値を示す。
C:DOCK8欠損AND TgマウスのヘルパーT細胞を抗原で刺激すると、大量のIL-31が産生される。
- 研究者からひとこと:
- アトピー性皮膚炎の病態を解明したいという私達の思いが、ようやく実を結びました。新しい治療薬の開発につながることを期待し、今後さらに研究を進めて参ります。
背景
内容
研究グループは、DOCK8という分子を欠損した患者さんが重篤なアトピー性皮膚炎を発症することに着目し、このタンパク質の機能解析に着手しました。このため、まず、DOCK8が発現できないように遺伝子操作したマウス(DOCK8欠損マウス)を、TCRトランスジェニック(以下Tg)マウス(※4)の一種であるANDというマウスと交配したところ、掻破行動を伴う重篤なアトピー様皮膚炎を自然発症し(図1A)、血中のIL-31が異常高値を示すことを見いだしました(図1B)。このマウスのヘルパーT細胞を抗原で刺激したところ、DOCK8を発現するマウス(野生型マウス)と比較して、IL-31の産生が顕著に亢進していました(図1C)。このことから、DOCK8がIL-31産生を抑制する機能をもつことが明らかになりました。
次に、IL-31の産生制御機構を明らかにするため、野生型マウスとDOCK8欠損マウスのヘルパーT細胞における遺伝子発現を詳細に調べたところ、EPAS1という遺伝子産物の発現が両者の間で異なっていることを見いだしました。DOCK8欠損マウスのヘルパーT細胞においてEPAS1の発現を抑制すると、IL-31の産生が著減しました(図2A)。さらに、ヘルパーT細胞においてEPAS1が発現できないように遺伝子操作したマウスを作製し、DOCK8欠損AND Tgマウスと交配したところ、アトピー様皮膚炎の発症が完全に阻止されました(図2B)。これまでに、EPAS1はARNTという分子と協調して低酸素応答を制御することが知られていましたが、EPAS1によるIL-31の産生誘導にARNTは必要ではなく、別のSP1という分子が関与していることがわかりました。一方、EPAS1は細胞質から核に移行して機能しますが、DOCK8はMST1という分子を介して、EPAS1の核への移行を抑制していることを突き止めました。以上より、DOCK8の下流でEPAS1が作動し、EPAS1がIL-31産生に重要な役割を演じることが明らかになりました。
そこで最後に、ヒトヘルパーT細胞におけるEPAS1の重要性につき検討を行いました。アトピー性皮膚炎患者さんの血清では、健常者に比べてIL-31の濃度が高値であり(図3A)、患者さんのヘルパーT細胞を刺激すると、大量のIL-31が産生されます(図3B)。しかしながら、このIL-31の産生は、EPAS1の発現を抑制することで、著減しました(図3C)。このことは、アトピー性皮膚炎患者さんのIL-31産生もEPAS1に依存していることを示しています。
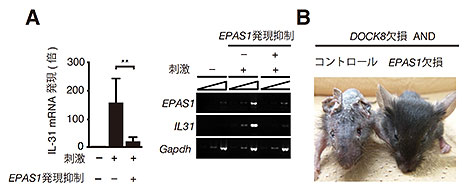 (図2)EPAS1はIL-31産生の鍵分子である
(図2)EPAS1はIL-31産生の鍵分子である
A:DOCK8欠損AND TgマウスのヘルパーT細胞においてEPAS1の発現を抑制すると、IL-31の産生が著減する。
B:ヘルパーT細胞においてEPAS1が発現できないように遺伝子操作したDOCK8欠損AND Tgマウス(写真右)では、アトピー様皮膚炎の発症が阻止される。
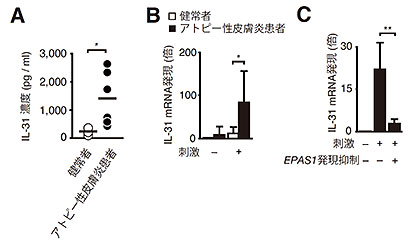 (図3)EPAS1は、アトピー性皮膚炎患者さんのIL-31産生にも重要である
(図3)EPAS1は、アトピー性皮膚炎患者さんのIL-31産生にも重要である
B:アトピー性皮膚炎患者さんのヘルパーT細胞は、刺激に伴い大量のIL-31を産生する。
C:アトピー性皮膚炎患者さんのヘルパーT細胞におけるIL-31の産生は、EPAS1に依存している。
今後の展開
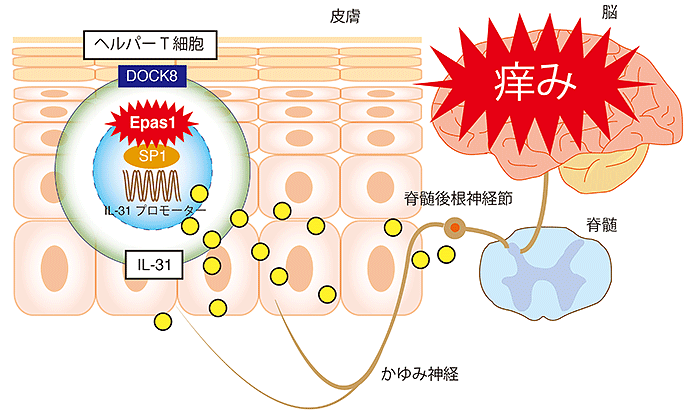 (図4)IL-31の産生と痒み発症メカニズムの模式図
(図4)IL-31の産生と痒み発症メカニズムの模式図
本研究について
用語解説
- (※1)ヘルパーT細胞:
- リンパ球の一種であり、CD4 T細胞とも呼ばれる。サイトカインという液性因子を分泌し、B細胞を刺激または補助して抗体の産生を促す機能を有する。
- (※2)ヒスタミン:
- マスト細胞等から放出される化学物質で、アレルギー反応において中心的役割を演じることが知られている。
- (※3)脊髄後根神経節:
- 感覚情報を伝える知覚神経路に位置する神経細胞の集団。
- (※4)TCRトランスジェニックマウス:
- T細胞表面に存在する抗原受容体(TCR)を遺伝子操作で強制発現したマウス。このマウスは特定の抗原を認識するT細胞の機能解析に適している。
論文名
- “The transcription factor EPAS1 links DOCK8 deficiency to atopic skin inflammation via IL31 induction”
- (転写因子Epas1はIL31産生を介してDOCK8欠損とアトピー性皮膚炎を関連づける)
雑誌名:Nature Communications
doi: 10.1038/NCOMMS13946
お問い合わせ
内容に関するお問い合わせ
国立大学法人九州大学
生体防御医学研究所 主幹教授 福井 宣規(ふくい よしのり)
TEL:092-642-6827 FAX:092-642-6829
Mail:fukui“AT”bioreg.kyushu-u.ac.jp
広報に関するお問い合わせ
国立大学法人九州大学
広報室
〒819-0395 福岡市西区元岡744
TEL:092-802-2130 FAX:092-802-2139
Mail:koho“AT”jimu.kyushu-u.ac.jp
AMED事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
革新的先端研究開発支援事業
戦略推進部 研究企画課
TEL:03-6870-2224
Mail:kenkyuk-ask“AT”amed.go.jp
創薬基盤推進研究事業
戦略推進部 医薬品研究課
TEL:03-6870-2219
Mail:souyakukiban“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成29年1月9日
最終更新日 平成29年1月9日


