筋萎縮性側索硬化症(ALS)に対するiPS細胞創薬に基づいた医師主導治験を開始
プレスリリース
慶應義塾大学医学部
慶應義塾大学病院
日本医療研究開発機構
慶應義塾大学病院神経内科診療科部長の中原仁教授、診療科副部長の高橋愼一准教授らは、慶應義塾大学医学部生理学教室の岡野栄之教授らとともに疾患特異的iPS細胞を用いた創薬技術を応用し新たに見出したALS治療薬の候補、ロピニロール塩酸塩(本治験薬)の安全性・有効性を評価するための第I/IIa相医師主導治験を開始しました。本治験は、有効な治療法に乏しいALS患者さんを対象に慶應義塾大学病院にて実施する予定です。
本治験薬は、これまでパーキンソン病の治療薬として1996年から世界中で広く使用されてきた薬です。日本における使用経験も数多く蓄積されており、1日1回の投薬で効果が持続するもの(徐放錠)もあります。本治験は患者さんに負担の少ない徐放錠を使用しています。
岡野教授のグループでは、神経疾患を持つ患者さん由来の組織からiPS細胞を樹立し(疾患特異的iPS細胞)、長年にわたり研究を進めてきました。ALSは、これまで適切な病態モデルがなく動物実験を介した研究が困難でしたが、岡野教授のグループは、患者さん由来のiPS細胞モデルを駆使した革新的なドラッグスクリーニングの手法を開発し、有望なALS治療薬の候補を同定しました。
本治験が、これまで有効な治療法に乏しかった重度の神経難病であるALS患者さんに大いなる福音となることが期待されます。
研究の背景と概要
ALSは「難病の患者に対する医療等に関する法律」において難病指定を受けている難治性神経疾患の一つで、脊髄運動ニューロン(注1)の障害による筋萎縮と筋力の低下を特徴とする進行性の病気です。歩行困難、言語障害、嚥下障害および呼吸障害などの症状があり、本人の意識や知覚が正常であるにも関わらず、生活やコミュニケーションの自由が阻害されるため、生活の質(QOL)は著しく低下します。また、経過には個人差があるものの、発症から死亡ないしは呼吸器装着までの期間は20~48か月であると報告されています(日本神経学会:筋萎縮性側索硬化症診療ガイドライン2013)。
ALSの病態としては、これまでの研究から、ALS 発症後に生じる細胞プロセス、すなわち、神経突起の短縮、ミトコンドリア機能障害、異常タンパク質凝集、酸化ストレスの亢進、神経興奮毒性、神経炎症、アポトーシス(神経細胞死)の亢進といった病態が推測されています。また、ALSの実験モデル(注2)として家族性ALSの原因遺伝子を導入した変異マウスなどが多く用いられてきましたが、実際のヒト脊髄における病態を十分に再現し得たモデルは未だ存在しません。
そこで、慶應義塾大学医学部生理学教室(岡野栄之教授)では、2016年にヒトiPS細胞(注3)を用いたヒト脊髄運動ニューロンの作製および革新的な治療薬探索の実験手法を開発しました。これを用いて、健常者由来およびALS患者さん由来の血液細胞から作ったiPS細胞を誘導して脊髄運動ニューロンを作製し、既に薬として使用されている1,232種類の化合物の中からALS病態の改善を狙ったドラッグスクリーニングを実施しました。その結果、脳内移行性や副作用を含む安全性などを考慮した上で、ロピニロール塩酸塩を最適なALS治療候補薬として同定しました。今回の実験では、家族性ALSの患者さん(一部の遺伝子異常を除く)のみならず、ALSの大多数を占める孤発性ALS患者さんのうち約70%にも効果がある可能性が示されました。
本治験は、ALS患者さんに対する当該薬剤の安全性と効果を確認する目的で実施され、今後、有効な治療法に乏しかったALS患者さんへの適用が期待されます。また、本治験は世界初のALSの患者さんに対するiPS細胞創薬の成功事例になる可能性を秘めています(図1)。
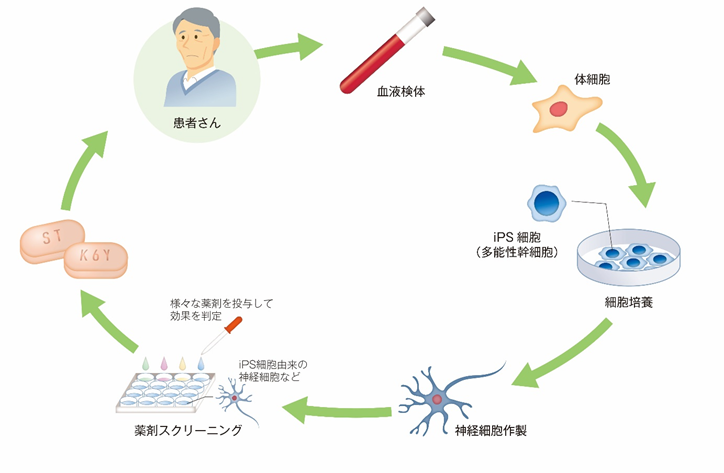
図1.iPS細胞創薬
治験薬の概要
治験薬であるロピニロール塩酸塩は、英国グラクソ・スミスクライン社でドパミンの構造をもとに創製・開発されたドパミン受容体作動薬(注4)です。パーキンソン病に対する治療薬として、1996年に英国において承認されたのをはじめ、現在、日本を含む多くの国で承認されています。
ロピニロール塩酸塩は、2型ドパミン受容体刺激のみならず、動物モデルにおける、①抗酸化作用、②神経栄養因子産生促進作用、③神経幹細胞の増殖促進作用といった神経保護効果が示されています。
今回、患者さんのiPS細胞由来運動ニューロンモデルに対してロピニロール塩酸塩を作用させたところ、神経突起の短縮、アポトーシスの増加、ミトコンドリア機能障害、異常タンパク質凝集、酸化ストレスの亢進、といったALS病態が改善し、さらにはALSの原因である運動ニューロンの神経細胞死を抑制することがわかりました(図2)。
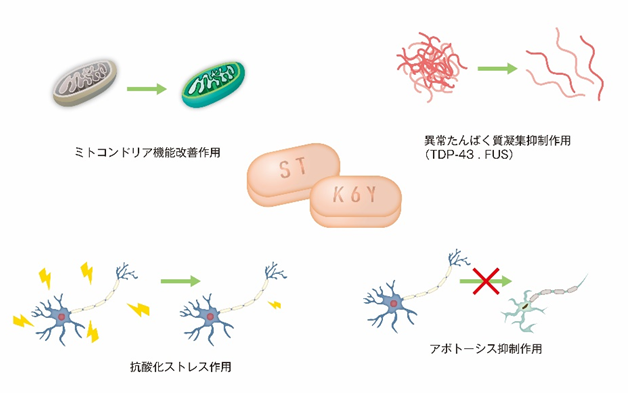
図2.ALSに対するロピニロール塩酸塩の期待される作用
治験の対象と概要
本治験では、①ALSの診断基準(世界神経学会El Escorial改訂)の「ALS可能性高し検査陽性」、「ALS可能性高し」または「ALS確実」に該当し、発症後60か月以内の方、②ALSの重症度分類が1(家事・就労がおおむね可能)または2(日常生活がおおむね自立)の方、③年齢が20歳から80歳の方、④身体機能の評価尺度であるALSFRS-Rの全項目が2点以上の方、⑤%FVC(呼吸機能)が70%以上の方(呼吸機能が保たれている方)、⑥治験期間中、慶應義塾大学病院外来通院(一部入院)が可能な方を対象とします(全ての条件を満たす事が必須)。
ただし、①治験への登録30日以内に他の治験または介入を伴う臨床研究に参加した方、②家族性ALSの原因遺伝子であるSOD-1変異の家族歴をもっている方(またはSOD-1 変異を過去に診断されたことのある方)、③がんを合併している方(またはがんの治癒後5年以上経過していない方)は、本治験にはご参加いただけません(いずれに該当した場合も不可)。
全体のスケジュールとして、投与前3か月間の症状観察期間、6か月間の二重盲検期(実際のロピニロール塩酸塩を服用される方が15名、プラセボ(注5)を服用される方が5名)、その後治験の継続を希望される方には、本治験が終了するまでの期間に応じて、4週間から約22週間程度、継続投与期としてロピニロール塩酸塩を服用していただくことができます。なお、本治験の終了間近で4週間以上の投与ができない場合は、継続投与期の実施はできません。
投与開始時と終了時に1週間程度の入院が必要で、服用開始後は最大8週間まで毎週外来通院を行う必要があります。その後は1か月ごとの通院となります。
初回投与から観察期間終了時までの安全性(副作用の有無)および忍容性(決められた量を服用し続けられるか)を本治験の主要評価項目とします(図3)。
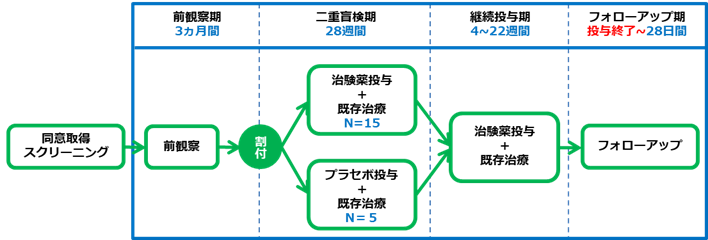
図3.治験スケジュール概要
留意事項
- 今回の治験は、世界で初めてロピニロール塩酸塩をALS患者さんに使用する臨床試験です。
- ALS患者さんに対するロピニロール塩酸塩の有効性や安全性は、まだ確認されていません。
- ロピニロール塩酸塩は、今回の治験、および今後の追加治験の動向を踏まえ、薬事承認を得ることが出来ましたら、ALS患者さんにご使用頂けることになります。
- したがって、現時点では、一般診療においてロピニロール塩酸塩をALS患者さんに対して治療目的で使用することは避けてください。
特記事項
本治験実施までに行った研究は、国立研究開発法人日本医療研究開発機構(AMED)再生医療実現拠点ネットワークプログラム「神経疾患特異的iPS細胞を活用した病態解明と新規治療法の創出を目指した研究」および橋渡し研究加速ネットワークプログラム、橋渡し研究支援拠点(慶應義塾大学)の支援によって行われました。
また、本治験の実施においては、AMED難治性疾患実用化研究事業「iPS細胞創薬に基づいた新規筋萎縮性側索硬化症(ALS)治療薬であるロピニロール塩酸塩の実用化第1/2a相試験」、株式会社ケイファーマからの資金支援、ならびにグラクソ・スミスクライン株式会社から治験薬の提供を受け、慶應義塾大学病院で実施します。
本研究内容と関連する特許として「筋萎縮性側索硬化症治療剤及び治療用組成物」がすでに特許出願されています。
用語解説
- (注1)脊髄運動ニューロン:
- 身体の筋肉を動かすための神経細胞
- (注2)実験モデル:
- 薬の効果を確認するために、ヒトと同じ病気にさせた動物や細胞
- (注3)iPS細胞(induced pluripotent stem cell):
- 身体のどんな細胞にも変化できる力を持つ細胞
- (注4)ドパミン受容体作動薬:
- ドパミンの形に似た薬で、体内に入ることにより、ドパミンと同じ作用を示す
- (注5)プラセボ:
- ロピニロール塩酸塩の錠剤と見た目の区別はつかないが、ロピニロール塩酸塩の有効成分が含まれていないもの
お問い合わせ先
本発表資料のお問い合わせ先/治験に関するお問い合わせ先
慶應義塾大学病院 神経内科 診療科部長
教授 中原 仁(なかはら じん)
慶應義塾大学病院 神経内科 診療科副部長
准教授 高橋 愼一(たかはし しんいち)
TEL:03-5363-3788 FAX:03-3353-1272
E-mail:nakahara”AT”a6.keio.jp
takashin”AT”tka.att.ne.jp
研究に関するお問い合わせ先
慶應義塾大学医学部生理学教室
教授 岡野 栄之(おかの ひでゆき)
TEL:03-5363-3747 FAX:03-3357-5445
E-mail : hidokano”AT”a2.keio.jp
本リリースの発信元
慶應義塾大学
信濃町キャンパス総務課:鈴木・山崎
〒160-8582 東京都新宿区信濃町35
TEL:03-5363-3611 FAX:03-5363-3612
E-mail:med-koho”AT”adst.keio.ac.jp
K Pharmaの事業に関するお問い合わせ先
株式会社ケイファーマ(K Pharma, Inc.)
〒102-0075 東京都港区六本木7-7-7
Tri-Seven Roppongi 8F
代表取締役社長 福島 弘明
TEL:03-6629-3380
E-mail:komei.fukushima”AT”kpharma.co.jp
AMEDの事業に関するお問い合わせ先
国立研究開発法人 日本医療研究開発機構(AMED)
〒100-0004 東京都千代田区大手町1-7-1
読売新聞ビル
戦略推進部 難病研究課
TEL:03-6870-2223
E-mail: nambyo-info”AT”amed.go.jp
戦略推進部 再生医療研究課
TEL:03-6870-2220
E-mail:saisei”AT”amed.go.jp
※E-mailは上記アドレス”AT”の部分を@に変えてください。
掲載日 平成30年12月3日
最終更新日 平成30年12月3日


