白血病の発症に関わる新たな分子機構を発見―血液を正常に作るための巧妙なしくみ―
プレスリリース
大阪大学
日本医療研究開発機構(AMED)
研究成果のポイント
- 造血幹細胞や造血前駆細胞※1の増殖を適切に調整する分子としてRegnase-1を同定し、その発現の異常が白血病の発症に繋がることを発見した。
- Regnase-1は造血幹細胞の制御に必要な転写因子※2のmRNAを分解することで、造血幹細胞の転写ネットワークを制御していることが解った。
- 白血病の発症に関わる新たな分子機構が解明されたことで、Regnase-1などを標的とした新概念に基づく白血病治療薬や再発抑制薬の開発が期待される。
概要
大阪大学微生物病研究所の木戸屋浩康助教、高倉伸幸教授(免疫学フロンティア研究センター兼任)らの研究グループは、リボヌクレアーゼ※3であるRegnase-1が造血幹細胞および造血前駆細胞の自己複製 ※4を制御していることを明らかにしました。また、Regnase-1遺伝子を欠失させたマウスでは急性骨髄性白血病と類似した症状を示すことを発見し、Regnase-1が白血病の発症に関与していることを明らかにしました。
生体内に血液細胞を供給し続けるためには、血液の幹細胞である造血幹細胞や造血前駆細胞の増殖や分化を適切に制御する必要があります。この制御が異常になると、血液細胞が過剰に増殖するなど、白血病の発症へと繋がります。
日本における白血病の発生率は年々増加傾向にあり、年間約8,500名が死亡しています(2017年、国立がん研究センターによる調査)。小児から高齢者まで幅広い年齢層で発生しますが、特に若年層にて発生頻度が高いことから、治療法の確立が社会的に求められています。
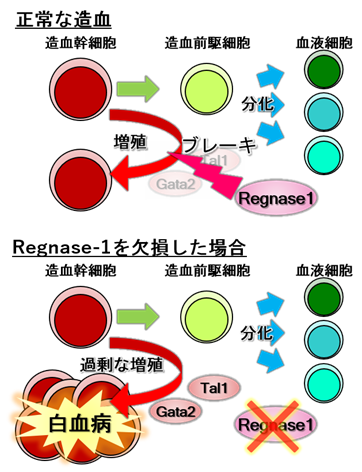
これまで、造血幹細胞制御や白血病発症に関わる分子群が同定されていましたが、本研究ではこれまで考えられてこなかったリボヌクレアーゼであるRegnase-1を新たに同定しました。これにより、Regnase-1などのリボヌクレアーゼを標的とした新概念に基づく白血病治療薬や再発抑制薬の開発が期待されます(図1)。
研究の背景と成果
私たちの体の中では白血球、赤血球、血小板といった血液細胞が常に作り出されていますが、これらは血液の幹細胞である「造血幹細胞」が増殖・分化することで維持されています。血液のがんである白血病は、何らかの原因で造血幹細胞や造血前駆細胞が正常に増殖・分化することができず、異常な細胞が増加してしまうことで起こる病気です。このような異常が起きないように、造血幹細胞は様々な分子によって緻密に増殖と分化のバランスが制御されているわけですが、本研究で新たにその機能が発見されたRegnase-1も造血幹細胞の異常な増殖に対するブレーキとして働く分子です。
今回の発見の特徴的な点は、Regnase-1のユニークな機能にあります。Regnase-1は標的とする特定のRNAを分解する働きを持つ分子であり、遺伝子の発現量を制御する役割を持つことが報告されていました。本研究ではRegnase-1遺伝子を欠失した造血幹細胞が過剰に増殖し続けてしてしまい(図2)、白血病を発症してしまうことをマウスモデルにて明らかにしました(図3)。これまで、造血幹細胞制御や白血病発症に関わる遺伝子として、エピジェネティック制御※5やシグナル伝達制御分子などが見つかっていましたが、今回初めてRNAを分解する分子(リボヌクレアーゼ)も関与していることが明らかになりました。
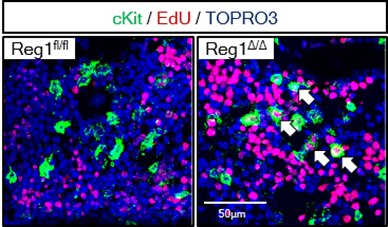
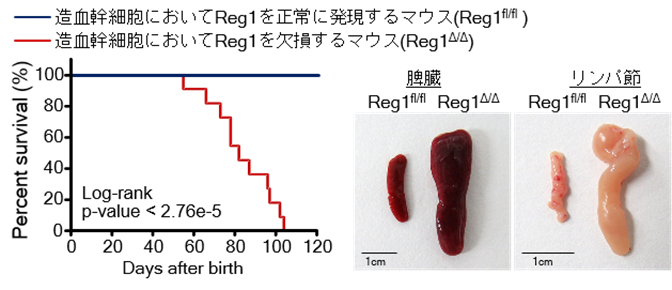
造血幹細胞の増殖や分化の制御は生命活動の維持に重要であり、異常が起きないように点検機構が働いているため、単一の遺伝子異常が起きても白血病が発症することは稀です。しかしながら、Regnase-1遺伝子を欠失したマウスはわずか3ヶ月ほどで重篤な造血異常によって死亡してしまいます。その原因を調べるため、Regnase-1の機能を解析したところ、Regnase-1がGata2やTal1※6といった造血幹細胞の制御に重要な転写因子のmRNAを分解することで、造血幹細胞の増殖を制御する転写ネットワークを制御していることが明らかとなりました。そのため、Regnase-1のみの欠失でも広範囲の遺伝子発現の変化が誘導されてしまい、白血病の発症が誘導されてしまうと考えられます。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果により、白血病の発症にリボヌクレアーゼであるRegnase-1の異常が関与している可能性が示されました。白血病は若年層に多く発症するがんであり、同世代のがんの約4分の1とも言われています。治療法の発展によって寛解できるようになりつつありますが、患者さんの多くは再発の恐怖に悩まされており、完全寛解を可能とする治療法の開発が望まれています。今回、白血病の原因となる分子機構が新たに同定されたことで、Regnase-1などを標的とした新概念に基づく白血病治療薬や再発抑制薬の開発が期待されます。
特記事項
本研究成果により、白血病の発症にリボヌクレアーゼであるRegnase-1の異常が関与している可能性が示されました。白血病は若年層に多く発症するがんであり、同世代のがんの約4分の1とも言われています。治療法の発展によって寛解できるようになりつつありますが、患者さんの多くは再発の恐怖に悩まされており、完全寛解を可能とする治療法の開発が望まれています。今回、白血病の原因となる分子機構が新たに同定されたことで、Regnase-1などを標的とした新概念に基づく白血病治療薬や再発抑制薬の開発が期待されます。
特記事項
本研究成果は、2019年3月6日(水)19時(日本時間)に英国科学誌「Nature Communications」(オンライン)に掲載されます。
- タイトル
- “Regnase-1-mediated post-transcriptional regulation is essential for hematopoietic stem and progenitor cell homeostasis”
- 著者
- Hiroyasu Kidoya1*, Fumitaka Muramatsu1, Teppei Shimamura2, Weizhen Jia1, Takashi Satoh3, Yumiko Hayashi1, Hisamichi Naito1, Yuya Kunisaki4, Fumio Arai4, Masahide Seki5, Yutaka Suzuki5, Tsuyoshi Osawa6, Shizuo Akira3, Nobuyuki Takakura1*. (*責任著者)
- 所属
-
- 大阪大学 微生物病研究所情 報伝達分野
- 名古屋大学大学院 医学系研究科 システム生物学分野
- 大阪大学 免疫学フロンティア研究センター 自然免疫学
- 九州大学 大学院医学研究院 幹細胞再生修復医学分野
- 東京大学大学院 新領域創成科学研究科 メディカル情報生命専攻 生命システム観測分野
- 東京大学 先端科学技術研究センター ニュートリオミクス・腫瘍学分野
なお、本研究は、国立研究開発法人日本医療研究開発機構(AMED)の次世代がん医療創生研究事業における研究開発課題「白血病細胞-骨髄腫瘍血管を巡る負のスパイラルを断ち切る治療標的の同定」(研究開発代表者:木戸屋浩康)、老化メカニズムの解明・制御プロジェクト「個体・臓器老化研究拠点」(研究代表者:片桐秀樹)の研究課題「血管老化の分子機構の解明とその制御(研究分担者:高倉伸幸)」の一環として行われ、また、日本学術振興会科学研究助成KAKENHI(16H06147、18K19475、15K14380)を受け、名古屋大学大学院 医学系研究科 島村徹平准教授の協力を得て行われました。
研究者のコメント
白血病は化学療法や骨髄移植によって治療可能になったと一般的に認知されていますが、再発の抑制や、再発した場合の治療法の開発は課題として残されています。若くして罹患してしまった子供達や、その親族の気持ちを考えると「高確率で治療できる」でよいとは決して言えません。本研究の成果が、白血病の根治に繋がることを心より願うと共に、さらなる研究に邁進したいと考えています。
用語説明
- ※1 造血幹細胞・造血前駆細胞
- 主に骨髄に存在し、白血球、赤血球、血小板などの血液細胞を生みだす血液の幹細胞を造血幹細胞と呼び、造血幹細胞から血液細胞への分化の途中段階にある未熟な細胞を造血前駆細胞と呼ぶ。造血幹細胞は全ての血液細胞に分化する能力を有しているが、造血前駆細胞が分化可能な細胞は限られている。
- ※2 転写因子
- DNAに書き込まれた遺伝子の情報に基づいたRNAの合成(転写)を制御するはたらきをもつタンパク質。DNA上のプロモーターやエンハンサーといった領域に特異的に結合する。
- ※3 リボヌクレアーゼ
- リボ核酸(RNA)のリン酸ジエステル結合を加水分解によって切断する酵素。
- ※4 自己複製
- 細胞が分裂することによって自身の複製をつくり出すこと。幹細胞は、細胞分裂により1つ,もしくは2つの母幹細胞と同じ能力をもった娘幹細胞を生み出す。
- ※5 エピジェネティック制御
- 遺伝子配列の変化を伴わない遺伝子発現の制御。DNAの塩基やDNAが巻き付くタンパク質(ヒストン)がメチル化、アセチル化などの化学修飾が遺伝子の発現や複製などに関係することが示されている。
- ※6 Gata2・Tal1
- ともに造血細胞の制御に重要な遺伝子の発現を制御する転写因子。これらの分子の変異や制御機構の破綻は白血病と深く関与していることが知られている。
本件に関する問い合わせ先
研究に関するお問い合わせ
大阪大学 微生物病研究所 情報伝達分野
教授 高倉 伸幸(たかくら のぶゆき)
助教 木戸屋 浩康(きどや ひろやす)
TEL:06-6105-6053 FAX:06-6879-8314
E-mail:kidoya"AT"biken.osaka-u.ac.jp
ホームページ:http://st.biken.osaka-u.ac.jp/
AMED事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 がん研究課
〒100-0004 東京都千代田区大手町1‐7-1
TEL:03-6870-2221
E-mail:cancer"AT"amed.go.jp
基盤研究事業部 研究企画課
TEL:03-6870-2224 FAX:03-6870-2246
E-mail:kenkyuk-ask"AT"amed.go.jp
※E-mailは上記アドレス"AT"の部分を@に変えてください。
掲載日 平成31年3月6日
最終更新日 平成31年3月6日


