先天性尿素サイクル異常症でヒトES細胞を用いた治験を実施―ヒトES細胞由来の肝細胞のヒトへの移植は、世界初!―
プレスリリース
国立成育医療研究センター
日本医療研究開発機構
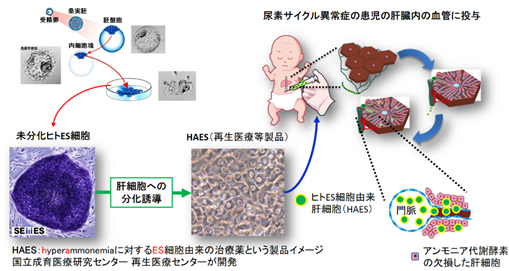
国立成育医療研究センター(所在地:東京都世田谷区大蔵、理事長:五十嵐隆)臓器移植センターの笠原群生センター長、福田晃也診療部長、 阪本靖介副センター長、堀川玲子内分泌代謝科部長、研究所の再生医療センター梅澤明弘センター長らのグループは、2019年10月21日より「先天性尿素サイクル異常症に対するHAES移植治療の医師主導治験―新生児期発症型患者を対象とした探索的試験―」という医師主導治験を行いました。本医師主導治験の患者は、有毒なアンモニアを体内で分解できない尿素サイクル異常症を患った生後6日の新生児です。国立成育医療研究センター1)で作製したヒト胚性幹細胞(ヒトES細胞2))由来の肝細胞(HAES)を使い、患者が根治療法として肝移植を行える生後3~5カ月(体重約6キログラム)に成長するまでの「橋渡しの治療」として、HAES を肝臓の血管内に注射する肝細胞移植(図1)を行いました。今回、HAES移植をヒトに対して行った臨床試験として世界で初めて成功し、次の治療である肝移植も無事に終えることができました。これは、HAESの移植により、患者の血中アンモニア濃度の上昇が抑えることができたためと考えます。
これまでの肝細胞移植治療では、肝細胞の安定供給が得られないことが最大の課題でしたが、ヒトES細胞から肝細胞を安定して作製することができるようになり、その安全性と有効性を検証する今回の医師主導治験=「橋渡しの治療」が成功したことで、今後は肝移植まで辿り着けなかった小さな命をより安全に肝移植までつなげられることが期待されます。
プレスリリースのポイント
- ヒトES細胞を使い、ヒトを対象にした治験は日本初。また、ヒトES細胞由来の肝細胞を、肝疾患の治療に用いた治験としては世界初です。
- 本医師主導治験において、ヒトES細胞から作成した肝細胞をヒトに移植する安全性および、有効性を検証することができました。(手術手技に伴う合併症もありませんでした。)
- 本医師主導治験において、世界1例目の被験者に肝細胞移植を完了。これまで肝移植までたどりつけなかった患者さんを、より安全に肝移植までつなぐことができました。
- 今回の治療方法は、先天性の尿素サイクル異常症の患者および家族にとって、根治療法となる肝移植までの待機期間中に、高アンモニア血症発作を回避するための従来の治療法に上乗せ効果のあるものとして期待されます。また将来的な遺伝子治療にも貢献できる可能性があります。
背景・目的
新生児に対する肝移植は、技術的に困難であるばかりでなく、移植された肝臓が患者の腹腔内容積に対して相対的に過大となることから、呼吸不全や肝臓の圧迫による血流障害などの生命に関わる重篤な合併症を起こすことが多くあります。そのため、通常は、安全に移植することが可能な体重6キログラムまで患者が成長するのを待って肝移植を行います。
今回の医師主導治験の対象疾患である「尿素サイクル異常症3~6)」は、先天性疾患で出生後まもなく発症することから蛋白摂取制限、薬物療法、血液濾過透析による治療を行いながら7)、肝移植ができる体格(体重6キログラム)に成長するまで3~5か月間は待機しなければなりません8)。脳死肝移植ドナーから摘出した肝臓から分離・凍結保存した肝細胞を利用することができる欧米では、この待機期間をより安全にするために、発症直後の新生児期に肝細胞移植をすることによって、血中アンモニア濃度の上昇を抑える治療が行われてきました。しかし、脳死肝移植ドナーからの肝細胞を利用できない日本では、肝細胞移植の細胞供給源(セルソース)として、安定した品質の肝細胞を安定供給することが、この病気の最大の課題となっていました。
そこで当センターは、新たなセルソースとしてほぼ無限に増殖させることができる、多能性幹細胞であるヒトES細胞由来の肝細胞に注目しました。ヒトES細胞を、肝細胞に分化誘導した状態で凍結保存しておくことで、緊急の移植にも対応できます。当センターは、国内に2つしかないヒトES細胞樹立機関として認められており、ヒトES細胞を使って、新生児をより安全に肝移植までつなぐことができる新たな治療法の確立を目指しました。
患者の症状と本医師主導治験の概要・成果について
(生後2日目) 高アンモニア血症発病
今回の医師主導治験の患者は、出生時、出生後24時間は特に問題無く経過していたが、生後2日目に、多呼吸、筋緊張亢進、けいれんなどの症状が出現。血液検査で 2,026 µg/dl(正常値66µg/dl以下)と著明な高アンモニア血症が認められ、尿素サイクル異常症の疑いで当センターに搬送、持続的血液ろ過透析、薬物療法などの集中治療を開始。その後、生化学的、遺伝子学的検査にて重症の尿素サイクル異常症(シトルリン血症Ⅰ型)と確定診断。
(生後6日目) HAES肝細胞移植術実施
患者家族によるHAES肝細胞移植に関する同意と、効果安全性評価委員会による被験者候補の適格性、医師主導治験実施の承認を得た後に、門脈圧・門脈血流などをモニタリングしながら1億9千万個のHAES肝細胞を2日間に分けて投与。肝細胞移植の手技による合併症・有害事象なく投与を完了。
(肝細胞移植後9日目)
患者の全身状態は良好で、ICUを退出して一般病棟管理へ移行。
(肝細胞移植後9週経過後)
蛋白摂取量の漸増はあったが血中アンモニア濃度の上昇はなく、体重約5キログラムまでの増加が得られたため退院。
(肝細胞移植後3か月経過後)
定期外来受診時の血液検査で、アンモニア値を含め特記すべき異常なく経過。
(肝細胞移植後5か月経過後) 生体肝移植術実施
父親をドナーとする生体肝移植術を実施。拒絶反応に対して免疫抑制療法を強化後は軽快し、その後、合併症を起こすことなく経過。
(生体肝移植後2か月) 軽快退院
退院時生後6か月
本医師主導治験の選択基準・除外基準
選択基準である、新生児期発症型の先天性尿素サイクル異常症の患児であり、低体重(6キログラム以下)、肝移植を安全に実施できると判断された時点で肝移植を行うことが予定されていること。かつ、除外基準である、B型肝炎ウイルス、C型肝炎ウイルス、AIDSウイルスへの感染、心疾患、肺疾患、神経疾患、悪性腫瘍等の疾患が否定されていること。
今後の展望・発表者のコメント
- 今回の医師主導治験の成功により、肝疾患の患者に対するヒトES細胞を用いた世界初の臨床試験における安全性が示されました。本医師主導治験をモデルケースとして、肝疾患に関する再生医療等製品の開発につながっていくことが期待されます。
- 今後も症例を重ね、引き続き安全性、有効性の検証を行っていきます9)。
- 日本において、各臓器・疾患に対するヒトES細胞由来製品における利点を生かして治療応用を進めて行くことにより、より多くの難病に対する治療法の確立、また治療成績の向上が期待されます。
特記事項
本研究開発は、国立研究開発法人日本医療研究開発機構(AMED)再生医療実現拠点ネットワークプログラム及び再生医療実用化研究事業の一環として行われました。
参考資料
- 1)国立成育医療研究センター 研究所について
- 国立成育医療研究センター 研究所(所在地:東京都世田谷区大蔵、研究所長:松原洋一)は、日本で2施設しかないヒトES細胞樹立機関のうちの1つで、日本におけるヒトES細胞研究の拠点としての役割を担っています。国立成育医療研究センターでは、現在までに、7株のヒトES細胞(SEES1-7)を樹立してきました。再生医療センター長の梅澤明弘を中心として、ヒトES細胞を用いた尿素サイクル異常症患者の肝細胞移植治療のための、HAES(ヒトES細胞由来肝細胞様細胞)を開発しています(図3、図4)。日本で唯一、医薬品医療機器等法に則ったヒトES細胞からの再生医療等製品の医師主導治験を進めています。
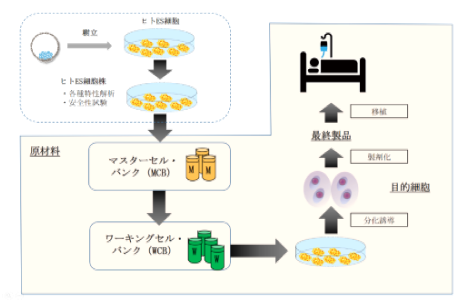
【図3 HAES(ヒトES細胞由来再生医療等製品)ができるまで】 
【図4 液体窒素の容器に凍結保存されたHAES(ヒトES細胞由来再生医療等製品)】 - 2)ヒトES細胞とは
- ヒトES細胞とは「Embryonic Stem Cell」の略で、日本語で「胚性幹細胞」、つまり胚の内部細胞塊を用いて作られた幹細胞です。ヒトES細胞は発生初期のヒトの受精胚の細胞から作られるため、受精卵と同じように、私たちのからだを構成するあらゆる細胞へと変わる能力(多分化能)を持っています。ヒトES細胞は、適切な培養環境で維持すれば、半永久的に増殖能・多分化能を維持することができると言われています。多分化能を維持する培養環境から、神経や血液などに分化する培養環境へ移すと、その環境に応じてさまざまな細胞に分化していくことも分かっています。
- 3)先天性尿素サイクル異常症とは
- 「尿素サイクル」は主に肝臓において、生体内で発生する有毒なアンモニア(NH3)を無毒な尿素に変える経路(図5)です。尿素サイクル異常症は尿素合成経路の代謝系に先天的な異常があり、高アンモニア血症の症状などで発症する一群の疾患です。
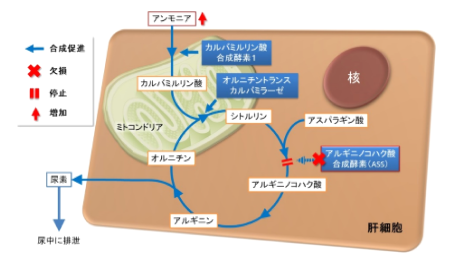
【図5 尿素サイクル異常症(シトルリン血症Ⅰ型)の酵素欠損部位】 - 4)先天性尿素サイクル異常症の原因
- 遺伝性の疾患のため、家族に尿素サイクル異常症の患者がいる場合は、尿素サイクル異常症を発症する確率は高くなります。尿素サイクルの代謝に関わる酵素の欠損症は複数あり、N-アセチルグルタミン酸合成酵素欠損症、カルバミルリン酸合成酵素欠損症、シトルリン血症Ⅰ型、アルギニノコハク酸尿症、アルギニン血症は、遺伝形式が「常染色体劣性(潜性)遺伝」で、オルニチントランスカルバミラーゼ欠損症は「X連鎖性遺伝」です。常染色体劣性(潜性)遺伝の場合、ご両親は保因者となり、その子どもは4分の1の確率で発症します。保因者の方は、症状など全く問題がなく、治療も必要ありません。しかし、突然変異による発症は、少なからず見られます。
- 5)先天性尿素サイクル異常症の症状
- 嘔吐、哺乳力低下、多呼吸、けいれん、意識障害、行動異常、発達障害などが見られ、時には命にかかわる重篤な状態になることもあります。
- 6)先天性尿素サイクル異常症の患者数
- 尿素サイクル異常症の発症頻度は8,000~44,000人に1人程度と推定されています。
【表1 日本における疾患別の患者発症頻度および推定患者数】
疾患名 頻度 国内推定患者数 カルバミルリン酸合成酵素欠損症 80万人に1人 約100人 オルニチントランスカルバミラーゼ欠損症 8万人に1人 約500人 シトルリン血症I型 53万人に1人 100人未満 アルギニノコハク酸尿症 7万人に1人 約100人 アルギニン血症 220万人に1人 100人未満 - 7)先天性尿素サイクル異常症の治療法
- 食事療法と薬物・アミノ酸療法が基本です。急性期には点滴、中心静脈栄養、血液透析を行うこともあります。食事療法はタンパク質の摂取量を制限しますが、栄養障害を起こさないように適切に行います。薬物としては、アンモニアを体外に排泄させる薬として安息香酸ナトリウムとフェニル酪酸ナトリウムがあります。アミノ酸療法はアルギニンとシトルリンがあり、尿素サイクル異常症の中で、アルギニンとシトルリンが不足する疾患に対して使用します。高アンモニア血症の発作がコントロール不良な例に対しては、肝移植が根治療法となります。
- 8)先天性尿素サイクル異常症で、新生児期に肝移植が困難で、肝細胞移植が必要な理由
- 可及的早期に肝移植をすることが望ましいとされていますが、新生児に対する肝移植に関しては、死亡につながる重篤な術後合併症を引き起こすリスクが高いため、体重6キログラム前後になって比較的安全に肝移植が可能になるまで待たなければなりません。しかし、6キログラムまでの体重増加を待つ3~5か月の間に、先に述べた治療を行っていても、発作的に重篤アンモニア血症が引き起こされることがあり、アンモニア値が高くなるほど、また発作回数が多いほど、脳に重篤な障害がでて、死亡する場合も少なくありません。最終的に肝移植ができたとしても、脳へのダメージは不可逆的であるため、肝移植が安全にできるまでの“橋渡し的治療”が必要とされてきました。肝細胞移植であれば、生後まもない新生児にも安全に行うことができる治療として従来の治療に上乗せ効果が期待されてきました(図6)。
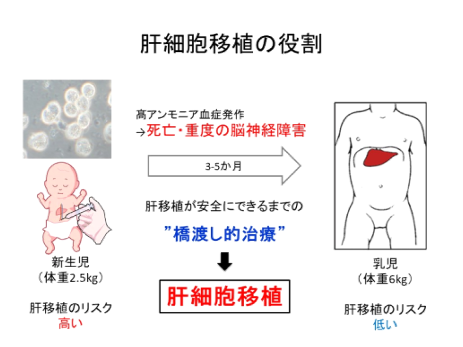
【図6 肝細胞移植の役割:肝移植が安全にできるまでの“橋渡し的治療”の必要性】 - 9)本医師主導治験の安全性について
- 本医師主導治験では、安全性を評価することも大きな目的の1つです。投与された肝細胞はすべて肝内の門脈内、あるいはその先の類洞内(肝細胞が並んでいる領域)に定着し、全身に広がることはありません。臓器移植としての肝移植の際に自己肝を全摘出することにより、投与したHAES(ヒトES細胞由来再生医療等製品)はすべて回収されるため、肝臓以外の細胞移植治療にはない、より客観的な安全性の評価ができます。
患者ご家族のコメント
初めに、我が子が今回の治療を受けることができ無事に元気よく退院できたことに対し、心より感謝申し上げます。先生方、看護師の皆さま、病院スタッフの皆さま、研究者の皆さま、関わってくださった全ての皆さま、ありがとうございます。
私たちの体験をお話します。私たちは、我が子が無事に生まれた感動から間もなく突然その症状はおき、絶望に襲われました。我が子がこちらの成育医療研究センターに運ばれ、何万人に一人の難病であることが分かりました。先生方の懸命な治療のおかげで、なんとか一命はとりとめました。しかし、命にかかわる発作は、今後いつまた襲いかかるか分からない状態であるということを知らされました。
その中で、希望の光が今回の治療でした。先生からは「この治療は、世界で初めての治療です。」と言われました。私たちは「なぜ我が子がそんな大変なことをしなければならないのか」と悩みました。悩んだ結果、命を救ってくれた先生がおっしゃるのだから大丈夫だと決断し、信頼してここまで進んできました。
治療の途中も、悩み不安になることがあり、簡単な道のりではありませんでした。そのような私たちだからこそ、これから先、同じ難病に悩むご家族がいたら、この体験を伝え、相談にのり、生きる勇気になりたいと強く思います。
これから先は、救っていただいた我が子の成長を楽しみに見守りたいと思います。
今回の治療のために長い年月をかけ研究し、最先端の医療の提供に関わって下さった全ての皆さまに感謝申し上げます。ありがとうございました。
お問い合わせ先
国立研究開発法人国立成育医療研究センター
企画戦略局 広報企画室 村上・近藤
TEL:03-3416-0181(代表)
E-mail:koho"AT"ncchd.go.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
再生・細胞医療・遺伝子治療事業部 再生医療研究開発課
TEL:03-6870-2220
E-mail:saisei"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和2年5月21日
最終更新日 令和2年5月21日


