損傷した筋肉が筋幹細胞を活性化させることを発見―筋疾患の病態解明や創薬開発に期待―
プレスリリース
熊本大学
日本医療研究開発機構
ポイント
- 肉離れ等で損傷した筋肉を再生するためには、筋幹細胞の活性化、増殖、筋分化という3つのステップが必要です。しかし、最初のステップである筋幹細胞の活性化のメカニズムについては、ほとんどわかっていませんでした。
- 本研究グループは、損傷した筋肉から漏出する成分が筋幹細胞を活性化させるといった、極めて合理的な組織再生の仕組みがあることを発見しました。
- 本研究では、損傷した筋肉から漏出する成分を「損傷筋線維由来因子(DMDFs)」と命名しました。今後、さまざまなDMDFsの多様な機能を解明することで、筋疾患の病態解明や創薬開発への展開が期待されます。
概要
私たちは激しい運動等で筋肉が損傷しても再生する力を備えています。この再生には筋線維の周囲に存在するサテライト細胞*1と呼ばれる筋幹細胞が欠かせません。サテライト細胞は通常眠った状態(休止期)で存在していますが、筋がダメージを受けて損傷すると速やかに、目覚め(活性化)、増殖を繰り返し、筋分化することで、損傷した筋線維を再生します。つまり、筋線維が損傷して再生するまでには、サテライト細胞の活性化、増殖、筋分化という3つのステップが必要になります。しかし、最初のステップである活性化はどのように起こるのか、そのメカニズムについてはよくわかっていませんでした。
今回、熊本大学発生医学研究所筋発生再生分野の土屋吉史研究員(日本学術振興会PD特別研究員)は、小野悠介准教授、長崎大学の増本博司講師とともに、培養系での筋損傷モデルを構築し、損傷した筋線維から漏出する成分がサテライト細胞を活性化させることを見出しました。本研究グループはこのような漏出成分を「損傷筋線維由来因子(DMDFs:Damaged myofiber-derived factors)」と命名し、DMDFsの質量分析解析を行い、サテライト細胞を活性化させるタンパク質の同定を試みました。その結果、DMDFsとして同定された代謝酵素は、休止期のサテライト細胞を速やかに活性化させ、筋損傷からの再生を加速させる働きがあることを見出しました。本研究から、損傷した筋肉そのものがサテライト細胞を活性化させるといった、極めて合理的で効率的な再生メカニズムが存在することが明らかになりました。DMDFsは多種多様な機能があると予想されるため、今後、DMDFsのさらなる機能解明を進め、筋疾患の病態解明や創薬開発へ展開していきます。
本研究成果は、国際幹細胞学会の学会誌Stem Cell Reportsのオンライン版に令和2年9月4日(日本時間)に掲載されます。
背景
筋肉(骨格筋)は収縮する筋線維が束になって構成されており、個々の筋線維の周囲には新たに筋線維を作り出すことのできるサテライト細胞が存在します(図1)。激しい運動による肉離れや打撲等により筋線維は損傷しても再生できるのは、このサテライト細胞の働きのおかげです。また、サテライト細胞は、筋再生に加え、発育段階での筋の成長や筋力トレーニングによる筋肥大においても欠かせない役割を担っています。一方、筋ジストロフィーなどの難治性筋疾患や、近年増加の一途を辿る加齢性筋脆弱症(サルコペニア*2)の病態においては、サテライト細胞の数の減少や機能の低下がみられます。このことから、筋肉の再生治療研究において、サテライト細胞の制御機構の解明は重要な課題となっています。
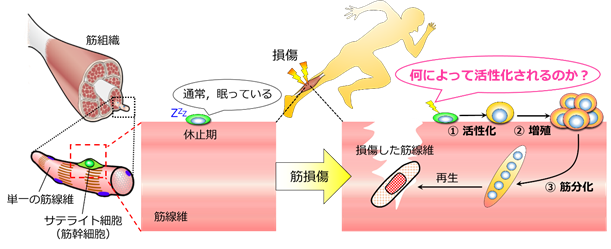
成熟した骨格筋では、サテライト細胞は通常、休止期の状態で存在しています。筋損傷等の刺激が入るとサテライト細胞は速やかに活性化し、増殖を繰り返します。その後、筋分化し、既存の筋線維あるいは互いに融合することで筋線維を再生します。すなわち、損傷後、筋線維が再生されるまでには、サテライト細胞の活性化、増殖、筋分化という3つのステップが必要になります。しかし、最初のステップである活性化はどのように誘導されるのか、その仕組みについてはほとんどわかっていませんでした(図1)。
研究の成果
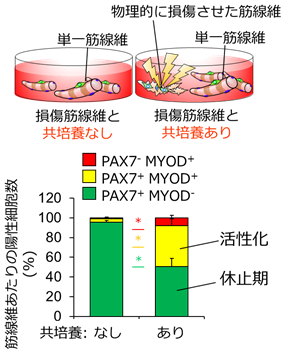
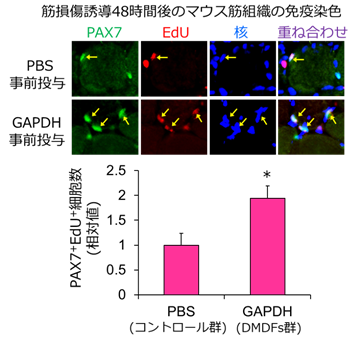
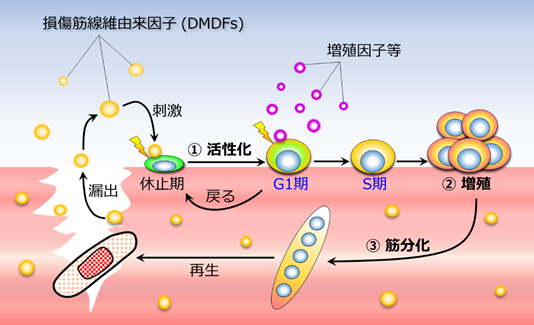
筋線維が損傷するとサテライト細胞は活性化されることから、本研究グループは筋損傷そのものが活性化のトリガーになると予想しました(図1)。しかし、骨格筋は、筋細胞とサテライト細胞以外に、血管、神経、間質組織等に存在する多様な細胞集団で構成されるため、動物の筋損傷モデルでこの仮説を証明することは困難です。そこで本研究グループは、マウス筋組織から単離した単一の筋線維に物理的損傷を加え壊死させる培養系での筋損傷モデルを構築しました。本損傷モデルを用いて解析した結果、損傷筋線維から漏出する成分はサテライト細胞を活性化させ、活性化した細胞は細胞分裂の準備期にあたるG1期に入ることを見出しました(図2)。このサテライト細胞の活性化は、損傷筋線維から漏出する成分を除去すると再び休止状態に戻ることから、損傷筋線維から漏出する成分は活性化のスイッチのような役割があると推察されます。本研究では、損傷した筋から漏出した成分を「損傷筋線維由来因子(DMDFs;Damaged myofiber-derived factors)」と命名し、質量分析によりDMDFsを同定しました。DMDFsとして同定されたタンパク質のほとんどは代謝酵素であり、その中にはグリセルアルデヒド-3-リン酸デヒドロゲナーゼ(GAPDH)*3などの解糖系酵素や、筋逸脱酵素として筋疾患のバイオマーカーとして使われているものが含まれていました。GAPDHは、本来の機能に加えて別の役割をもつムーンライティングタンパク質*4として知られており、細胞死の制御や免疫反応の媒介など、解糖系酵素以外の機能が確認されています。そこで本研究グループは、DMDFsとして同定した代謝酵素がサテライト細胞の活性化に与える影響を調べました。その結果、GAPDHを含む代謝性酵素を休止期のサテライト細胞に曝露すると、サテライト細胞は活性化しG1期に入ることを確認しました。さらに、マウス骨格筋にGAPDHを事前投与し、続いて薬剤により筋損傷を誘導すると、サテライト細胞の増殖は加速しました(図3)。以上の結果から、DMDFsは、休止期のサテライト細胞を活性化させ、筋損傷後、迅速な筋再生を誘導する機能を持つことが示唆されました。損傷した筋そのものがサテライト細胞を活性化させるメカニズムは、極めて合理的で効率の良い組織再生の仕組みであると言えます(図3、4)。
展開
本研究では、DMDFsを介した新たな筋損傷―再生モデルを提唱しました。しかし、DMDFsがどのようにサテライト細胞を活性化させるのか、活性化にかかる詳細な分子機序は不明であり、今後の課題として残りました。DMDFsのムーンライティング機能は、サテライト細胞の活性化に加え、多種多様であると予想されます。近年、骨格筋はさまざまな因子を血液中に分泌し、脳、肝臓、脂肪組織など他の臓器・組織に影響を与えることがわかってきました。したがって、DMDFsは血液循環を介して、損傷筋と他臓器との連関に関与する可能性も考えられます。今後、DMDFsの機能解明をさらに進めることで、筋疾患の病態解明や創薬開発への展開が期待されます。
用語解説
- *1 サテライト細胞
- 骨格筋の組織幹細胞。骨格筋は筋線維の束で構成されており、サテライト細胞は筋線維と基底膜の間に位置している。サテライト細胞は強力な筋再生能をもつため、筋疾患治療への応用が期待されている。
- *2 サルコペニア
- 加齢にともなう筋力・筋量減少症。介助の必要のない自立した生活を送るために、サルコペニア発症の予防改善策を見出すことは喫緊の課題である。
- *3 GAPDH
- グリセルアルデヒド-3-リン酸デヒドロゲナーゼ。解糖系酵素として細胞に豊富に発現する。解糖系酵素としてだけでなく、細胞死、転写、膜輸送などに関連しており、ムーンライティング機能があると報告されている。
- *4 ムーンライティングタンパク質
- 主要な機能に加えて別の機能をもつタンパク質。「moonlighting」は「副業」を意味することに由来。
特記事項
本研究は、AMED(再生医療実現拠点ネットワークプログラム幹細胞・再生医学イノベーション創出プログラム、難治性疾患実用化研究事業)、JSPS科研費、武田科学振興財団の助成を受けて実施されました。
論文情報
- 論文名
- Damaged myofiber-derived metabolic enzymes act as activators of muscle satellite cells(損傷筋線維由来代謝酵素は筋サテライト細胞の活性化因子として働く)
- 著者
- 土屋吉史1、2、北嶋康雄1、2、増本博司3、小野悠介1、2、4*
- 所属
-
- 熊本大学 発生医学研究所 筋発生再生分野
- 長崎大学 大学院医歯薬学総合研究科
- 長崎大学 医学部共同利用研究センター
- 熊本大学 大学院生命科学研究部附属健康長寿代謝制御研究センター
- 掲載誌
- Stem Cell Reports
- DOI
- 10.1016/j.stemcr.2020.08.002
お問い合わせ先
本発表資料のお問い合わせ先
熊本大学発生医学研究所 筋発生再生分野
准教授 小野悠介
〒860-0811 熊本市中央区本荘2-2-1
Tel:096-373-6601 Fax:096-373-6604
E-mail:ono-y“AT”kumamoto-u.ac.jp
AMED事業に関するお問い合わせ先
日本医療研究開発機構
再生・細胞医療・遺伝子治療事業部 再生医療研究開発課
Tel:03-6870-2220
E-mail:saiseinw“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和2年9月4日
最終更新日 令和2年9月4日


