改良型オキシトシン経鼻スプレーに自閉スペクトラム症中核症状に対する改善効果
プレスリリース
国立大学法人浜松医科大学
国立研究開発法人日本医療研究開発機構
研究成果のポイント
- 自閉スペクトラム症(用語解説1)の中核症状に対する世界初の治療薬としての承認申請を目指している新しい改良型のオキシトシン(用語解説2)経鼻スプレーの有効性を認めました。
- オキシトシンによる自閉スペクトラム症中核症状の改善効果に、U字型の用量反応関係があることを世界で初めて示しました。
- 従来検討されていたよりも低用量で改善効果が最大となることを示しました。
概要
浜松医科大学精神医学講座 山末英典教授は、北海道大学(責任医師:齊藤卓弥特任教授)、東北大学(責任医師:本多奈美准教授)、東京大学(責任医師:金生由紀子准教授)、名古屋大学(責任医師:岡田俊准教授(現国立精神・神経医療研究センター部長))、大阪大学(責任医師:池田学教授)、九州大学(責任医師:鬼塚俊明教授)との共同研究チームにより、帝人ファーマ株式会社と共同して改良したオキシトシン経鼻スプレーの医師主導治験(用語解説3)を実施し、自閉スペクトラム症の中核症状に対する初の治療薬として期待される改良型オキシトシン経鼻スプレーの有効性と安全性を示しました。
自閉スペクトラム症は、表情や声色を活用して相手の気持ちを汲み取ることが難しいといった対人コミュニケーションの障害と、興味や関心が偏りやすく同じ行動を繰り返しやすいという常同行動と限定的興味を主な症状とし、一般人口の54人に1人の割合で認められる発達障害ですが、その治療法は確立されていません。これまで、山末教授をはじめとした国内外の研究者が、授乳促進の適応として欧州で承認されているオキシトシン経鼻スプレー(従来型)の自閉スペクトラム症に対する有効性を検討する臨床試験を行ってきました。しかし、この従来型の単回投与では、一貫して改善効果が報告されてきた一方で、反復投与では、改善したという報告もあれば改善を認めなかったとする報告もあり、結果が異なっていました。
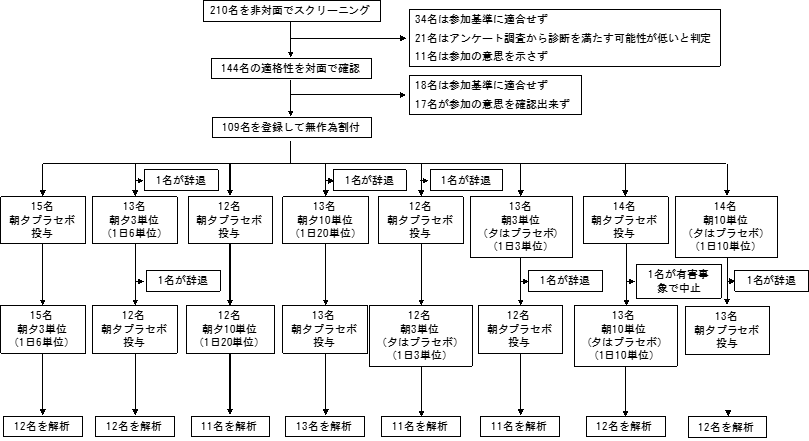
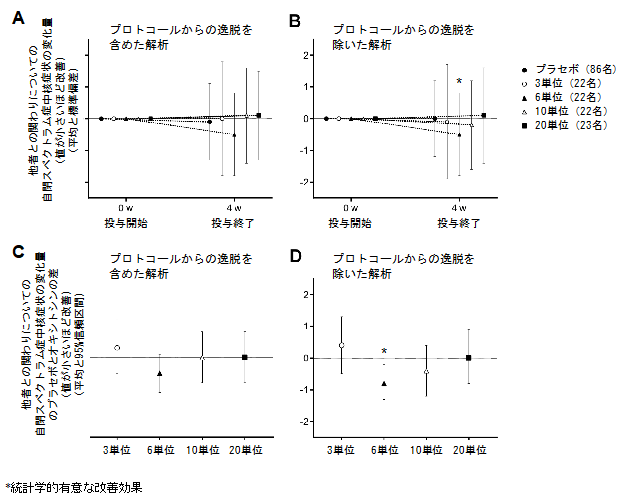
今回の医師主導治験では、授乳促進目的の従来型オキシトシン経鼻スプレーよりも生物学的利用能(用語解説4)を高める改良を行って開発した改良型オキシトシン経鼻スプレーについて、自閉スペクトラム症に対する有効性を初めて検討しました(図1)。その結果、決められた投与方法が守られなかったなどプロトコールからの逸脱のあった参加者を除外した解析で、主要評価項目としていた自閉スペクトラム症中核症状“他者との関わりについて”の改善が認められました。この有効性は、従来型製剤の単回投与で最も有効性が示されていたものに基づいた用量(1日48単位)よりも低い用量(1日6単位:ウサギでのデータを基に従来型に換算すると1日21.6単位)で認められ、この用量をピークとしたU字型の用量反応関係を認めました(図2)。
改良型オキシトシン経鼻スプレーについて初めて有効性を検討した今回の医師主導治験の結果は、さらに大規模な治験を行って確認する必要があるため、改良型オキシトシン経鼻スプレーを承認申請するための次段階の治験計画について検討を進めていきます。なお、本研究は、国立研究開発法人日本医療研究開発機構(AMED)の臨床研究・治験推進研究事業(代表:浜松医科大学・山末英典教授)および脳科学研究戦略推進プログラム『臨床と基礎研究の連携強化による精神・神経疾患の克服(融合脳):発達障害・統合失調症研究チーム(チーム長:浜松医科大学・山末英典教授)』の一環として行われました。
これらの成果は、英科学誌「BRAIN」に、2022年1月24日に公表されました。
研究の背景
自閉スペクトラム症(Autism Spectrum Disorder: ASD)は、米国疾病予防管理センターによって2020年に発表された最新の統計によれば、一般人口の54人に1人の割合で出現する頻度の高い発達障害です。社会的コミュニケーション障害と常同行動・限定的興味という中核症状は、2-3歳で明らかになり一生涯続きます。現状では、その医療上の必要性が世界的に大きいにも関わらず、これらの中核症状に対して有効な治療薬は無く、改善を期待するよりも、行動や感じ方のパターンの特徴として捉えて、その特徴にあった対処方法を身につけることが対応の主流になっています。
研究代表者の山末教授らは、ASDの中核症状に対する治療薬の候補として、オキシトシン経鼻スプレーの有効性や安全性を検討してきました(JAMA Psychiatry 2014; Brain 2014; Molecular Psychiatry 2015; Brain 2015; Molecular Psychiatry 2020; Molecular Psychiatry 2021)。欧米でも行われてきた研究と山末教授らの研究では、オキシトシンの社会的コミュニケーションの障害への効果は、単回投与では有効だったと一貫して報告されている一方、反復投与では、効果がなかった、あるいは山末教授らの研究のように、副次評価項目で効果を示したものの、主要評価項目に対しては有効性が見られなかった(Molecular Psychiatry 2020)などと報告されており、結果が異なっていました。この結果が異なる理由として、山末教授らが報告した反復投与することでオキシトシンの効果が減衰すること(Brain 2019)、に加えて、単回投与で最大の効果が得られる用量が反復投与では最適な用量ではない可能性などが考えられていました。
研究手法・成果
今回、生物学的利用能を改良して低用量から高用量まで幅広く検討することが出来る改良型オキシトシン経鼻スプレーについて、ASD中核症状に対する有効性と最適な用量を検討する臨床試験を行いました。この改良型オキシトシン経鼻スプレーは、山末教授が帝人ファーマと共同して開発し、帝人ファーマが行ったウサギの脳内での検討では従来の製剤の3.6倍の脳への移行性が認められ、健常人を対象にした安全性と薬物動態を確認する医師主導治験をすでに終えていました。今回の試験は、二重盲検プラセボ対照(用語解説5)で全国7つの大学病院での多施設試験として、医師主導治験の枠組みで、ASD中核症状に対する有効性を検討しました。
4週間の治験薬を投与する期間では、低用量の改良型オキシトシン製剤(3単位)の1日1回投与(3単位)、低用量オキシトシンの1日2回投与(6単位)、高用量オキシトシン(10単位)の1日1回投与(10単位)、高用量オキシトシンの1日2回投与(20単位)のいずれかに各参加者は振り分けられました。治験薬の有効性を評価する主要評価項目には、ASDの中核症状を評点して診断をする際のゴールドスタンダードとして世界的に認められている方法の他者との関わりについての項目の点数(0点から14点の範囲の点数が付き、点数が高いほど症状が重い)の4週間の投与期間前後の変化量を用いました。各参加者は、4種類の用量(1日3単位、6単位、10単位、20単位)のいずれかのオキシトシン投与を4週間行い、さらに参加者全員が4週間のプラセボ投与も受けました。オキシトシン投与を4週間受けた後に4週間の休薬期間を挟んで4週間のプラセボ投与を受ける参加者と、逆の順番でプラセボ投与を4週間受けた後に4週間の休薬期間を挟んで4週間のオキシトシン投与を受ける参加者に、ランダムに振り分けられました。2018年6月に最初の参加者が登録され、2020年3月に最後の参加者の全観察期間が終了しました。
その結果、109名の正常知能のASDと診断された参加者がランダムな振り分けを受けて、そのうち102名の参加者が試験を完了しました(図1)。用量と改善効果の関係性の検討では、6単位の投与効果をピークとしてU字型の用量反応関係が示されました。決められた投与方法が守られなかったなどのプロトコールからの逸脱のあった参加者を除いた最大94名での解析では、主要評価項目である他者との関わりについてのASD中核症状得点について、オキシトシン6単位の投与による統計学的に有意な改善が認められました(図2)。一方で、プロトコールからの逸脱のあった参加者を含めた解析では、主要評価項目および主要評価項目での有効性の検討を捕捉する目的で設けた副次評価項目に統計学的に有意な改善を認めませんでした。
安全性については、いずれの用量でも深刻な有害事象は認めませんでした。軽微なものまで含めた有害事象の発現割合は、3単位投与期間中が24.0%、6単位投与期間中が46.4%、10単位投与期間中が40.7%、20単位投与期間中が40.0%、プラセボ投与期間中が36.9%という結果でした。
早期第II相試験と位置付けた今回の治験は、生物学的利用能を高めた改良型オキシトシン経鼻スプレーの有効性を初めて検討し、この新製剤の特長を活かして低用量から高用量までの幅の広い用量設定をすることで、他者との関わりについてのASD中核症状への有効性が、従来の製剤(改良前の製剤)の単回投与で最も有効性が示されていた用量(1日48単位)よりも低い用量(1日6単位:ウサギでのデータを基に従来型に換算すると1日21.6単位)で、この用量をピークとしたU字型の用量反応関係が認められることを初めて見出しました。オキシトシンについて、今回の様な生物学的利用能を高めた新製剤について有効性を検討した臨床試験は国内外で例がなく、二重盲検プラセボ対照などの厳密な方法を用いてこのような重要な結果を報告する本試験は画期的なものと考えられます。今回、本試験結果を報告する論文が、臨床神経科学の学術誌BRAIN誌に掲載決定の運びとなりました。
今後の展開
改良型オキシトシン経鼻スプレーの有効性を初めて検討した今回の治験の結果は、今後さらに多くの参加者を対象とした規模の大きな治験を行って確認する必要があります。特に、今回の治験で有意な改善を見出せなかった、決められた投与方法が守られなかったなどのプロトコールからの逸脱があった参加者も含めた解析は、プロトコールからの逸脱を認めた参加者を除外した解析よりも、日常診療の場面での治療には近いと考えられており、こうした解析でも有意な改善を示すことが重要視されています。そのため、今後は、改良型オキシトシン経鼻スプレーの次段階の治験及び承認申請に協力する企業パートナーを探していきます。
用語解説
- (用語解説1)自閉スペクトラム症(自閉症スペクトラム障害)
- 従来の自閉症からアスペルガー障害や特定不能の広汎性発達障害までを含む概念です。自閉症的な特性は、重度の知的障害を伴った自閉症から、知的機能の高い自閉症を経由し、自閉スペクトラム症の症状を持ちながらも症状の数が少なく程度も軽い正常範囲の人まで続くスペクトラムを形成するという考えに基づいています。
- (用語解説2)オキシトシン
- 脳の下垂体後葉から分泌されるホルモンで、従来は子宮平滑筋収縮作用を介した分娩促進や乳腺の筋線維を収縮させる作用を介した乳汁分泌促進作用が知られていました。しかし一方で男女を問わず脳内にも多くのオキシトシン受容体が分布していることが知られ、脳への未知の作用についても関心が持たれていました。そうした中、健康な大学生などを対象とした研究において、他者と信頼関係を築きやすくする効果などが報告されて注目を集めていました。
- (用語解説3)医師主導治験
- 医薬品の安全性・有効性を調べ、厚生労働省の承認を得るための臨床試験である、「治験」について、2003年の薬事法改正後からは、製薬企業等と同様に医師自ら治験を企画・立案し、治験計画届を提出して実施できるようになりました。この治験の準備から管理を医師自ら行うことを医師主導治験といいます。
- (用語解説4)生物学的利用能
- 投与された薬剤のうち、どれだけの量が体内に取り込まれるかの程度や割合のことを言います。
- (用語解説5)二重盲検プラセボ対照
- プラセボとは有効成分を含まない偽薬のことです。思い込みなどから生じる偽薬によるプラセボ効果や観察者の先入観などを排除するために、臨床試験の参加者も試験担当者も偽薬か有効成分を含む実薬か分からない状態で投薬や検査を行って、治療薬の有効性・安全性を検討する方法です。
論文情報
- 発表雑誌
- BRAIN (ブレイン)
- 論文タイトル
- Effect of a novel nasal oxytocin spray with enhanced bioavailability on autism: A randomised trial
- 著者
- Hidenori Yamasue*, Masaki Kojima, Hitoshi Kuwabara, Miho Kuroda, Kaori Matsumoto, Chieko Kanai, Naoko Inada, Keiho Owada, Keiko Ochi, Nobutaka Ono, Seico Benner, Tomoyasu Wakuda, Yosuke Kameno, Jun Inoue, Taeko Harada, Kenji Tsuchiya, Kazuo Umemura, Aya Yamauchi, Nanayo Ogawa, Itaru Kushima, Norio Ozaki, Satoshi Suyama, Takuya Saito, Yukari Uemura, Junko Hamada, Yukiko Kano, Nami Honda, Saya Kikuchi, Moe Seto, Hiroaki Tomita, Noriko Miyoshi, Megumi Matsumoto, Yuko Kawaguchi, Koji Kanai, Manabu Ikeda, Itta Nakamura, Shuichi Isomura, Yoji Hirano, Toshiaki Onitsuka, Hirotaka Kosaka, Takashi Okada
*責任著者
研究グループ
本研究は、浜松医科大学(代表・責任医師:山末英典教授)と、北海道大学(責任医師:齊藤卓弥 特任教授)、東北大学(責任医師:本多奈美准教授)、東京大学(責任医師:金生由紀子准教授)、名古屋大学(責任医師:岡田俊准教授(現国立精神・神経医療研究センター部長))、大阪大学(責任医師:池田学教授)、九州大学(鬼塚俊明教授)、帝人ファーマとの共同研究で、日本医療研究開発機構(AMED)臨床研究・治験推進研究事業(代表:浜松医科大学・山末英典)および、脳科学研究戦略推進プログラム『臨床と基礎研究の連携強化による精神・神経疾患の克服(融合脳):発達障害・統合失調症研究チーム(チーム長:浜松医科大学・山末英典)』の一環として行われました。
研究支援
日本医療研究開発機構(AMED)の臨床研究・治験推進研究事業(2017年5月~2021年3月、代表:浜松医科大学・山末英典)および、脳科学研究戦略推進プログラム『臨床と基礎研究の連携強化による精神・神経疾患の克服(融合脳):発達障害・統合失調症研究チーム(2016年4月~2017年4月、チーム長:浜松医科大学・山末英典)』ならびに、浜松医科大学精神医学講座の委任経理金の援助で行いました。また、帝人ファーマから治験薬の提供を受けました。
お問い合わせ先
本件に関するお問い合わせ先
国立大学法人浜松医科大学 精神医学講座
〒431-3192 浜松市東区半田山1-20-1
教授 山末 英典
TEL:053-435-2295 FAX:053-435-3621
E-mail:yamasue"AT"hama-med.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構
〒100-0004 東京都千代田区大手町1-7-1 読売新聞ビル
創薬事業部 規制科学推進課
TEL:03-6870-2235
E-mail:rinsho-crt"AT"amed.go.jp
疾患基礎研究事業部 疾患基礎研究課
TEL:03-6870-2222
E-mail:brain-pm"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和4年1月25日
最終更新日 令和4年1月25日


