最長寿げっ歯類ハダカデバネズミから神経幹細胞の単離と培養に成功―脳の老化やがんを防ぐ方法の開発に貢献―
成果情報
熊本大学
慶應義塾大学
日本医療研究開発機構
ポイント
- 老化しにくい・がんになりにくい最長寿げっ歯類ハダカデバネズミから神経幹細胞※1を単離・培養することに成功しました。
- ハダカデバネズミ神経幹細胞は、ハツカネズミ(マウス)の神経幹細胞と比べて、増殖が遅く、DNA損傷への耐性を持つことが分かりました。
- 上記の神経幹細胞の特徴が、ハダカデバネズミの長い生涯の中で神経幹細胞の枯渇や機能不全を防ぐ一因である可能性が考えられます。
概要説明
熊本大学大学院医学教育部博士課程2年の山村祐紀大学院生、同大学院先導機構/同大学院生命科学研究部老化・健康長寿学講座の河村佳見助教、三浦恭子准教授らは、慶應義塾大学医学部先端医科学研究所遺伝子制御研究部門の大西伸幸訪問研究員、佐谷秀行教授と共同で、ハダカデバネズミ(以下、「デバ」)の脳から神経幹細胞を単離・培養することに世界で初めて成功しました。神経幹細胞は、ニューロンなどの細胞を供給することで、中枢神経系の恒常性維持を支えており、その枯渇や機能異常は、脳の老化やがんの一因となります。デバは老化やがんがおこりにくく、現在確認されている上で最大寿命が37年を超える最長寿げっ歯類であり、その幹細胞も枯渇や機能不全に耐性を持つ可能性があります。しかし、これまでデバの神経幹細胞は殆ど研究されていませんでした。今回、本研究グループは、デバ神経幹細胞の単離・培養に世界で初めて成功し、それをマウス由来の神経幹細胞と比較しました。その結果、デバ神経幹細胞は、マウスに比べて、増殖速度が遅いこと、DNA修復が早く開始され細胞死が起こりにくいことを明らかにしました。これらのデバ神経幹細胞の特徴は、30年を超えるデバの長い生存期間の中で脳の恒常性維持に寄与している可能性があります。今後さらに研究を発展させることで、ヒトの脳の老化やがんを防ぐ新たな方法の開発に貢献することが期待できます。
本研究成果は、科学雑誌「Inflammation and Regeneration」に2021年11月1日に掲載されました。本研究は、日本医療研究開発機構(AMED)「再生医療実現拠点ネットワークプログラム(幹細胞・再生医学イノベーション創出プログラム)」、「老化メカニズムの解明・制御プロジェクト」、文部科学省科学研究費助成事業などの支援を受けて実施したものです。
説明
背景
デバは、アフリカ北東部の地下に暮らす小型のげっ歯類です。マウスと同程度の大きさですが、マウスの寿命が3年程度であるのに対し、デバは最大寿命が30年を超える最長寿のげっ歯類として知られています。また、老化しにくく、生涯に渡って殆ど腫瘍形成が起こらない顕著ながん化耐性を持つことから、近年大きな注目を集めています。
神経幹細胞は、主に脳の脳室下帯や海馬歯状回に存在する組織幹細胞で、ニューロンなどの分化細胞を供給することで中枢神経系の恒常性維持に寄与しています。そして神経幹細胞の枯渇や機能不全は老化やがんの一因となります。
最長寿げっ歯類であるデバの神経幹細胞は、このような幹細胞の枯渇や機能不全に耐性を持つことが予測されますが、これまでに殆ど研究されてきませんでした。そこで本研究では、デバの脳室下帯から神経幹細胞を単離し、その基礎的な性状を解析しました。
研究の内容と成果
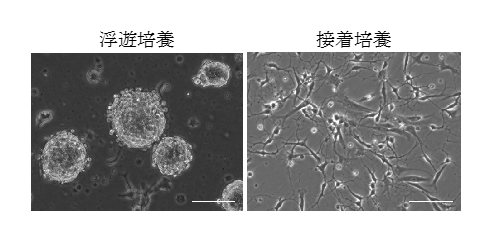
デバ新生仔の脳室下帯から神経幹細胞及び神経前駆細胞※2(以下、「神経幹/前駆細胞」)を単離し、浮遊培養及び接着培養の培養条件を確立しました(図1)。そして、培養した細胞を免疫蛍光染色することにより、SOX2などの神経幹細胞マーカーが発現することを確認しました。また、同細胞を分化誘導するとニューロン・アストロサイト※3・オリゴデンドロサイト※4が出現することが確認され、神経幹細胞としての基本的な要件を満たした状態で維持できていることが明らかになりました(図2)。
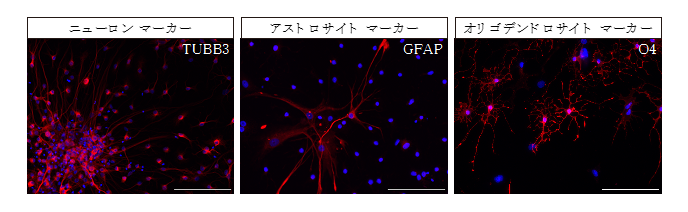
デバ神経幹/前駆細胞はニューロン・アストロサイト・オリゴデンドロサイト(赤色)へ分化できることが確認された。青色:細胞核。スケールバー:100 µm。
続いて同じ方法で単離したマウス神経幹/前駆細胞とデバ神経幹/前駆細胞について、同じ培養条件で細胞増殖を比較しました。その結果、デバ神経幹/前駆細胞は、マウスと比較して倍加時間が1.5倍ほど長く、細胞周期のG0期(細胞分裂を停止している期間)及びG1期(細胞分裂の準備期間)に属する細胞の割合が高いことが明らかになりました(図3)。
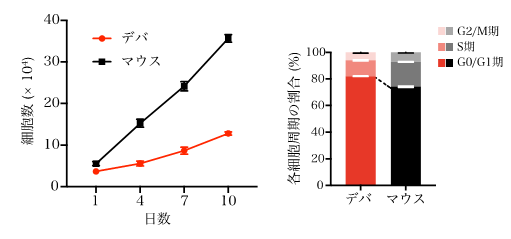
デバ神経幹/前駆細胞は増殖が遅く、G0/G1期の割合が高いことが明らかになった。
次に、デバ及びマウスの神経幹/前駆細胞にγ線※5を照射しDNA損傷応答を比較しました。デバ神経幹/前駆細胞は、DNA二重鎖切断マーカーであるγH2AXのシグナル強度がマウスと比較して低く抑えられており、DNA損傷修復マーカーである53BP1やpATMがより多く損傷部位に集積していました(図4)。また、デバ神経幹/前駆細胞はマウスとは異なり、γ線を照射して24時間後においても細胞死が殆ど亢進していませんでした。以上のことから、デバ神経幹/前駆細胞はDNA損傷に対して耐性を持つと考えられます。
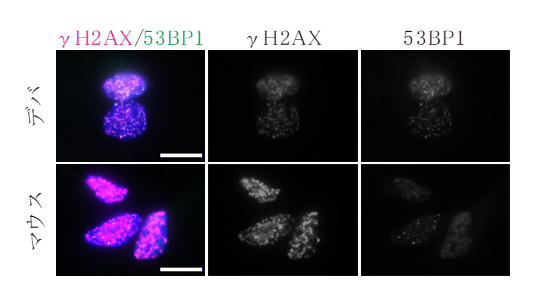
展開
デバ神経幹/前駆細胞が持つ細胞増殖の遅さやDNA損傷への耐性は、デバの長い生涯の中で神経幹細胞の枯渇や機能不全を防ぐ一因である可能性があります。本研究は、デバの長寿やがん化耐性のメカニズムを理解する上で重要な知見を提供するものです。さらに研究を発展させることで、ヒトの脳の老化やがんを防ぐ新たな方法の開発に貢献することが期待できます。
用語解説
- ※1 神経幹細胞
- 未分化な状態を保って増殖する自己複製能と、中枢神経系を構成するニューロン・アストロサイト ・オリゴデンドロサイトへ分化する能力を持つ。
- ※2 神経前駆細胞
- 未分化ではあるが、限られた分裂回数の後に神経系細胞へ分化を遂げるように運命付けられた細胞。
- ※3 アストロサイト
- 中枢神経系を構成するグリア細胞の一種。ニューロンへの栄養供給や構造的な支持など様々な役割をもつ。
- ※4 オリゴデンドロサイト
- 中枢神経系を構成するグリア細胞の一種。ニューロンの軸索部分を覆うミエリンを形成するなどの役割をもつ。
- ※5 γ線
- DNA損傷の中で最も重篤なDNA二重鎖切断を引き起こす。
論文情報
- 論文名
- Isolation and characterization of neural stem/progenitor cells in the subventricular zone of the naked mole-rat brain
- 著者
- Yuki Yamamura, Yoshimi Kawamura, Yuki Oiwa, Kaori Oka, Nobuyuki Onishi, Hideyuki Saya, and Kyoko Miura
- 掲載誌
- Inflammation and Regeneration
- doi
- 10.1186/s41232-021-00182-7
- URL
- https://inflammregen.biomedcentral.com/articles/10.1186/s41232-021-00182-7
お問い合わせ先
研究に関すること
熊本大学大学院先導機構/同大学院生命科学研究部 老化・健康長寿学講座
准教授 三浦恭子
電話:096-373-6852
E-mail:miurak“AT”kumamoto-u.ac.jp
報道に関すること
熊本大学 総務部 総務課 広報戦略室
電話:096-342-3269
E-mail:sos-koho“AT”jimu.kumamoto-u.ac.jp
慶應義塾大学 信濃町キャンパス総務課
電話:03-5363-3611
E-mail:med-koho“AT”adst.keio.ac.jp
AMED事業に関するお問い合わせ先
日本医療研究開発機構(AMED)
再生医療実現拠点ネットワークプログラム(幹細胞・再生医学イノベーション創出プログラム)
再生・細胞医療・遺伝子治療事業部 再生医療研究開発課
電話:03-6870-2220
E-mail:saiseinw“AT”amed.go.jp
老化メカニズムの解明・制御プロジェクト
疾患基礎研究事業部 疾患基礎研究課
電話:03-6870-2286
E-mail:aging“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和3年11月1日
最終更新日 令和3年11月1日


