多数のがん遺伝子変異を効率よく解析する「MANO法」の開発
 多数のがん遺伝子変異を効率よく解析する画期的な手法の開発
多数のがん遺伝子変異を効率よく解析する画期的な手法の開発
創薬戦略部 医薬品研究課
がん発症との関連性や抗がん剤に対する感受性を明らかに
東京大学の間野博行教授、高阪真路特任助教ら(当時所属)は、がん細胞中には臨床的意義が不明な遺伝子変異が数多くあることに注目し、培養細胞を用いてこれらの遺伝子変異を効率的に評価する新しい手法「MANO法」を開発しました。遺伝子変異のそれぞれのがん化能や抗がん剤の有効性を体系的に解明するツールとなり得るため、一人ひとりの遺伝子を調べその人に合う治療法を選択するがんゲノム医療の推進に大きく貢献できると期待されます。
取り組み
近年、がん細胞中の遺伝子変異(遺伝子を構成するDNAの塩基配列が変わり、正常な遺伝子と異なる情報を持つもの)が、がん発症と深く関わっていることが明らかになりつつあります。しかし、このがん遺伝子変異の中で働きが分かっているものはごくわずかで、大半はがんとの関係やがん治療薬の有効性が解明されていません。例えば、肺腺がんと関係の深いEGFR遺伝子の変異は1000種類以上あるといわれていますが、これまでは一つひとつの変異を個別に解析していたため多くの時間と労力がかかり、働きが分かっている遺伝子変異は30種類程度しかありませんでした。
国立がん研究センター研究所の間野博行所長(2018年3月まで東京大学大学院教授併任)と同研究所の高阪真路主任研究員(同3月まで東京大学大学院特任助教)らは、数百種類の遺伝子変異の働きを一度に解析することができる新しい手法「MANO法」(mixed-all-nominated-mutants-in-one method)を開発しました。
「MANO法」は、培養細胞に調べたい複数の遺伝子変異に目印となる塩基配列を付け、導入し、20日間一定の条件で培養します。細胞が増殖すればがん化の可能性(がん化能)があると分かるため、導入した遺伝子に付けた目印の量を「次世代シーケンサー」(DNAの塩基配列を高速に調べる装置)で測定し、それぞれの遺伝子変異が細胞の増殖にどのような影響を与えたかを調べるという方法です。
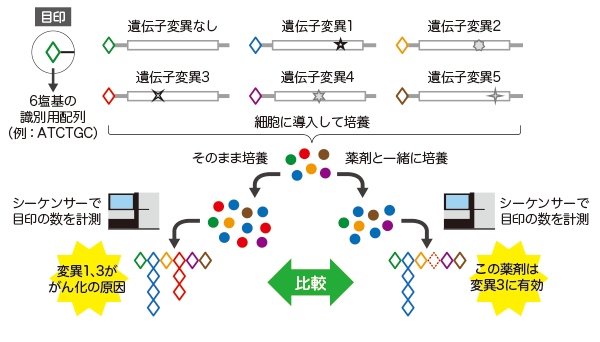
一度に数百種類調べられるため、これまで働きが分かっていなかった遺伝子変異を網羅的に解析できると期待されます。また、培養段階で抗がん剤を加えれば、その細胞の増殖の変化をみることにより、どの抗がん剤がどの遺伝子変異に対して有効なのか、また有効でないのかも調べることができます。
成果
研究グループはMANO法を使い、101種類のEGFR遺伝子変異を調べたところ、64種類の遺伝子変異に細胞を増殖させる働きがあることが分かりました。さらにEGFR遺伝子変異のある患者さんに現在使われている6種類の抗がん剤(EGFR阻害薬)による影響を調べたところ、同じEGFR遺伝子変異であっても、細胞の増殖が抑えられない変異や、遺伝子変異がいくつか重なると細胞の増殖が抑えられにくくなることも分かりました。
今回、MANO法で調べたEGFR遺伝子の各遺伝子変異の抗がん剤に対する感受性は、実際に患者さんに使用した際の知見と一致していたことから、MANO法で得られる情報は、臨床に応用できることが期待されます。
展望
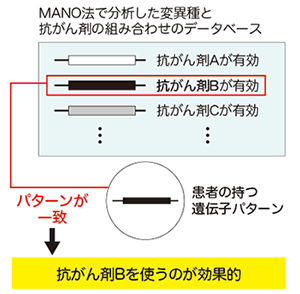
がん患者の遺伝情報を調べて最適な治療法を選択する「がんゲノム医療」が始まっています。医薬品開発において、多数の遺伝子変異に対して、一度に医薬品候補化合物の効果を比較評価することができるため、新たな分子標的薬の探索にも応用可能な技術と考えられます。さらに、がん遺伝子変異の働きを解明し、網羅的にデータベース化すれば、一人ひとりの患者さんに最適な治療薬を選ぶことが可能になります。「シンプルだが、大変パワフルなツール」と間野所長が話すように、一度に大量の遺伝子変異の解析ができるMANO法はがんゲノム医療の実現に資する画期的な手法となることが期待されます。
関連リンク
最終更新日 平成30年11月15日


