AMEDシンポジウム2017開催レポート:招待講演② レギュラトリー・サイエンスに基づくイノベーションの活性化(1)
 招待講演➁ レギュラトリー・サイエンスに基づくイノベーションの活性化―「合理的な医療」を目指して―
招待講演➁ レギュラトリー・サイエンスに基づくイノベーションの活性化―「合理的な医療」を目指して―
近藤 達也氏(独立行政法人 医薬品医療機器総合機構 理事長)

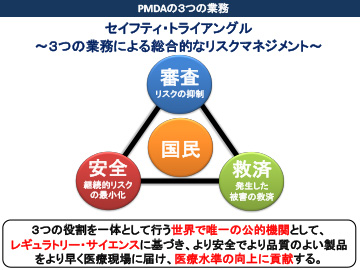
医薬品医療機器総合機構(PMDA)は、医薬品・医療機器に関する審査、安全対策、健康被害救済の3つを主な業務として医療水準の向上に貢献しています。PMDAが推進する「レギュラトリー・サイエンス」は、成果を的確に予測する「評価」と、技術を社会にどのように適用させるかを「適正規制」するもので、日本が世界をリードしていくために、一層の強化が求められています。 近藤理事長は日本の医薬品・医療機器開発の大きな問題とされてきたドラッグ・ラグ、デバイス・ラグを解消し、レギュラトリー・サイエンス総合相談や先駆け審査指定制度など、レギュラトリー・サイエンスに基づく規制のイノベーションを推し進めています。また、アカデミアとの交流促進や実用化を支援する相談事業の充実などで、開発分野の合理化も目指しています。
レギュラトリー・サイエンスとは
PMDAの近藤です。今日は、レギュラトリー・サイエンスを中心にして、それに基づくイノベーションの活性化について、お話させていただこうと思います。
2014年に薬事法は「医薬品・医療機器等の品質、有効性、安全性の確保等に関する法律(薬機法)」と名称を変え、新たに医療機器や再生医療などの製品に関しても制度として明確化されました。私たちPMDAでは、その薬機法に基づいた医薬品・医療機器等に関する「審査」、「安全対策」、「(健康被害)救済」の3つを主な業務としています。
演題にあります「レギュラトリー・サイエンス(RS)」という概念は、1981年に国立衛生試験所(現・国立医薬品食品衛生研究所)の副所長であった内山充氏によって提唱されたものです。
レギュラトリー・サイエンスとは、科学技術の進歩の所産をメリットとデメリットの観点から評価・予測する方法を研究し、社会生活との調和の上で、最も望ましい形に調整することであり、そこにはコンプライアンスが必要です。
また内山氏は、レギュラトリー・サイエンスを2つの要素に分けておられます。
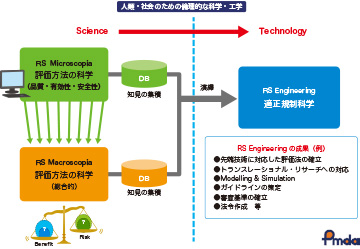
一つは、科学技術のもたらす成果をよいことも、悪いことも的確に予測するという「評価科学」、つまりこれは本当にいいものかどうか、どういう点がよくない点かということを評価・予測する科学です。
もう一つは、人間と社会との調整を実現するという「適正規制科学」です。適正規制科学とは、評価されて決まったものを社会にどのように適用するか、例えばトランスレーショナル・リサーチに応用するとか、ガイドラインを策定する、法令をつくる、審査基準を確立するなど人類や社会のための倫理的な考察を加えた科学・工学です。
いろいろな化学物質の発明、発見が社会に出るとき、この評価科学が正しくないと潰されてしまいます。私たちは、価値のあるものを正しく評価するような仕組みを、国全体で考えていかなければならない。また、それをどう育てていくかということを考えていかなければなりません。まさしくレギュラトリー・サイエンスの活性化が必要なのです。
ところが、日本は他の研究開発先進国に比べて、レギュラトリー・サイエンスの定着がやや弱いと考えています。多くの発明や研究が、外国で初めて評価され、実用化されているのが実状です。日本も、他の国がやっていないことを否定するのではなく、新しいものを評価する国になっていかなければなりません。
最終更新日 平成29年10月16日