AMEDシンポジウム2017開催レポート:招待講演② レギュラトリー・サイエンスに基づくイノベーションの活性化(2)
 招待講演➁ レギュラトリー・サイエンスに基づくイノベーションの活性化―「合理的な医療」を目指して―
招待講演➁ レギュラトリー・サイエンスに基づくイノベーションの活性化―「合理的な医療」を目指して―
近藤 達也氏(独立行政法人 医薬品医療機器総合機構 理事長)
レギュラトリー・サイエンスに基づいてアカデミアと連携強化
PMDAでは科学的な判断の高度化を図るため、アカデミー発のトランスレーショナル・リサーチを推進することを目指しています。そのため、レギュラトリー・サイエンスに基づき、アカデミアとの連携強化を図っています。
まず、2009年からPMDAの職員が社会人入学の形で大学院生となり、PMDAの業務に従事しつつ、PMDA業務に関連した研究を行うことにより学位取得を目指す「連携大学院制度」を開始しました。2010年には当時、国立がん研究センター総長(現・山形大学医学部がんセンター長)の嘉山孝正氏と組んで、レギュラトリー・サイエンスに関する講座を初めて開設しました。2014年までに19の大学と連携大学院制度を結び、レギュラトリー・サイエンスに関係する学術論文や学位を持った人材を育てています。
また、2012年から2016年度にかけて革新的医薬品・医療機器・再生医療製品実用化促進事業を、2015年からは包括的連携協定制度をスタートさせました。包括的連携制度では大学だけでなく、国立がん研究センターなどのナショナルセンターとも連携し、人材の交流を進めています。
2012年に設置した科学委員会は、PMDAの審査員が自信を持って判断できるような仕組みを作るため、医薬品、医療機器に関して優れた学識経験・研究業績を有する研究者に集まっていただき意見交換を行っています。直近では、希少な疾患における臨床評価のあり方、新薬開発の現状と問題点、AIの活用などを検討テーマとして、さまざまな角度からご議論をいただいています。
PMDAの革新的な医薬品・医療機器等の開発促進への取り組み―有効成分の審査期間は世界最速
日本は歴史的に見ても創薬能力や医療機器の開発・改良能力が高く、規制当局であるPMDAもそれに対応していくことが求められています。それがレギュラトリー・サイエンスの「適正規制」の改革です。
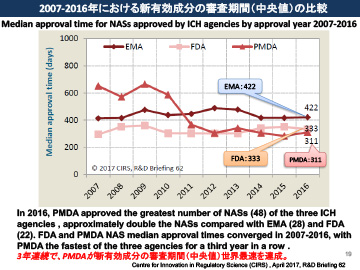
米国CIRSの発表では、PMDAは2014年から3年連続で新有効成分の審査期間で世界最速を達成しています。2007年には600日以上かかっていたのが、2016年には311日まで短縮しているのです。つまり日本が世界に先駆けて新薬を承認するような時代になってきたということで、これは審査能力の高さを表しています。承認された新有効成分の品目数でも、日本は昨年米国を抜いて世界トップです。
どのようにして審査期間を短縮したのかというと、承認申請前に企業がPMDAに相談をする仕組みを作り、しっかりと話し合いをして無駄な時間を使わないようにしたのです。
規制当局自身もイノベーションを
さて、医薬品・医療機器もどんどんイノベーションが生まれますが、規制当局自身もレギュラトリー・サイエンスを用いて規制をより合理的・効率的に改革をしていかなければなりません。
そこでPMDAは、開発段階では、有望なシーズの開発を次段階に結びつける支援として、薬事戦略相談事業を始めました。審査段階では科学委員会の設置、再生医療等製品の条件・期限付き承認の開始、革新的医薬品・医療機器・再生医療等製品の日本発の開発を支援する「先駆け審査指定制度」も世界で最初に作りました。市販後は、電子診療情報等を安全対策へ活用する体制を構築するための事業、MIHARI Projectを実施してまいりました。この5年間でさまざまな試行調査を通じて、各種電子診療情報データベースへのアクセス確保、データ特性評価、及び、薬剤疫学手法の検討を行い、医薬品処方後の有害事象発現リスクの定量的評価や、安全対策措置の影響評価、処方実態調査等が行える体制を構築しました。また、平成30年度からは医療情報データベースシステム「MID-NET」を本格運用し、MID-NETを通じて得られるリアルワールドデータを使った自発的な安全対策等を実施する予定です。こういうことを次々と創意工夫してやっています。
最終更新日 平成29年10月16日