AMEDシンポジウム2017開催レポート:成果報告③ 国産技術による次世代バイオ医薬品製造技術基盤の開発(1)
 成果報告➂ 国産技術による次世代バイオ医薬品製造技術基盤の開発
成果報告➂ 国産技術による次世代バイオ医薬品製造技術基盤の開発
大政 健史氏(大阪大学大学院教授)
医薬品市場においてこれから大きな成長が期待されるバイオ医薬品ですが、日本には優れた要素技術が多数ある一方、製造技術基盤や生産拠点の整備の遅れがボトルネックとなっています。
こうした問題点を解消するため、「国産技術による次世代バイオ医薬品製造技術基盤の開発」が平成25年度から5カ年の計画で進行中です。純国産のバイオ医薬品の製造基盤の確立を目指し、プロジェクトリーダーの大政健史氏(大阪大学大学院教授)を中心に、28企業、3団体、1国法、4大学による技術研究組合が結成され、オールジャパンによる取り組みが進んでいます。研究成果を実際の製造に活かすための研究施設「神戸GMP施設」についても紹介されました。

はじめに
本日は、抗体医薬品等のバイオ医薬品の製造技術基盤の開発についてお話をさせていただきます。 バイオ医薬品にはさまざまな定義がありますが、ここで取り上げるのは、たんぱく質や哺乳類の細胞、ウイルス、バクテリアなどの生物によって生産される物質に由来するものです。例えば「オプジーボ」という免疫作用を利用した抗がん剤、「アクテムラ」という関節リウマチに効くような抗体医薬もバイオ医薬品です。
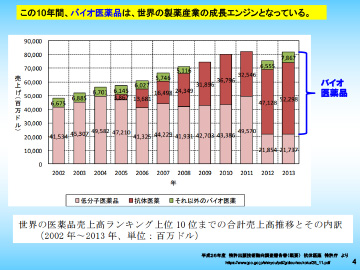
バイオ医薬品はここ10年ほど、世界の製薬産業の成長エンジンとして数多く上市されてきました。2013年には世界の売り上げベスト10のうち約7割をバイオ医薬品が占めています。バイオ医薬品、特に抗体医薬は、今後も持続して大きく成長すると期待されています。
従来の医薬品とは全く異なる製造工程
バイオ医薬品は分子量が多く、抗体医薬の分子量は15万ぐらいです。ヒト成長ホルモン分子量が3000ぐらい、アスピリンのような小さな化合物は21ぐらいです。アスピリンを自転車に例えると、ヒト成長ホルモンは車、抗体医薬はビジネスジェット並みの非常に大きな分子であるといえ、抗体医薬がいかに複雑かお分かりになっていただけると思います。
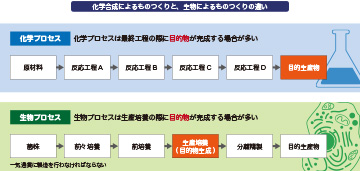
また、バイオ医薬品は生き物を使うため、製造も非常に難しいのです。従来のように化学合成で医薬品を作る場合は、反応工程を分けて行うことも可能です。例えば、原材料から中間反応物までを別の国にて合成し、それを輸入して、また別の国で次の反応工程を行い中間反応物を得て、それを輸入して最後の仕上げの合成だけ日本で行うようなことも可能です。一方、バイオ医薬品は生き物を使うため、途中まで別の国で行うということができません。最初から最後まで同じところで、一気通貫に製造することが必要です。また、菌株(細胞)の培養から目的物生成、分離精製、製剤化に至るまで同じ技術で、継続して品質管理することが求められます。今日作った抗体医薬品と10年後に作る抗体医薬品が、すべて同じ品質でないとならないのです。
「技術研究組合」で取り組
先ほど、バイオ医薬品はこれから大きく成長する市場だとお話しました。世界の医薬品売り上げベスト10のうち、抗体医薬は6品目もあります。バイオ医薬品の製造は複雑で高度な技術が必要です。主に先進国で抗体医薬に関するさまざまな技術が開発されており、非常にポテンシャルが高いのはアメリカですが、日本も世界ベスト2の非常に高い技術を有しています。また、ドイツ、イギリス等、たくさんの国が拮抗している状態になっています。 そこで、我が国での本分野の研究開発をさらに推し進めるために、国際基準に適合した次世代抗体医薬等の製造技術の基盤の研究開発を行う研究課題が平成25年度からスタートし、現在、AMEDの支援のもとで運営されています。
この研究課題では28企業、3団体、1国法、4大学が技術研究組合を作り、一体となって取り組んでいます。各企業等がさまざまな技術を持ち寄って、一緒に製造プロセス全体を開発することが狙いです。これは、各企業の一つひとつの技術は非常に優れているものの、それらを組み合わせて開発することが今までなかったからです。
知的財産についても、技術研究組合制度を使って一元化し、ユーザーである製薬会社の意見も取り入れて、実際のプロジェクトを一体運営する形で動いています。 研究開発は、細胞の構築、培養、分離・精製、品質管理、ウイルスの安全性の管理技術の開発、それらを一体としてプラットフォーム化する技術開発から構成されています。研究開発の項目も非常に多岐にわたり、現在は約90の研究課題、約550人の研究者が参画しています。
最終更新日 平成29年10月17日