AMEDシンポジウム2017開催レポート:成果報告➅ ヒトiPS細胞技術を活用した薬理試験法の開発と国際標準化(2)
 成果報告➅ ヒトiPS細胞技術を活用した薬理試験法の開発と国際標準化
成果報告➅ ヒトiPS細胞技術を活用した薬理試験法の開発と国際標準化
末松 誠(AMED理事長)
諫田 泰成氏(国立医薬品食品衛生研究所 薬理部長)
ヒトiPS細胞を用いた大規模な検証実験の実施
私たちは、ヒトiPS細胞由来心筋細胞を用いて、世界で初めてTdPの発生予測に関する大規模な検証実験を実施しました。ヒトiPS細胞由来心筋細胞の電気活動を多点電極(MEA)システムにより記録する薬理評価を実施しました。陽性対照化合物を心筋シートに添加したところ、TdPの発生メカニズムに関わる早期後脱分極(EAD)やTriggered Activityなど異常な心臓の電気活動を示す指標を見いだすことができました。これらは従来のhERG試験では評価できないことから、有用な指標となることが考えられました。
この試験法の有用性を示すため、TdPのリスクが異なる60種類の化合物を選定して大規模な検証実験を実施しました。さらに、TdPリスクのスコア化を行い、各化合物のスコアをプロットするグラフを作成しました。縦軸にTdPリスクスコア、横軸には作用が認められた濃度と臨床有効血中濃度との比を取ったところ、19種類の高リスク化合物と17種類の低リスク化合物、それ以外の化合物に分類することができました。
臨床データとの類似性は80%以上
高リスク化合物、低リスク化合物を実際のTdPの発生に関する臨床データと比較したところ、感度や特異度・正確性は80%以上という非常に高い値が得られました。従って、ヒトiPS細胞由来心筋細胞はヒトの心臓に極めて近い薬理作用を示し、ヒトiPS細胞技術を活用した安全性薬理試験の可能性が示されました。
また、近年大きな問題となっている抗がん剤による心毒性についてもヒトiPS細胞由来心筋細胞による収縮評価などが有用な試験法として活用できる可能性が考えられ、ヒト特異的な心筋収縮評価法の構築に向けてFDA(米国食品医薬品局)と議論を行っています。

中枢神経と肝臓の新たな評価方法も研究
我々は、心臓と並んで有害作用の多い神経と肝臓についても試験法を確立すべく、評価法の開発を進めているところです。
医薬品候補化合物の中枢神経系への影響は非常に重要で、中枢神経系は臨床になって初めて判明する副作用が多いというデータがあります。これまで齧歯類の行動薬理試験に依存していましたが、これをヒトiPS細胞の試験に代替して非臨床の段階から臨床試験で起こりうる副作用を予測することができれば、被験者の安全性の確保、研究開発の効率化などが期待されます。
また、重度の肝障害が原因となり安全性の面からグローバル市場から撤退した医薬品も多いため、ヒトiPS細胞由来肝臓細胞の応用が期待されています。特に、重度肝障害の進展予後については経験則(Hy's Law)に基づいて診断されていますが、重度肝障害の肝臓で見られる胆汁のうっ滞がヒトiPS細胞由来肝臓細胞でも同じように見られることから、胆汁の排泄能を指標にした肝障害試験法の確立が期待されています。
国際協調
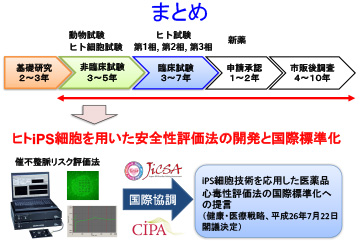
試験法に発展させるには国際協調が非常に重要なポイントとなります。日本だけで試験法を作って医薬品の評価をしても、世界で使ってもらえなければ本当の意味で標準化とは言えません。全てプロトコルやデータなどを取り終えてから海外に情報を提供しても、そのままでは使ってもらえずガラパゴス化することが考えられます。我々は、海外の研究者と協力体制を確立して、早い段階から実験プロトコルや化合物のデータシェアリングを行い、本当に使えそうだという感触を共有したうえでバリデーションに進む戦略をとって、国際標準化に向けた議論を重ねています。
これまで我々から米国のコンソーシアムであるCiPA(Comprehensive in vitro Proarrhythmia Assay)にプロトコルを提案し、予備データなどの共有を行ってきた結果、現在はコード化した化合物を用いた国際検証試験に発展しています。国際検証試験は米国科学雑誌「Science」に取り上げられるなど非常に注目も高く、国際標準化に向けて着実に進んでいます。
以上のように、地道な作業を一つひとつ積み重ねながら安全な薬を生み出すためのレギュラトリーサイエンスを推進するとともに、国際的なルールづくりに積極的に取り組み、ヒトiPS細胞を使った試験法が新しい安全性薬理試験として実用化することを目指します。
創薬における「死の谷」を克服するための日本発の「ヒト試験系」の臨床試験として、アカデミアはもちろん製薬会社からもヒトiPS細胞による安全性評価法への関心は非常に高く、国際標準化に向けて期待が高まっており、来場の方々は熱心に聞き入っていました。
最終更新日 平成29年10月17日