全胞状奇胎の原因を探る細胞モデルを作製―母体を絨毛がんから守るために―
プレスリリース
国立大学法人東北大学大学院医学系研究科
国立大学法人東北大学病院
国立研究開発法人日本医療研究開発機構
発表のポイント
- 全胞状奇胎注1とは子宮内で異常な受精卵が増殖したものであり、増殖が進行すると高頻度で絨毛(じゅうもう)がん注2を発生する。
- 本研究では、ヒトの全胞状奇胎より胎盤幹細胞(TSmole細胞)注3株を世界で初めて作製することに成功した。
- TSmole細胞注4株は、全胞状奇胎から絨毛がんが発生する仕組みを明らかにし、胞状奇胎の診断や病態の解明、治療法の開発に役立つと期待される。
概要
東北大学大学院医学系研究科情報遺伝学分野の高橋聡太(たかはし そうた) 大学院生、岡江寛明(おかえ ひろあき)准教授、有馬隆博(ありま たかひろ)教授のグループは、ヒト全胞状奇胎由来胎盤幹細胞(TSmole細胞)株の作製に世界で初めて成功しました。
全胞状奇胎は、受精卵から卵子由来の核が消失し、精子由来の核のみが増えていく異常妊娠の一つです。全胞状奇胎の増殖が進行すると絨毛がんなどの悪性腫瘍が高い頻度で発生します。これまで、全胞状奇胎の良い実験モデルが存在しなかったことから、全胞状奇胎がどのような遺伝子の働きによって増殖するのか十分には明らかになっていませんでした。本研究では、ヒトの全胞状奇胎に由来するTSmole細胞株を世界で初めて作製することに成功しました。通常の細胞では細胞密度が高くなると増殖が止まりますが、TSmole細胞株では細胞密度が高くても増殖が止まり難くなっており、このことが絨毛がんの発生を引き起こしている可能性が示唆されます。TSmole細胞株は、全胞状奇胎の診断や病態の解明、さらには治療法の開発に役立つと期待されます。また、全胞状奇胎から絨毛がんが発生する仕組みを研究する上で有用であると期待されます。
本成果は、2019年12月2日(月)午後3時(米国東部時間、日本時間12月3日(火)午前5時)Proceedings of the National Academy of Sciences of the United States of America(PNAS)に掲載されます。
研究内容
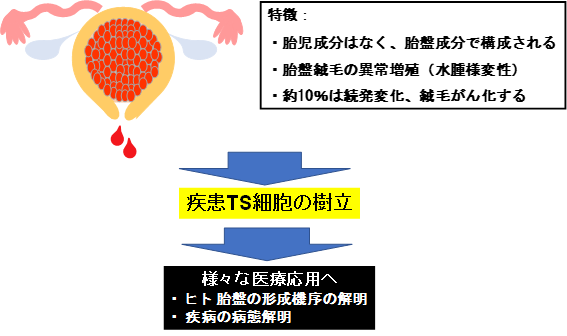
全胞状奇胎は、受精卵から卵子由来の核が消失することによって起こる異常妊娠の一つであり、胎盤を作る主な細胞である栄養膜細胞注5が異常に増殖するという特徴を持ちます。全胞状奇胎のおよそ10% は、侵入奇胎注6や絨毛がんといった悪性腫瘍に移行することが知られており、臨床上の重大な問題になっています。
通常、ヒトの体の細胞は母親および父親由来の遺伝子を一セットずつ持っており、多くの遺伝子は母親および父親由来の遺伝子の両方が働きます。しかし、一部の遺伝子は、母親由来もしくは父親由来の遺伝子のみが働くことが知られています。この現象はゲノム刷り込み(ゲノムインプリンティング)と呼ばれ、ヒトには100個以上のインプリント遺伝子注7が存在することが分かっています。全胞状奇胎の発症には、これらインプリント遺伝子の異常が大きく関わっていると考えられていますが、ヒトの栄養膜細胞の培養が困難であったことから、どのインプリント遺伝子が、どのような仕組みで全胞状奇胎を引き起こしているのか、これまで不明のままでした。
本研究では、当研究室で確立したヒト胎盤栄養膜幹(Trophoblast Stem:TS)細胞の培養技術を利用し、ヒト患者の全胞状奇胎の組織からTSmole細胞株を作製することに成功しました(図1)。健常人由来の正常なTS細胞株とTSmole細胞株の遺伝子の発現を網羅的に比較したところ、大部分の遺伝子の発現パターンは同等でしたが、TSmole細胞株ではインプリント遺伝子の異常な発現が観察されました。インプリント遺伝子の働きは、特定のDNA領域(アレル特異的メチル化領域)に、メチル化という目印(DNAメチル化)が付くことによって制御されています。このアレル特異的メチル化領域注8のDNAメチル化を解析した結果、TSmole細胞株では、ほとんどの領域で目印付くのは父親由来であることが分かりました。
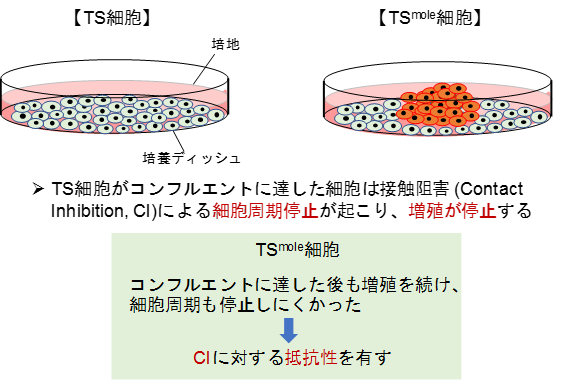
全胞状奇胎では細胞が異常に増殖することから、TSmole細胞株はTS細胞株より早く増殖することが予想されましたが、通常の培養条件では細胞の増殖速度に差は見られませんでした。臨床的な研究から、体内で全胞状奇胎の栄養膜細胞は健常人の正常な栄養膜細胞に比べ、重なって増殖する傾向があることが報告されていました。そこで、高い細胞密度で細胞の増殖を調べた結果、TSmole細胞株はTS細胞株よりもよく増殖することが分かりました(図2)。興味深いことに、TS細胞株では、母親由来の遺伝子のみが働くインプリント遺伝子の一つであるp57KIP2遺伝子(p57KIP2)の発現が、細胞密度が高くなるに従って上昇しましたが、TSmole細胞株ではp57KIP2はほとんど発現していませんでした。p57KIP2は細胞の増殖を抑える機能があること、TSmole細胞株においてp57KIP2を強制的に機能させると細胞の増殖が止まること、p57KIP2を破壊したTS細胞株は高い細胞密度でも増殖が止まらないことから、p57KIP2の機能の抑制が、TSmole細胞株での増殖異常の原因であることが明らかになりました。p57KIP2の発現抑制は、絨毛がんのみならず、多くの成人がんにおいても報告されています。よって、本研究で明らかとなったp57KIP2による増殖抑制の仕組みは、多様ながんの発生の理解につながる可能性があります。
本研究は、文部科学省 科学研究費補助金 新学術領域研究(研究領域提案型)における「全能性プログラム」における研究課題「着床前胚に由来する幹細胞を用いた全能性の再構築」(研究代表者:岡江寛明)、国立研究開発法人 日本医療研究開発機構(AMED)の「再生医療実現拠点ネットワークプログラム」における研究開発課題「再生医療等に用いるヒト胎盤由来幹細胞の細胞特性の解明」(研究代表者:岡江寛明)、国立研究開発法人 日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「エピゲノム研究に基づく診断・治療へ向けた新技術の創出」における「生殖発生にかかわる細胞のエピゲノム解析基盤研究」(研究開発代表者:佐々木裕之の研究開発分担者:有馬隆博)および国立研究開発法人 日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「健康・医療の向上に向けた早期ライフステージにおける生命現象の解明」における研究開発課題「ヒト胎盤の発生・分化に関する理解と臓器チップモデルの作製」(研究開発代表者:有馬隆博)により、行われました。
用語説明
- 注1 全胞状奇胎:
- 精子と卵子の受精の異常によって起こる異常妊娠のひとつ。卵子由来の核(DNA)が消失し、精子由来の核のみからなる受精卵より発生する。胎児の発育はみられない。
- 注2 絨毛がん:
- 胎盤を作る主な細胞である栄養膜細胞ががん化したもの。
- 注3 胎盤幹細胞(TS細胞):
- 全ての栄養膜細胞の元となる細胞。
- 注4 TSmole細胞:
- 全胞状奇胎由来のTS細胞。
- 注5 栄養膜細胞:
- 胎盤を作る主な細胞で、妊娠を維持するために必要なホルモンの産生や、胎児と母体との間の栄養やガスの交換を行う。
- 注6 侵入奇胎:
- 胞状奇胎が周りの子宮組織に拡がることによってできる腫瘍。
- 注7 インプリント遺伝子:
- 父親由来または、母親由来の対立遺伝子(アリル)のみの遺伝子発現を示す。
- 注8 アレル特異的メチル化領域:
- インプリント遺伝子の調節は、この領域のDNAメチル化によって制御されている。
論文題目
- Title:
- Loss of p57KIP2 expression confers resistance to contact inhibition in human androgenetic trophoblast stem cells
- Authors:
- Sota Takahashi, Hiroaki Okae, Norio Kobayashi, Akane Kitamura, Kanako Kumada, Nobuo Yaegashi, Takahiro Arima
- 日本語タイトル:
- p57KIP2はヒト胎盤幹細胞において接触阻害を制御する
- 著者:
- 高橋聡太、岡江寛明、小林記緒、北村茜、熊田佳那子、八重樫伸生、有馬隆博
- 雑誌名:
- Proceedings of the National Academy of Sciences of the United States of America
- DOI:
- 10.1073/pnas.1916019116
お問い合わせ先
研究に関すること
東北大学大学院医学系研究科情報遺伝学分野
教授 有馬 隆博(ありま たかひろ)
電話番号:022-717-7844
Eメール:tarima"AT"med.tohoku.ac.jp
取材に関すること
東北大学大学院医学系研究科・医学部広報室
電話番号:022-717-7891
FAX番号:022-717-8187
Eメール:pr-office"AT"med.tohoku.ac.jp
AMED 事業に関するお問い合わせ先
再生医療実現拠点ネットワークプログラム
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 再生医療研究課
電話番号:03-6870-2220
Eメール:saisei"AT"amed.go.jp
革新的先端研究開発支援事業(AMED-CREST)
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
電話番号:03-6870-2224
Eメール:kenkyuk-ask"AT"amed.go.jp
※Eメールは上記アドレス"AT"の部分を@に変えてください。
関連リンク
掲載日 令和元年12月3日
最終更新日 令和元年12月3日


