水溶性化合物による組織透明化の化学―包括的ケミカルプロファイリングに基づく化学的原理の体系化―
プレスリリース
理化学研究所
東京大学
新潟大学
日本医療研究開発機構
理化学研究所(理研)生命機能科学研究センター合成生物学チームの上田泰己チームリーダー(東京大学大学院医学系研究科機能生物学専攻システムズ薬理学教授)、新潟大学脳研究所システム脳病態学分野の田井中一貴特任教授、東京大学大学院医学系研究科機能生物学専攻システムズ薬理学の村上達哉日本学術振興会特別研究員らの共同研究グループは、水溶性化合物を用いた組織透明化の化学的原理の体系化に向けて、求められる透明化パラメータ(脱脂・脱色・屈折率調整・脱灰)[1]の包括的なプロファイリングに基づいた合理的手法を開発しました。
本研究成果により、ヒト臓器全細胞解析に向けて、従来の偶発的発見に依存した透明化試薬の開発戦略から、化学的原理に基づく合理的な開発戦略へのパラダイムシフトが期待できます。
今回、共同研究グループは、それぞれのパラメータに対して約1,600種類の水溶性化合物の「包括的なケミカルプロファイリング」を実施しました。その結果、①脱脂には塩を含まないオクタノール/水分配係数(logP)[2]の高いアミン(脂溶性アミンおよびアミノアルコールなど)が効果的であること、②脱色にはN-アルキルイミダゾールが効果的であること、③屈折率調整には芳香族アミドが効果的であること、④脱灰にはリン酸カルシウムのリン酸イオンのプロトン化(水素付加)が重要であることを見いだしました。さらに、各パラメータにおいて最適化されたケミカルカクテルを統合した一連の新しい「CUBIC[3]」プロトコール(手順)を開発することで、マウスの各種臓器および骨を含むマウス全身、ヒト組織を含む大きな霊長類サンプルの高度な透明化に成功しました。
本研究は、米国の科学雑誌『Cell Reports』オンライン版(8月21日付け:日本時間8月22日)に掲載されます。
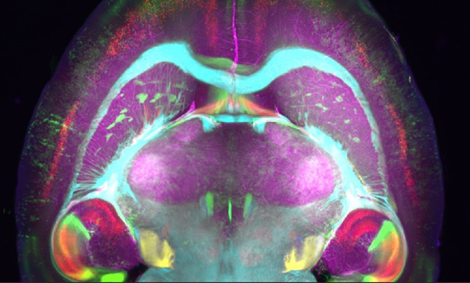
図 マウス全脳遺伝子発現状況の一細胞解像度の比較観察
※共同研究グループ
理化学研究所 生命機能科学研究センター
合成生物学チーム
チームリーダー 上田 泰己(うえだ ひろき)
(東京大学大学院 医学系研究科 機能生物学専攻 システムズ薬理学 教授)
無細胞タンパク質合成研究ユニット
ユニットリーダー 清水 義宏(しみず よしひろ)
新潟大学 脳研究所
システム脳病態学分野
特任教授 田井中 一貴(たいなか かずき)
病理学分野
教授 柿田 明美(かきた あきよし)
動物資源開発研究分野
教授 笹岡 俊邦(ささおか としくに)
東京大学大学院 医学系研究科
機能生物学専攻 システムズ薬理学
日本学術振興会特別研究員 村上 達哉(むらかみ たつや)
病因・病理学専攻 人体病理学・病理診断学
教授 深山 正久(ふかやま まさし)
病因・病理学専攻 分子病理学
教授 宮園 浩平(みやぞの こうへい)
疾患生命工学センター 構造生理学部門
教授 河西 春郎(かさい はるお)
京都大学大学院 医学研究科 医学専攻 高次脳科学講座 神経生物学
教授 伊佐 正(いさ ただし)
大阪大学大学院 医学系研究科 病態病理学講座
教授 森井 英一(もりい えいいち)
福島県立医科大学 生体情報伝達研究所 生体機能研究部門
教授 小林 和人(こばやし かずと)
日本大学 医学部 細胞分子薬理学部門
特任教授 飯野 正光(いいの まさみつ)
慶應義塾大学 医学部 精神・神経科学教室
教授 田中 謙二(たなか けんじ)
北海道大学 遺伝子病制御研究所・大学院医学研究科 分子神経免疫学分野
教授 村上 正晃(むらかみ まさあき)
群馬大学 生体調節研究所 脳病態制御分野
教授 林(高木)朗子(はやし(たかぎ)あきこ)
※研究支援
本研究は、日本医療研究開発機構(AMED)「革新的技術による脳機能ネットワーク全容解明プロジェクト」、「革新的バイオ医薬品創出基盤技術開発事業」、「革新的先端研究開発支援事業(AMED-CREST)」、「感染症研究革新イニシアティブ(J-PRIDE)」、および日本学術振興会(JSPS)「世界トップレベル研究拠点プログラム(WPI)」、科学研究費補助金基盤研究S「哺乳類生体リズム振動体の設計(研究代表者:上田泰己)」、基盤研究B「ヒト脳組織特異的染色による先進的3D神経病理学の確立(研究代表者:田井中一貴)」、新学術領域研究(研究領域提案型)「3D免疫染色によるタンパク質の老化基盤の解析(研究代表者:田井中一貴)」、民間研究助成(公益財団法人内藤記念科学振興財団、公益財団法人細胞科学研究財団、公益財団法人東京生化学研究会、公益財団法人ノバルティス科学振興財団)などの支援を受けて行われました。
背景
19世紀後半にドイツの解剖学者であるヴェルナー・シュパルテホルツが世界で初めて組織透明化技術の開発に着手して以来、さまざまな有機溶剤(例:欧州のBABB法、DISCO法)による透明化技術が開発されました。また、水溶性化合物による透明化試薬の開発にも長い歴史があり、1990年代にロシアのヴァレリー・ツーチンらによって糖やX線造影剤などが用いられた後、近年さまざまな透明化技術(例:日本のScale法、SeeDB法、CUBIC法、米国のCLARITY法)が開発されました。
これまでに生物の組織を透明化するために、どのような光学的性質(光の散乱、屈折、吸収)を実現すればよいかという物理学的な理論体系は確立されました。しかし、開発されたさまざまな透明化試薬がどのような原理で組織の透明化に寄与するのか、組織を透明化するのに求められる重要な化学的性質は何かといった単純かつ根本的な化学的疑問に答えることはできていませんでした。
これは、従来の透明化技術の開発戦略が、偶発的な発見および小規模な化合物群の場当たり的な組み合わせによる最適化に依存しており、化学種の多様性を網羅できていないこと、個々の化合物が持つ固有の化学的性質が考慮されていないことに起因しています。今後、生物学・医学における究極の課題であるヒト臓器全細胞解析に向けて、組織透明化技術がさらなる飛躍・発展を遂げるためには、学術的に確かな化学的理論の構築に資する、包括的アプローチに基づく開発戦略が望まれていました。
研究手法と成果
共同研究グループは、安全性を考慮して有機溶剤ではなく水溶性化合物に着目し、ハイスループットなスクリーニング系に基づく「包括的ケミカルプロファイリング」を考案しました(図1)。上田チームリーダーらが2014年に発表したマウス全脳透明化/3次元的イメージング技術「CUBIC」において開発した組織の「脱脂」効率の評価系となるin vitro(試験管内)スクリーニング手法注1)を参考に、組織透明化に求められるパラメータである「脱色」、「屈折率調整」、「脱灰」について、同様のスクリーニング手法を開発しました。そして、水溶性が期待される約1,600種類の化合物の水溶液を調整し、その手法でスクリーニングしました。それぞれの化合物は、特有の官能基、溶解度パラメータ、構造、幾何学的パラメータを含んでいます。スクリーニング結果に対して、20種類以上のケミカルパラメータをプロファイリングすることで、脱脂・脱色・屈折率調整・脱灰において重要な化学的性質が明らかになりました。
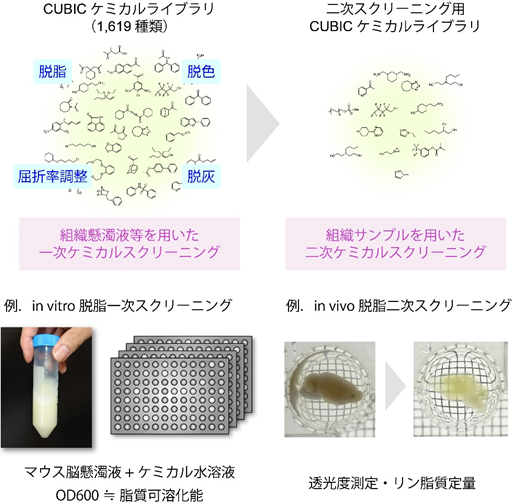
図1 組織透明化に向けた水溶性化合物の「包括的ケミカルプロファイリング」
まず、「脱脂」の一次スクリーニングでは官能基プロファイリングの結果、「脂溶性アミンとアミノアルコール・アミノエーテル」が有意に高い脂質可溶性を示しました(図2a))。これらのアミンに対して、どのケミカルパラメータが脂質可溶化能に寄与しているかを調べるために、多変量回帰分析[4]を行った結果、化合物の疎水性の指標である「オクタノール/水分配係数(logP)」が最も高い寄与度を示すことが分かりました(図2b))。次に、マウス脳を用いたニ次スクリーニングの結果、これらアミンのlogPと最終的な組織の透明度に正の相関関係があることが示され、一次スクリーニングで得られた仮説の妥当性が確認されました(図2c))。
従来のCUBICではアミノアルコールであるクアドロールが含まれているにもかかわらず、膨潤活性の高い尿素を必要としていましたが、これはクアドロールのlogP値が低い、つまり組織浸透性が低いことに起因していることが示されました。logP値の高い「1,3-ビスアミノメチルシクロヘキサン」や「N-ブチルジエタノールアミン」を用いることで、尿素を必要としないシンプルな脱脂カクテルの開発が可能になりました。
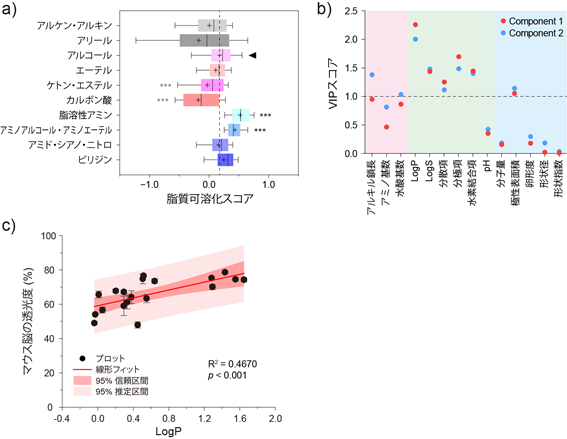
図2 脱脂における包括的ケミカルプロファイリング
「脱色」の一次スクリーニングではマウス血液を用いた官能基プロファイリングの結果、「N-アルキルイミダゾール」が有意に高い脱色活性を示しました(図3a))。マウス脾臓を用いたニ次スクリーニングの結果、N-アルキルイミダゾールが実際の臓器においても高い脱色活性を示すことが確認されました(図3b))。一般臓器に最も潤沢に含まれている吸収成分は、ヘモグロビンやミオグロビンに含まれるヘム[5]です。N-アルキルイミダゾールは、ヘムの配位子であるヒスチジン残基と類似の構造を持っていることから、非共有結合を介したヘムの高効率な溶出に寄与していると予想されます。
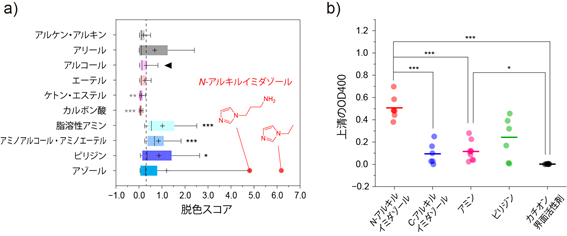
図3 脱色における包括的ケミカルプロファイリング
組織透明化の最終工程は、組織サンプルの屈折率の均一化です。組織サンプルは水よりも高い屈折率を持つため、屈折率の高い媒体を調整する必要があります。「屈折率調整」の一次スクリーニングでは、官能基プロファイリングの結果、芳香族を持つ化合物が有意に高い屈折率を示しました(図4a)。マウス肺を用いて高い屈折率・水溶性を示す化合物グループに対して多変量回帰分析を行った結果、アミド基が最も高い寄与度を示すことが分かりました(図4b)。このことから、「芳香族かつアミド基を持つ化合物」が最も屈折率調整剤に適していることが示されました。
これまで水溶性の屈折率調整剤において、イオヘキソールに代表されるX線造影剤が高い透明度を示すことから、組織透明化試薬 FocusClearTMを筆頭にX線造影剤を用いた種々の派生屈折率調整剤(例:RIMS、SeeDB2、PROTOSなど)が開発されました。しかし、一連のX線造影剤は高コストであるため、同等の透明化効率を示す安価な化合物の探索が求められてきました。今回の成果により、X線造影剤と同様の芳香族アミドであり、かつ安価な水溶性ビタミンの「ニコチンアミド」、鎮痛解熱薬である「アンチピリン」の発見に至りました。
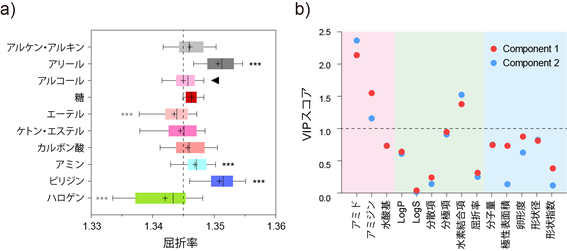
図4 屈折率調整における包括的ケミカルプロファイリング
さらに、「脱灰」においては、骨の主成分であるハイドロキシアパタイト(HAp)を用いたスクリーニング系を構築し、中性条件下で脱灰効果のあるキレート剤[6]のエチレンジアミン四酢酸(EDTA)[6]に着目しました。一般的に、脱灰は強酸性条件下において高効率に進行しますが、この条件は、その他の透明化条件や蛍光タンパク質のシグナル保持に適さないからです。EDTAは、pHが高くなるほどカルシウムイオン(Ca2+)に対するキレート能が高くなることが知られていますが、その予想に反してEDTA(EDTA-水酸化ナトリウム)の脱灰効果はpHが高くなるにつれて、急激に減弱することが分かりました(図5)。HApの溶解過程において、リン酸カルシウムのリン酸イオン(PO42-)のプロトン化(水素付加)の促進がHApの溶解に大きく寄与することが知られています。このことから、EDTAによる脱灰過程において、Ca2+のキレートよりも「PO42-のプロトン化」の方が大きく寄与することが示されました。
また、水酸化ナトリウムではなく、「N-ブチルジエタノールアミン」を用いてEDTAのpH調整を行った結果、弱塩基条件下でも高効率な脱灰効果を示すことが分かりました(図5)。このことから、「EDTAと有機塩基の組み合わせ」による脱灰カクテルを開発しました。
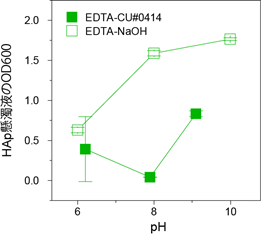
図5 脱灰における包括的ケミカルプロファイリング
最後に、包括的ケミカルプロファイリングに基づく合理的な組織透明化技術の開発戦略を考案しました(図6)。同定された化合物群を用いて、さらなる組み合わせ効果を検証することで最適な6種類のケミカルカクテルを開発しました。また、これらのケミカルカクテルを目的に応じて組み合わせることで一連の新しいCUBICプロトコール(手順、ProtocolⅠ、Ⅱ、Ⅲ、Ⅳ)を開発しました。これらの開発戦略は、開発者の目的に応じて自在に調整可能な合理的開発戦略になっています。
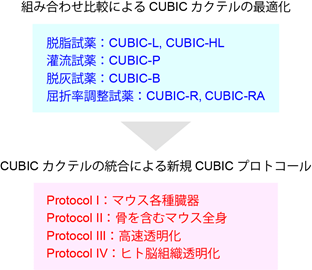
図6 包括的ケミカルプロファイリングに基づく組織透明化技術の開発戦略
そして、これらの四つの新しいプロトコールにより、マウスの各種臓器、および10 cm3以上の大きなヒト組織(肺と脳)の高度な透明化に成功しました(図7)。また、蛍光タンパク質に適用可能なマウス臓器用CUBIC ProtocolⅠを用いて、種々のレポーターマウス[7]の全脳イメージングを行い、各全脳画像を位置合わせし可視化することで、遺伝子発現の空間的差異を一細胞解像度で正確に比較することが可能になりました(図8)。

図7 新しいCUBICプロトコールによる組織透明化の応用例
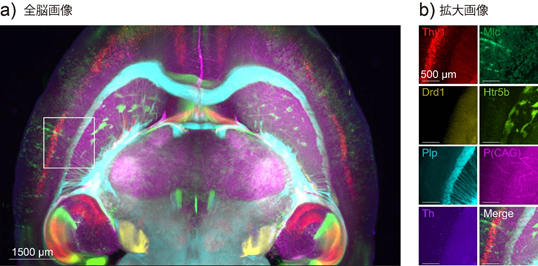
図8 マウス全脳遺伝子発現状況の一細胞解像度の比較観察
今後の期待
本研究は、組織透明化の化学的原理を体系化し、それぞれのパラメータに対して重要な化学的性質の抽出に成功したという意味で、組織化学的に極めて意義の大きな成果であると考えられます。生物学・医学において究極の課題であるヒト臓器の全細胞解析を実現するためには、より大きな組織を高度に透明化する必要があります。今後さらに透明化技術を飛躍・発展させるために、本研究を基盤とした化学的根拠の明確なアプローチによる合理的な開発戦略は、これからの新たなスタンダードとなることが期待できます。
論文情報
- タイトル
- Chemical Landscape for Tissue Clearing based on Hydrophilic Reagents.
- 著者名
- Kazuki Tainaka, Tatsuya C. Murakami, Etsuo A. Susaki, Chika Shimizu, Rie Saito, Kei Takahashi, Akiko Hayashi-Takagi, Hiroshi Sekiya, Yasunobu Arima, Satoshi Nojima, Masako Ikemura, Tetsuo Ushiku, Yoshihiro Shimizu, Masaaki Murakami, Kenji F. Tanaka, Masamitsu Iino, Haruo Kasai, Toshikuni Sasaoka, Kazuto Kobayashi, Kohei Miyazono, Eiichi Morii, Tadashi Isa, Masashi Fukayama, Akiyoshi Kakita and Hiroki R. Ueda
- 雑誌
- Cell Reports
- DOI
- 10.1016/j.celrep.2018.07.056
補足説明
- [1] 透明化パラメータ(脱脂・脱色・屈折率調整・脱灰)
- 組織透明化を実現するためには、組織を通過する光の散乱および吸収を解消することが重要であると考えられている。光の散乱は組織内の構成成分の屈折率差に起因しており、外来の媒体による組織内の屈折率の均一化(屈折率調整)の際に、組織中の脂質の除去(脱脂)および骨の除去(脱灰)が求められる。また、光の吸収は組織内に含まれるヘムを代表とする内因性色素に起因しており、色素の除去(脱色)が求められる。本研究では、組織透明化を実現するために、これらの化学的性質を独立したパラメータとして分離し、それぞれに効果的な化合物を探索するための包括的ケミカルプロファイリングを行った。
- [2] オクタノール/水分配係数(logP)
- 化合物をオクタノールと水の二つの溶媒相中に加えて平衡状態に達した際に、ニつの溶媒相における化合物の濃度比を示す。化合物の疎水性を示す指標となり、医薬品の吸収効率や環境汚染物質の土壌や地下水への移動予測などに用いられる。
- [3] CUBIC
- 臓器透明化と3次元イメージングのための化合物の混合溶液とコンピュータを用いた画像解析。本研究では、理研が2011年に開発した透明化試薬「Scale(スケール)」に着想を得て、尿素・アミノアルコール・界面活性剤からなる脱脂カクテルScaleCUBIC-1、およびショ糖・尿素・アミノアルコール・界面活性剤からなる屈折率調整カクテルScaleCUBIC-2を開発した。サンプルを試薬に浸すだけの効率的で再現性の良い方法で、複数のサンプルを同等な条件で高度に透明化することが可能となり、1細胞解像度の全臓器蛍光イメージングと情報科学的解析によるサンプル間のシグナル比較法が実現した。CUBICは、Clear, Unobstructed Brain and Body Imaging Cocktails and Computational analysisの略。
- [4] 多変量回帰分析
- 注目すべき目的変数を、多数の説明変数により回帰し解析する手法である。目的変数が単一の説明変数のみで説明できる場合には、目的変数と説明変数の関係性を比較的簡単に明らかにすることができる。しかし、複数の説明変数が存在する場合はそれぞれの説明変数間の相関関係(多重共線性)に考慮をする必要がある。本研究では、多重共線性の問題を回避するために多変量回帰分析の中でも特に部分的最小二乗回帰と呼ばれる解析手法を用いた。その上で説明変数の寄与率を算出した。
- [5] ヘム
- 鉄イオンを中心にポルフィリンという環状の有機化合物が取り囲んだ物質。生体内ではヘモグロビン、ミオグロビン、異物薬物代謝酵素(シトクロムP450)、ペルオキシダーゼ、電子伝達系酵素をはじめとするさまざまなタンパク質の補欠分子族(酵素の活性に不可欠な非タンパク質性の物質)として機能している。
- [6] キレート剤、エチレンジアミン四酢酸(EDTA)
- 二つ以上の配位原子を持ち金属イオンに結合する能力を持つ多座配位子をキレート剤と呼ぶ。キレート(chelate)はギリシア語のカニのハサミから出た語で、配位子と金属イオンの間に環構造が形成されることから用いられるようになった。配位座の化学的性質の違いにより、金属イオンに対する特異性が異なる。エチレンジアミン四酢酸は、2個の窒素原子、4個の酸素原子で六座配位子として働くキレート剤である。
- [7] レポーターマウス
- 各種のイメージング手法などを用いて遺伝子発現をモニターできるマウス。
発表者・機関窓口
発表者
理化学研究所 生命機能科学研究センター
合成生物学チーム
チームリーダー 上田 泰己(うえだ ひろき)
(東京大学大学院医学系研究科 機能生物学専攻 システムズ薬理学 教授)
TEL:06-6105-5241 FAX:06-6105-5241
E-mail:uedah-tky[at]umin.ac.jp
新潟大学 脳研究所 生命科学リソース研究センター
システム脳病態学分野
特任教授 田井中 一貴(たいなか かずき)
TEL:025-227-0900
E-mail:kztainaka[at]bri.niigata-u.ac.jp
東京大学大学院 医学系研究科
機能生物学専攻 システムズ薬理学
日本学術振興会特別研究員 村上 達哉(むらかみ たつや)
TEL:03-5841-3415 FAX:03-5841-3418
E-mail:murakami_t[at]m.u-tokyo.ac.jp
機関窓口
理化学研究所 広報室 報道担当
TEL:048-467-9272 FAX:048-462-4715
E-mail:ex-press[at]riken.jp
東京大学 医学部 総務係
TEL:03-5841-3304 FAX:03-5841-8585
E-mail:ishomu[at]m.u-tokyo.ac.jp
新潟大学 脳研究所 事務室 共同利用係
TEL:025-227-0565 FAX:025-227-0507
E-mail:noukyoudo[at]adm.niigata-u.ac.jp
AMED事業に関するお問い合わせ先
革新的バイオ医薬品創出基盤技術開発事業
日本医療研究開発機構(AMED) 創薬戦略部 医薬品研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2219 FAX:03-6870-2244
E-mail:kaku-bio27[at]amed.go.jp
感染症研究革新イニシアティブ(J-PRIDE)
日本医療研究開発機構(AMED) 戦略推進部 感染症研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2225
E-mail:kansen[at]amed.go.jp
革新的技術による脳機能ネットワーク全容解明プロジェクト
日本医療研究開発機構(AMED) 戦略推進部 脳と心の研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2222
E-mail:brain-pm[at]amed.go.jp
革新的先端研究開発支援事業(AMED-CREST)
日本医療研究開発機構(AMED) 基盤研究事業部 研究企画課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2224
E-mail:kenkyuk-ask[at]amed.go.jp
※上記の[at]は@に置き換えてください。
関連リンク
掲載日 平成30年8月22日
最終更新日 平成30年8月22日


