アーカイブ 東京医科歯科大学 疾患バイオリソースセンター(TMDU BRC)

[取材協力]
TMDU 疾患バイオリソースセンター センター長 稲澤 譲治先生
TMDU 疾患バイオリソースセンター 疾患多様性研究部門 田中 敏博先生
TMDU 疾患バイオリソースセンター バイオバンク部門 特任助教 竹本 暁先生
がんを含む生活習慣病から難治性の希少疾患
そして、歯学領域の試料と臨床情報を一元管理
2013年に設立された東京医科歯科大学(TMDU)疾患バイオリソースセンター(BRC)は、全学を挙げての試料収集システムを組み、また臨床情報との紐付けを可能にしている。順調に滑り出したその運営の詳細と今後の課題を、BRCに携わる3名の研究者に聞いた。
個別化医療に向けての診断・治療・予防法を産学官連携で開発するハブとしてのバイオバンク
TMDU BRCは、TMDU内において、がんを含む生活習慣病および難治性疾患等の患者の臨床検体から採取した試料と、それに付随する臨床情報およびゲノム情報を一元的に管理するバイオバンク事業を行っている。平成24~27年度の文部科学省特別教育研究経費の研究課題「疾患バイオリソースセンター設置による産学官イノベーション推進研究拠点の形成」の研究費をもとに2013(平成25)年に設立された施設だ。
がんを含む生活習慣病および難治性疾患に対する画期的な診断・治療・予防法の開発、安心・安全な個別化医療の実現を大きな目標とするTMDUでは、基礎生命科学研究からトランスレーショナル研究、さらに実用化までを視野に入れた一貫性のある産学官連携研究の推進、そして、ゲノム情報に基づく個別化医療に対応できる医療人の育成に資するインフラとして機能するバイオバンクが求められていた。もともと医学部附属病院と歯学部附属病院には臨床情報や病理検体が蓄積されていたことに加え、難治疾患研究所ゲノム応用研究部門、骨や歯のゲノムに特化した硬組織疾患ゲノムセンター、さらには生命倫理研究センターといったゲノムやバイオバンクに関連する組織がすでに設置されており、BRCにはこれらのハブになるような機能を担えるという期待も高かった。来院した患者から得た試料・診断情報のコホートが基本だ。
附属病院を持つ大学に共通する課題ではあるが、TMDUでも大学内の個々の研究者が患者検体を集め、解析をし、データを抽出して、予防・診断・治療の方法を研究・開発してきた。しかし、それでは検体数が少なく、研究の価値が上がりにくい。また、研究が一段落した後や研究者が異動した後に検体が散逸してしまうこともよくある。「このような状態では検体を提供してくださった患者さんの気持ちに報いることができず、倫理的な問題も出てきます。そこで、バイオリソースとゲノム情報を大学の機関のものと位置づけて、医学・歯学領域の将来の研究利用のための包括的な同意(以下、包括同意)を得た状態で、臨床情報とともにBRC バイオバンクに集約・管理できるよう全体のシステムを構築しました。全学でこれを有効活用、大規模な研究にも利用できるようにしたのです」と稲澤 譲治BRCセンター長は話す。
医師の作業負担を軽減する電子カルテでのオーダーシステムと大学病院の強みを活かした試料採取に関わる外科医・病理医の連携
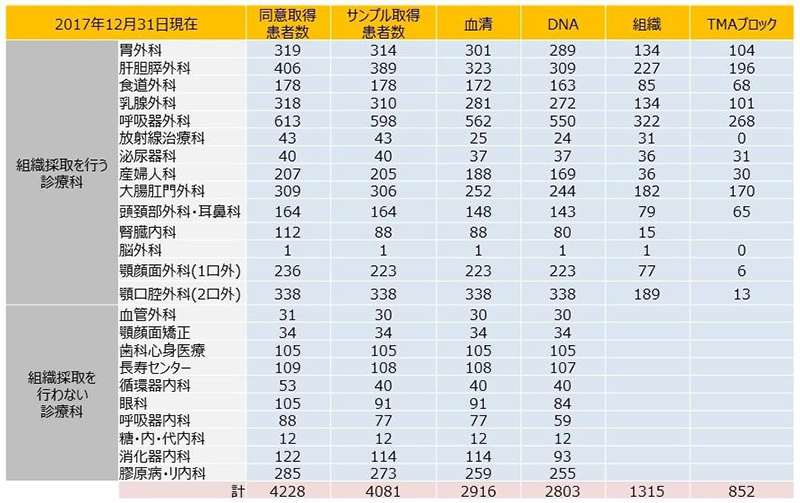
BRCでは現在、全血、血清、DNA、がんなどの病理組織(肺、乳腺、食道、胃、大腸、肝、胆膵、口腔) 、組織アレイ(TMA)ブロック などの試料と付随する臨床情報およびゲノム情報 を保存、提供している。稲澤センター長のもと、疾患多様性研究部門・3名、バイオバンク部門・8名、メディカルインフォーマティクス部門・2名、医療倫理部門・1名、客員教授・2名 計17名と運営自体はコンパクトな規模で行われている。その約2/3は、学部や学内センター職との併任。その体制が成り立つ要因は、全学を挙げた協力体制システムだ。「AMED『オーダーメイド医療実現プロジェクト』の第2・3期に渡る10年間参加し、その中でバイオバンクの重要さを、私自身が研究者として痛感したことが大きく影響しました。かつ、試料収集のシステムについて情報を見聞きすることができましたので、それを踏まえて本学ではどうすべきかを考えて、BRCでの形や全学での協力体制などを構想しました」と稲澤センター長は当時を振り返る。
その運営システムの大きな特徴の1つは、包括同意取得の有無や血液採取のオーダーを附属病院の電子カルテシステムに組み込み、個人情報を除いた電子カルテ情報を有効に活用している点だ。
がんを含む生活習慣病や難治性疾患などBRCが規定している疾患の患者には、まず臨床医が試料提供の包括同意を取る。同意の有無の結果は、電子カルテシステムの画面上にある記入欄をクリックするだけでよいため、臨床医の負担は少ない。検体からの試料採取から保存までの管理と情報管理室の運用を担うBRC バイオバンク部門の竹本 暁特任助教によると「これまでに臨床医が同意を取るのを忘れたケースは、ほとんどありません」と言う。また、稲澤センター長は、患者の皆さんは"自分の検体が役に立つのであれば"と非常に好意的で、これまでの同意撤回は10件以下であることに感謝をにじませた。 なお、各診療科独自の研究があれば、同時並行で包括同意を取ることになっている。
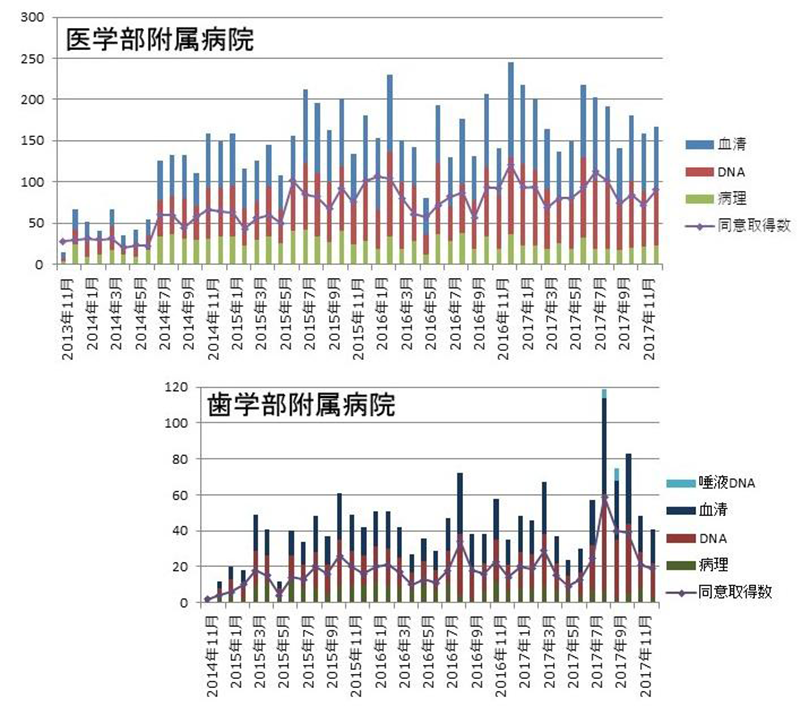
稲澤センター長らは、BRC開設前から医学部と歯学部に所属する臨床医に向けてバイオバンクの意義や包括同意の取り方を伝える説明会を50回以上開催している。この説明会に参加し登録しなければ、包括同意所得の権利と操作が認められないと言う。38の診療科から、すでに900人近いの学内の臨床医が参加、2017年12月末現在、登録医師数は370名、同意取得数は延べ4,228名と、右肩上がりだ。(図1・2)

電子カルテ上で、通常の採血とバイオバンク用の採血オーダーが同時にでき、臨床医の負担が少ない。採血は14ml(小中学生は7ml)で、検査部 採血室で通常の臨床検査と共通で行う。新しい血液試料が採取されるとBRCに連絡が行き、センター専任の技術員が取りに行く。これをBRCバイオリソーステクノロジー室で、同意文書確認後に発行される個人情報のない採血管用ラベルに貼り替えるなどの匿名化の処理、新しいサンプルID・チューブIDを付与した上でバーコード入力と血清分離とDNA抽出を行う。血清、DNAを各1.0ml、0.7mlのチューブに分注し 、血清は-150℃のフリーザーで、DNAは4℃のコールドルームにて保存する。(写真1・2)
手術や生検で採取した組織検体を、外科医と病理医が連携して扱うのも特徴的だ。検体は外科医が医学部附属病院 病理部門にあるマクロコントロール室に直接届け、それを病理医が肉眼で確認し、標本のトリミング、貼り付けを行った上で写真を撮影。病理診断に必要のない余剰検体(5mm~1cm角)を採取し、BRCの技術員による液体窒素での凍結処理後、病理IDを付与してBRCバイオリソース室の-150℃のフリーザーで保管する。「今後の利活用を考えて、試料からタンパク、RNA、DNA、ゲノムのすべてを採取できるように、樹脂で包埋する検体の保存方法 を導入して標準化しました」(稲澤センター長)手術件数と検体数はBRCのコンピューターで確認でき、手続きや検体に不備があったときにはトレースできるようになっている。

試料は、24時間体制の試料保存モニタリングシステムで管理され、管理画面から一覧でき、異常発生時にはアラートメールで管理者に通報される仕組みだ。
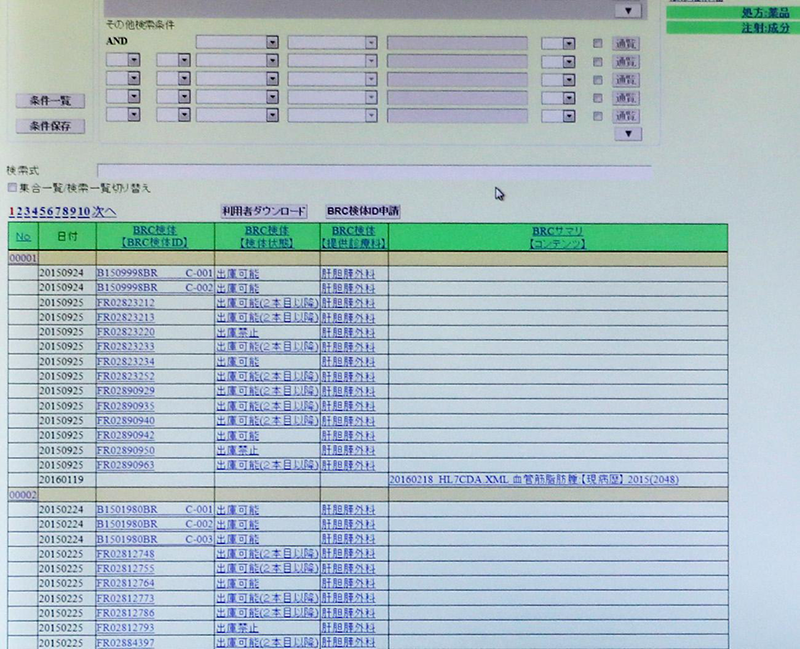
臨床情報との連結にも工夫を凝らした。「病院の電子カルテシステムの中の個人情報を抜いた臨床情報が毎日定時に定期更新されて、BRCのサーバーに送られてくるようになっています」(竹本特任助教)。最終的には、患者IDと試料固有のID、病理ID、臨床情報や検査番号とが紐付された状態で、BRCの診断情報・試料保管情報データベースに集約される。
これらの情報は、入室等に個人認証カードキーや独立設定キーなどを必要とする情報サーバー室内のPC端末でしか検索できない状態で、セキュリティを担保している。
歯学部附属病院では唾液を試料として収集

TMDUは歯学部附属病院を持つだけに、唾液という歯学特有の試料も集めている。同病院では一般の歯科では治療しにくい、比較的まれな疾患の診療も多いと言う。例えば顎口腔外科学では口腔の家族性腫瘍を研究しており、唾液のゲノムが有力な研究対象になるのだ。「もともと歯学部附属病院の医療スタッフや患者さんには採血はなじみがありません。当初、バイオバンクのシステムは医学部附属病院をメインに考えていましたが、歯学部附属病院の特徴を活かすには唾液がよい試料となりました」(稲澤センター長)。唾液の提供は、同意への患者意識のハードルも下がり、取りやすいと言う。
ただし、唾液中には口腔内の細菌が存在しているため、ゲノム解析の結果にも細菌のゲノム情報が反映されてしまう。「ヒトゲノムのみを扱う研究者にとっては役に立たないノイズですが、口腔内細菌叢と全身状態には相関があるとわかっているので、着眼点次第では興味深い解析ができます。医学部附属病院と歯学部附属病院の電子カルテは現時点では別々のシステムですが、患者IDが共通化されているので、例えば、歯周病の患者さんが循環器疾患になった場合、統合したデータとして扱うことができます」とBRC 疾患多様性研究部門の田中 敏博教授は話す。採取する唾液は2~10 mlほどだ。
がんを含む生活習慣病の診断・治療・予防に向けて子どもから大人まで、広報にも力を注ぐ
がんを含む生活習慣病予防のためには、健常者の診断、試料の入手も必要となる。ゲノム研究のコントロールとしても必要だ。BRCでは、TMDUの健診予防医学センターで健診を受けた、病気がないと判断される人にも包括同意を得て、一部の試料を採取している。理解の上で試料提供、包括同意取得のためにも、BRCが製作した患者や一般向けにWebサイトやパンフレットによる広報にも力を入れている。「Webサイトは試料を提供してくださった方々への報告でもあり、また、提供を考える方にも参考となります。今後、ゲノム医療が進むといっても、一般の方々に知識があってこそ、健康管理や行動変容が起こる。そういう意味で私たちはコミュニケーションツールを介して社会への啓発に努めています」と稲澤センター長は話す。
子ども向けのパンフレットも用意していると言う。「本学の小児科は非常に熱心に取り組んでいる。独自にサンプルを保存するシステムが、BRC開設以前からありました。なおかつ小児の場合は大量に何回も採血するわけになかなかいきませんね。少量でも非常にいい状態で試料を保存するということを手がけていました。その上で、(患者・医師ともに)無理のない範囲でと進めています」(稲澤センター長)。
プレシジョン・メディシンとレアディジーズに貢献するゲノム医療研究に向けて

プレシジョン・メディシン(精密医療、個別化医療)への対応も特徴的だ。「循環器領域においては罹患者の多いコモンディジーズとして、高齢者に多く発症する不整脈の一種である心房細動、あるいは心臓の血管が詰まる心筋梗塞が挙げられます。それらは、ゲノム上に存在する一塩基多型(Single Nucleotide Polymorphism:SNPs)から発症の危険度がわかります」と田中教授は説明する。これらを一人ひとりの健康管理に使ってもらおうというプロジェクトが東京医科歯科大学長寿・健康人生推進センターにて進行中である。
頻度が低い、稀な疾患として田中教授は、QT延長症候群に注目している。「耳慣れない疾患名かもしれませんが、不整脈の一種です。普段は症状がありませんが、不整脈が起きると、心臓がポンプの機能を果たさなくなって失神発作を起こす、あるいは突然死につながってしまう非常に危険な病気です。遺伝子の稀な変異が疾患の直接の原因です」10年ほど前に、この疾患の遺伝子検査が保険でカバーされるようになったと言う。また、現在判明している15の原因遺伝子のうち、主な3個のいずれに異常があるかによって薬の効きが異なること、同じ遺伝子の異常であっても変異の存在箇所によって予後が異なることが明らかになっている。「診療ガイドラインまでには至っていませんが、遺伝子情報を診療に活かす素地はでき上がっています」
遺伝子レベルでの研究成果を、診療に還元していこうとするモチベーションの高さがBRCから感じられる。
5年目で有償での分譲を開始製薬企業の臨床試験の分譲の条件が、発展の鍵
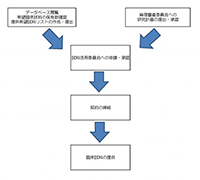
BRCでの分譲には、まずデータベースを閲覧した研究者が、研究内容や要望する試料を書いた申請書提出が必要だ。その際には、申請者やその他の関連する研究者の所属機関の倫理委員会の承認を得ていることが必須条件で、学内でも同様だ(図3参照)。それを踏まえて、外科医、病理医、産学連携研究センター関係者と多職種が構成するBRC内の試料活用委員会が研究の妥当性を検討する。試料活用委員会が承認した研究は、さらに要望された試料を提供した診療科や教室に照会され、その承諾を得るという手続きが行われる。これら申請から最終的な承諾、払い出し開始まで、約1~2か月かかると言う。研究の目的や計画が、その診療科や教室の研究と類似している場合は、分譲しないこともあり得る。
学内の研究者が分譲を求めて承認された場合、1本目は無料、2本目からは課金をする。「5年経って、ようやく今、有償での利用が始まりかけたところです。いい意味でのポジティブなスパイラルで回っていくことを期待しています」(稲澤センター長)。学内での利活用は、進みつつある。しかし、外部の研究者や企業での利用も推進したいが、まだ分譲したケースはない。
悩ましいのが製薬企業の臨床試験の扱いだ。個別化医療、プレシジョン・メディシン(精密医療)が求められる今、製薬企業は医薬品開発に遺伝子やゲノムの情報を組み込んで臨床試験を行っている。「グローバルな臨床試験では、製薬企業は当該臨床試験に利用するためだけでなく将来研究に利用するためのバイオバンクへの協力を求める場合があります。臨床試験は事前に医療機関の倫理委員会でその実施計画内容が審議され適正であると承認された後に実施されるます。勿論、医薬品医療機器総合機構(PMDA)もその内容を把握しています。一方で、当センターでは分譲の要件として研究計画を明らかにすることを求めていますが、新薬の開発研究を推進する製薬企業は具体的な研究計画を明かせないのが実状です。そして、具体的な研究計画が提示されなければ、バイオリソースを提供する側の機関の倫理委員会で承認を得ることも不可能です。そのため、例え難病の新薬開発という患者さんのためいのもなる研究にバイオリソースの提供が求められる場合であっても、製薬企業の開発研究には容易に協力できない状況です」(稲澤センター長)。また、国際的な臨床試験に参加できないと、新薬を使えるタイミングが遅くなり、それは患者には不利益となる。さらに、試料が活用されなければ、保存費用の負担も大きくなり、スペースも圧迫する。「活用されない、溜まるばかりの塩漬け状態ですと、物理的にもパンクするでしょう。そうなれば維持できない、過去のものは廃棄せざるを得なくなります」今後、ゲノムの研究がさらに進むと診療科や専門領域を超えた疾患の関連性がみられる可能性が高い。そうなれば、生活習慣病から難治性希少疾患や歯学領域までの試料と臨床情報を一元管理しているBRCの役割はますます大きくなる。「だからこそ、診療科を窓口にして集めた検体から得た試料と臨床情報はその診療科だけのものではなくて、大学全体のものであり、それを外部にも提供できるシステムの整備が重要です」と稲澤センター長はこのバイオバンクの設立の精神を強調した。

また、提供するだけサンプル数がない場合もある。産婦人科領域で、母胎血と胎児の関係を追う研究などでは、研究に使うだけの試料が足りず、その後、年単位で試料を収集し、十分な量が集まった段階で再度分譲の手続きに入った例もあったと言う。医薬品開発のターゲットが希少疾患である場合には試料の数が限られており、無限に出すことはできない。この点に関してBRCでは、非常にまれな疾患の試料は、最低限チューブ1本分の血清・DNAは10年以上保存すると決めている。ここに問題意識を持ち、近々の課題としてグローバルな展開を視野に1・2年の間に改善を目論んでいると稲澤センター長は語る。
これらは多くのバイオバンクが抱えている問題だ。「このままでは試料を提供してくださった患者さんたちに申し訳ない。現在、生命倫理研究センターや産学連携研究センターのメンバーを中心に、民間企業に倫理的にも社会的にも適正に試料が提供でき利用してもらえる方法を検討しながら、利活用推進を検討しているところです。恐らく1年以内にその新しい仕組みが発信できるのではないかと期待しています」(稲澤センター長)。
基礎の研究者と臨床の医師が手を組める組織づくりのために
BRCの試料収集が順調に進み、学内のプロジェクトとの連携が進んでいる理由として、稲澤センター長は、学長のガバナンス力と各医師や医療スタッフのマインドの高さを挙げる。「まず、学長をはじめ、理事会の理解や支援があること。この施設がオープンする前に、当時の学長が特別経費を付けてくれたことで施設整備だけでなく人員を配置でき、現学長は維持することに非常に注力してくれている。とても感謝しています。また、病理部門や外科、臨床検査部、医療情報部といった学内組織が積極的に携わってもらえることが(BRCの充実に)大きく貢献しています。最初の1年は持たれていた、"自分たちが使いたいがために試料を集めているのだろう"という誤解を解消して、今があります。竹本先生のように病院の人員である病理医がBRCへ派遣されているのも、その成果です」。大学病院の病理医であり、BRCと病理部門との連携を担う竹本特任助教は「これからの病理医は、形態だけではなく、遺伝子やゲノムも研究することが求められます。私もここに参画して、新しく研究を始めてみると本当に面白いのです」と自身の研究の展開を楽しんでいる様子だ。
何が大事かを個々に感じ取り、意識する人材が集えることは、間違えなくBRCの財産だ。
(取材日:2018年1月16日)
インタビュー映像
研究者経歴
稲澤 譲治(いなざわ じょうじ)
1956年、兵庫県生まれ。1982年に京都府立医科大学卒業。1991年に医学博士(京都府立医科大学)。1993年に同大学医学部 衛生学教室 講師、1996年に東京大学医科学研究所 ヒトゲノム解析センター 助教授を経て、1998年に東京医科歯科大学 難治疾患研究所 教授。2010年も同校硬組織疾患ゲノムセンター長(2014年3月まで)、2011年に同校学長特別補佐(2012年3月まで)、2012年に同校疾患バイオリソースセンター長、2014年に同校副理事(研究担当)、2016年に同校大学院医歯学総合研究科 遺伝学領域長も務める。専門は分子細胞遺伝学、遺伝医学、腫瘍遺伝学。
田中 敏博(たなか としひろ)
1966年、鹿児島県生まれ。1990年に東京大学医学部卒業。1996年に同校 大学院医学系研究科修了(医学博士)、1997年に同校医科学研究所 ヒトゲノム解析センター 助手、2000年に理化学研究所 遺伝子多型研究センター チームリーダー、2005年に同研究所同センター グループディレクター、2009年に同研究所 ゲノム医科学研究センター 副センター長。2013年に同研究所 統合生命医科学研究センター 副センター長(2016年3月まで)を併任しながら、2013年4月から東京医科歯科大学 疾患バイオリソースセンター 教授。専門は、循環器内科学、ゲノム医学、ゲノム疫学。
竹本 暁(たけもと あきら)
1982年、東京都生まれ。2007年に東京医科歯科大学医学部卒業。2012年に同校 疾患バイオリソースセンター 特任助教。専門は、人体病理学分野。
掲載日 平成30年4月16日
最終更新日 令和2年3月30日


