アーカイブ バイオバンク・ジャパン(BioBank Japan)

[取材協力]
東京大学医科学研究所 所長、教授 村上 善則先生
東京大学医科学研究所 特任教授 森崎 隆幸先生
我が国のいわゆる三大バイオバンクの1つ、バイオバンク・ジャパン(BBJ)は、2003年スタートという長い歴史と、疾患コホートとして約27万人分という登録患者数の多さで、世界的に見てもトップクラスを誇る、世界有数のものだ。約27万人分の試料や詳細な臨床情報データベースを提供することで、エビデンスの強い“日本発”の研究成果につなげ、国民に還元することを目ざしている。
長い歴史と規模の大きさ 世界トップクラスのバイオバンク
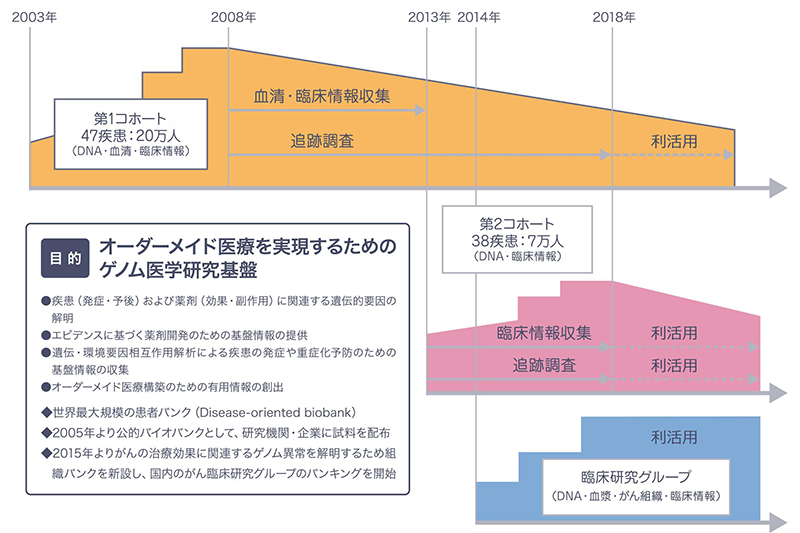
手術時に切除した組織などを研究目的で医療機関が保存することは以前からあったが、今日のように、疫学的に意味のある数の試料を最初からその目的で収集・保管・提供するバイオバンクは、ヒトゲノム計画と足並みを揃える形で登場してきた。そのうち、BBJは文部科学省のオーダーメイド医療実現化プロジェクトとして開始され、5年ごとに実施計画を見直し、2018年4月からは構築も新たに再出発した(図1)。
大規模バイオバンクとして古いのは、ヒトゲノム計画が進行中の1990年代後半にスタートしたアイスランドの国民を対象にした家系付きコホート「deCODE」のもので、登録者数は当時の同国・全人口となる約27万人。その次に、ヒトゲノム解読終了宣言がなされた2003年にスタートしたスウェーデンのKIバイオバンク(登録患者数・約28万人)とBBJ(登録患者数・約27万人)が並ぶ。
先駆者としての先見性の高さが、高品質な研究成果還元への源

BBJの現在の研究代表者であり、試料が保存され、事務局が置かれている東京大学医科学研究所の所長を務める村上善則教授は「BBJの特徴は、何と言ってもその歴史と規模、長期間追跡型の疾患コホートであること。そして、付随する臨床データの質の高さ」という。世界的にもわずかな前例しかない中、全国の12医療機関(72の医療施設)と共同で、研究利用同意を得た、51疾患、約27万人のDNA、血清(第1コホートのみ)、カルテ情報に基づく計5,800項目を超える臨床データを収集してきた。疾患は糖尿病や高脂血症(脂質異常症)などといった生活習慣病、各種のがん、白内障など、いわゆる"common disease"と呼ばれるものの441,557症例(2018年5月7日時点)が中心だ(図2、3)。多くの疾患に対して日本での患者数の1%に相当する人数の試料が集められている(うつ病など、ごく一部の疾患は除く)。これだけの試料および臨床データ数に加えて、10年を超える追跡データを用意したことの意義は大きい。
「疾患研究には最適なデータのはず」と村上所長は語る。
「糖尿病や高血圧症などの場合、診断されてもそのまま社会生活を続ける方がほとんどです。そのままの状態でいくか、年齢とともに状態が悪化していくのか──これは、国レベルでは大きな問題です。悪化する場合、どういう方向に進むのか。例えば糖尿病ならば、その後に腎臓が悪くなる人、神経にしびれが出る人、網膜症になる人と、おもにこの3つのタイプがあります。(BBJの登録患者数と追跡データがあれば)それぞれの疾患において、診断後どのような経過をたどるのかを解析し、検討することが可能になります」(村上所長)。
バンクによっては、臨床データがあるといっても、実際にはカルテ番号が添えられているだけの場合もあるという。こうなると、データを使う研究者は1つ1つカルテ情報を開いて、知りたい項目を探さなければならない。BBJの臨床データの質の高さ、そして、使い勝手の良さは、カルテ情報を詳細にデータ化し、すぐに取り出せるようにしたことに裏打ちされている。「住民コホートでは、(回答への労力などから)登録者へのアンケート設問数に限りがあります。10ページぐらいですと100から200項目が限度でしょう。内容も、例えば『血圧を下げるお薬を飲んでいますか』に『はい/いいえ』で答えるだけのこともあります。BBJのデータはカルテ情報をもとに記入しているので、具体的な薬の名前や服用量まで入っています。臨床データは各疾患共通のものとして2,500項目あり、それに加えて、疾患ごとに特徴的な情報も調査していますので、全体で約5,800項目になっています」(村上所長)。この調査票の内容は、「オーダーメイド医療の実現プログラム」のWebサイト「調査票」のページで確認できる。
BBJの強みである追跡調査は、苦労したところでもある。バンク登録は診断名が確定してから病院を通して行われるが、1人の患者が、ずっと同じ病院に通い続けるとは限らない。例えば特定のがんの場合、専門病院に転院することは珍しくない。糖尿病や高脂血症(脂質異常症)といった生活習慣病患者の場合は、長期間、普通に社会生活を送ることができるため、転居などに伴い、通う病院が変わったりする。そのようなケースに対して、BBJでは、(登録への同意取得以降)協力医療機関を受診されていない方への研究のための追跡調査(生存の確認)を、倫理審査後、内容の周知と拒否機会の確保を行った上で実施してきた。 日本には、米国のNDI(National Death Index)のような、学術研究のための生存確認に利用できる死亡統計データベースが存在しない。 よって、BBJは生存確認(お亡くなりになっていた場合には、死因情報を参照する『人口動態統計死亡データ』に紐づく、死亡年月日の確認)に必要な公文書請求を正当な理由をもって自治体に行ってきたが、1000件に数件の割合で拒絶されたという。 森崎隆幸特任教授は、この調査に関わる法制度的な難しさなどがあると語った。(詳細は、資料1を参照)
登録から10年を超えると「残念なことに亡くなる方も出てきます。私たちは死因も情報に加えています。(登録時に診断された)最初の疾患で亡くなられたのか、併発した合併症で他界されたのか、厚労省・人口動態統計での死因分類表に則って記載しています」(村上所長)。この追跡を約27万人に行うことの苦労をいとわない理由は、何より研究における有用さを見定めているからだ。
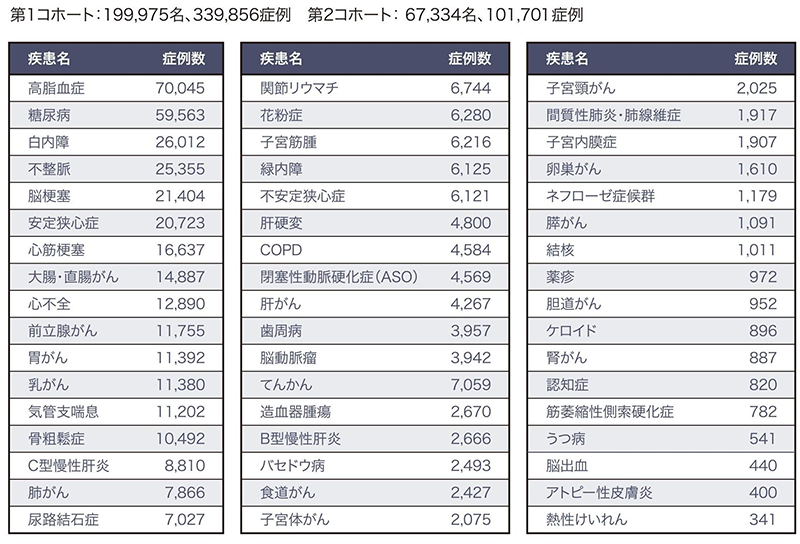
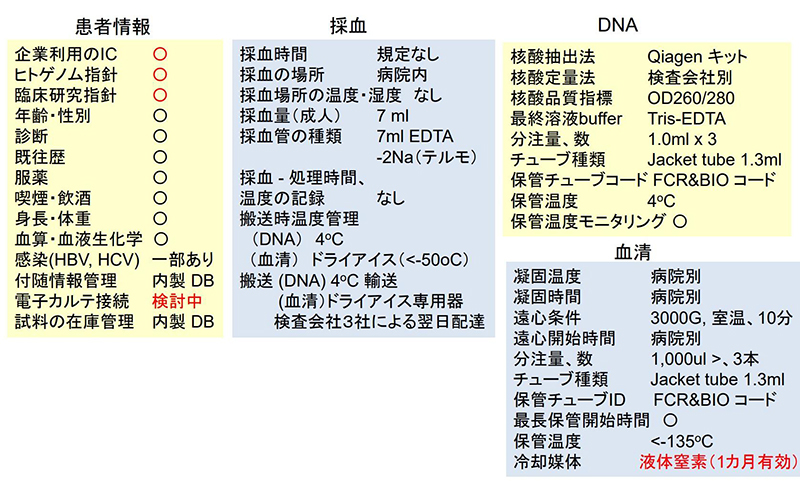
(出典:「第2回ゲノム医療実現のための研究基盤の充実・強化に関する検討会」資料(2017年4月21日))
分譲・共同研究申請手続きの合理化で、研究者へスピーディーな試料提供を目ざす

「研究のためにと多くの登録患者がご協力くださったのですから、(研究に)使ってもらわなくては『何のために集めたのか』となってしまいます」と森崎特任教授は語る。2018年度からの新しいBBJでは、試料の利活用のための保管、配布を引き続き行うが、分譲やデータ提供の手続き合理化など、試料やデータをもとに"研究しやすいシステム作り"にも注力している。
その1つが、研究者の提供申請から、実際に提供するまでの時間短縮化だ。現在、申請を承認するプロセスの見直しを行っており、2018年秋には、短縮化された新システムでの運営に移行する予定だ。2018年3月末までに、産学・計36機関に試料配布しているが、これを加速させたいと考えている。
※ なお、2018年9月現在、試料配布は、国内に法人を所有する機関に対して、配布された試料を国内で使用する場合に限って行っている。
研究者の立場から、提供を受けるまでの手順を見てみよう。まず、BBJサイト上から「保有試料検索システム」に入る(要事前アカウント申請)。ここから、BBJが保有する試料について「試料種別」「性別」「登録時年齢」「登録疾患名」「喫煙歴」「飲酒歴」「ゲノムワイド関連解析(Genome-Wide Association Study:GWAS)データの有無」を条件項目として検索でき、自分の研究に必要な試料やデータが何人分あるか調べられる。例えば、年齢の並び替えはもちろんのこと、収縮期血圧140mmHg以上/未満に区切る、高血圧症と心筋梗塞との併発例数をAND検索から調べるなどができる。
研究の目的や手法が具体的になったなら、研究計画書を添えてデータや試料の提供をBBJに申請する。これに対して試料等利用審査会による研究計画の妥当性や申請者側の研究実施体制等の審査がなされ、試料提供が認められる。必要に応じて、申請者の所属研究機関での倫理委員会承認取得も同時並行で行ってもらう。申請から承認まで1~2カ月程度かかるが、「1つが終わってから次のステップを始めるという形ではなく、(次の審査プロセスも)ある程度、同時に進めることで、研究者を待たせしないようにしたい」(森崎特任教授)。DNA配列データなどだけであれば、比較的すぐに提供できるという。詳細な臨床データや血清試料、組織試料を求める場合には、共同研究とすることもある。製薬会社のような企業にも分譲可能となるICを取得しており、配布された試料を使用して生じた特許等知的財産権については、全て研究機関や企業に帰属する対応としている。
試料の保存方法改善と情報化に挑む
さらに、試料を最大限に活かす工夫も進めている。これまで血清は1mlずつ3本のチューブで保存していたが、使う側からすると必ずしも1mlは必要でない場合が多い。しかし、余った分は品質の観点から再利用されずに処分されてしまう。この損失を最小化するためにBBJでは現在、一部の疾患について0.1mlずつ30本のチューブへと分注し直す作 業を進めている。「保存すべきチューブの本数が10倍になって、スペースなどの面でコストがかさみますが、利便性を優先しました」(森崎特任教授)。

写真3:NBDC研究データ検索画面
DNAに関しては、塩基配列をデータ化することでimmortalization(情報化)も進めてきた。「試料は分与して、なくなったら、終わり。でもデータ化すれば、何人に提供してもなくならない」と村上所長。研究者にとっても、データ解析から始められるというメリットがある。
BBJが2017年9月から科学技術振興機構(JST)バイオサイエンスデータベースセンター(NBDC)ヒトデータベース(写真3)を通じて公開で提供しているゲノムワイドの配列解析データ(集計データは非制限公開、個別データは制限公開)には2タイプある。
1つは、第1コホートのうち、20万人分のゲノムから90万カ所の一塩基多型(Single Nucleotide Polymorphism:SNP)をタイピングしたものだ。この90万カ所は国際的にもスタンダードとなっている位置で、遺伝的要因については網羅できると考えられている。このデータ提供を始めたところ、すぐに海外からメタ解析に使わせて欲しいという連絡が来たという。
もう1つは、1,000人分の全ゲノムシークエンスデータ(2018年8月公開)で、5種類の疾患(乳がん、大腸がん、前立腺がん、心筋梗塞、薬疹)の患者を対象にしている。BBJでは2019年度までに、あと2,000人分を追加したいと考えている。
それまでに使えたゲノムデータの多くは欧米人のもので、"人類全体"を語るには偏りがあった。そこに登場したBBJのゲノムデータは、大いに利用され、国際共同研究の成果としてNatureに9報、Nature Geneticsに60報が発表されている。疾患ごとの専門誌なども含めると国際誌だけで385報にのぼる(2017年12月末現在)。内訳は、がんやリンパ腫などの腫瘍性疾患は47報、骨粗鬆症や関節リウマチなど骨・結合組織疾患は47報、心筋梗塞や脳梗塞などの心疾患・脳血管疾患は25報などだ。2007年以降は毎月1~数報、2017年に至ってはほぼ毎週1報が発表されている計算になる。これだけの数の研究に使われたことが、BBJの試料やデータが評価を得ていることの何よりの証しだろう。
2018年に入ってからもBBJデータを使った研究成果は相次いでいる。例えば一般メディアもこぞって報道した日本人のアルコール代謝や栄養代謝の遺伝的変異に関する研究(参考資料2)などがある。こうした研究は、同じ配列を繰り返し読む、高深度で配列を読んだからこそできた解析だ。
未来を見据えた倫理的課題への対応、ELSI検討委員会 ~社会との信頼構築に向けて

「15万人もの参加者からいただいた貴重な試料や情報を、無駄にしたくない」。これは櫻井先生だけでなく、TMM計画メンバーの総意だ。「無駄にしたくない」には2つの思いが込められている。1つは、参加者に健康調査の結果などの情報をお返しして自身の健康に役立ててほしいという意味だ。「健康調査結果は、できるだけ速やかにお戻しするように意識しています。また、地域による結果の違いなどを示しながら改善策に活かしていただこうと、各地で説明会を開いています」(櫻井先生)。
もう1つの意味は、得られたデータを多くの研究に活用することだ。全ゲノムインピュテーションサービスはその一環だが、データの分譲や共同研究を通じて知見を積み重ねたいとしている。櫻井先生は、「(研究の中で)得られた知見を、さらに地域に返す循環を続けることが大事です。地域の健康支援、国のゲノム研究基盤の構築、個別化医療に向けた取り組みと、1つの研究室レベルでは到底経験できない大事業だからこそ、多くの研究者や職員と協力して推進していきたいと思っています」と取り組みへの意気込みを見せた。
研究プロジェクトのマネジメントには、日本医療研究開発機構(AMED)への出向経験が生かされているという。出向時の業務は、研究の計画立案・実施等の進捗管理、連携プロジェクトの調整やデータシェアリングの推進など、多岐に渡った。櫻井先生は「その経験があったからこそ、今の業務にやりがいを感じられている」と笑顔を見せた。
メディカルコーディネーターやプログラマーの登用が下支えに
バイオバンク運営のノウハウにも先鞭をつけてきた。BBJの先見性をよく物語るエピソードに、メディカルコーディナーター(MC)の存在がある。その役割は、バイオバンクへの協力を検討されている方々に、研究に関する必要な情報をわかりやすい提供し、自由な意思で、協力の可否を決めてもらうための支援だ。プロジェクト開始当時から予算をつけて各医療機関にMCを配置し、その人材養成を行ってきた。その数は2,000人に及ぶ。雇用の予算の出所はBBJであったが、MCは協力する医療機関の所属とした。「国費によるサポートがなくなっても、MCを有する病院は優遇されるようなシステムが社会に確立し、制度として自立できることを期待しました。残念ながら15年間ではそこまでは進みませんでしたが...」と村上所長は残念さと今後への期待をにじませた。
プロジェクトがスタートした2003年はまだ電子カルテが普及する前。400床以上の大規模病院での電子カルテ普及率は、2002年段階2.9%にすぎなかった時代だ(参考資料3:健康・医療・介護分野におけるICTの活用について(厚生労働省))。このため、MCは紙カルテに書かれた情報を電子データへ入力する作業も担っていたという。
しかし、手作業では。数字入力の全角・半角混在や入力ミスなどが起きる。「血液検査データの(基準値は4.0以上とされる)アルブミンで、4.5と入力すべきところを間違えて45と(ありえない数値)で入力されていたりすると、人的チェックを働かせなければ、平均値が滅茶苦茶になってしまいます。万単位、十万単位のデータでのクオリティコントロールにおいて、データクリーニングは必須」と村上所長は強調する。そのため、BBJでは常勤のコンピュータープログラマーが、データクリーニングを担ってきた。
走りながらの改善、壁は維持コスト

「2つのやり方があると思います。予想される課題をあらかじめすべてつぶしておいてからスタートさせる方法と、走り始めて、課題が現れるたびに、その都度、一つ一つ対処して改善していく方法。BBJは後者です」(森崎特任教授)。先に述べた血清試料の分注し直しがそれに当たるだろう。
試料の取り出し部分に関しても、新たな試みを始めている。4℃で保存しているDNAバンク(写真5)は、2次元バーコードとロボット技術のおかげで、試料の取り出し、提供用チューブへの分注、試料をもとの棚への再収納をすべて全自動化した。収容能力は200万本だ。
一方で、血清や血漿などは液体窒素が入ったマイナス150℃のタンク・58台(収容能力334万本)で保管している。この低温になると、霜が大敵となって機械化が難しいという。このため、必要な試料が入ったタンクの蓋を開けて試料を取り出すという作業を人が行っており、DNAに比べて提供までにどうしても時間がかかってしまう。
そこで、BBJでは窒素ガス100%、湿度0%の状態で組織試料を48万本収容できる保管装置(写真6)・12台とシステムを日本企業から導入した。水蒸気が発生しないので霜がつかず、完全自動化で取り出しなどが行える。もちろん、バイオバンキングのために日本でゼロから開発されたシステムだ。すでに何台かは稼働しており、がん組織などの特に重要と思われる試料はこちらに移している。素早い試料提供を考えるのであれば、この完全自動化できる保管庫は優れているが、維持コストが10倍近くかかるため、すべての試料を移していない。

なお、「オーダーメイド医療の実現プログラム」Webサイトの「バイオバンク・バーチャルツアー」では、バンク施設に関する動画を公開している。
資金もスペースも有限な中、どこが最適であるのかは、運営しながら都度、改善していくことになるだろう。分譲希望の件数が今後どのように推移していくかによっても、その"落としどころ"は変わってくるだろう。
田畑に例えれば開墾から始まったBBJは、実りを享受できる収穫の時期に入ったといえる。今後、ゲノム情報を用いた医療が広がりを見せる中で、さらなる利活用が期待される。
しかし、日本初のバイオバンクとして大規模な試料収集とシステム創設を見事にこなしたBBJだが、特に試料保存と利活用を推進しうる運営に関しては、前例のない挑戦が続く。
新たな試料登録を行わないことから、2018年4月からはMCに対する予算はつかず、アウトリーチ活動も1つの区切りを迎えた。それぞれの仕事に携わっていた人は、ほかのバイオバンクやゲノム情報を利用した医療に活躍の場を移すことになるだろう。だが、登録患者や社会に対する説明責任は、BBJの先見性が際立っていた部分であった。その縮小による影響について見定めることも、先駆者だからこそできることだろう。
インタビュー映像
研究者経歴
村上 善則(むらかみ よしのり)
1958年、大阪市生まれ。1983年に東京大学 医学部 医学科 卒業。同年から東京大学医学部附属病院第一内科 医員を勤め、1992年に医学博士(東京大学)。1992年に米国ユタ大学ハワードヒューズ研究所研究員、1994年に国立がんセンター研究所 室長、2000年に同研究所 プロジェクトリーダーを経て、2007年より現職。専門分野は、分子遺伝学。
森崎 隆幸(もりさき たかゆき)
1956年、香川県生まれ。1980年に東京大学医学部医学科卒業。内科臨床研修後、1984年3月に東京大学医科学研究所助手、1986年1月に医学博士(東京大学)。1987年11月より米国デューク大学医学部研究員、助教授、米国ペンシルバニア大学医学部助教授。1994年6月より国立研究開発法人国立循環器病研究センター(旧国立循環器病センター)にて室長、部長、東京工科大学 医療保健学部 教授を経て、2018年4月より現職。専門分野は、分子遺伝学、臨床遺伝学、内科学。
関連リンク
参考資料
- 参考資料1
「本人通知制度の実態と住民票を用いた予後調査への影響の検討」
永井亜貴子,武藤香織,井上悠輔.本人通知制度の実態と住民票を用いた予後調査への 影響の検討.日本公衆衛生雑誌,2018; 65(5): 223-232.
https://www.jstage.jst.go.jp/article/jph/65/5/65_17-071/_pdf/-char/ja/ - 参考資料2
Blood lipid-related low-frequency variants in LDLR and PCSK9 are associated with onset age and risk of myocardial infarction in Japanese.
Tomoyuki Tajima, Hiroyuki Morita*, Kaoru Ito*, Tsutomu Yamazaki, Michiaki Kubo, Issei Komuro, Yukihide Momozawa
Blood lipid-related low-frequency variants in LDLR and PCSK9 are associated with onset age and risk of myocardial infarction in Japanese.
掲載日 平成30年10月19日
最終更新日 令和2年3月30日


